*仅供医学专业人士阅读参考


如果直到现在,你还单纯地认为骨头的作用是支撑身体的一根梁,那就大错特错了。最近的研究发现,骨骼除了支撑身体、保护软组织器官和促进运动等作用外,还可能是一个内分泌器官。
虽然骨骼看上去与柔软的内分泌器官并不沾边,但是它确实可以分泌多种细胞因子,比如骨钙素、成纤维细胞生长因子23、骨保护素等,参与骨或非骨器官的稳态的调剂。
随着年龄增长,内分泌稳态发生变化,各种神经内激素水平变化影响着大脑神经元的衰老和死亡。与此同时,来自其他器官的激素水平变化也有可能对大脑产生影响。
近日,南京大学医学院附属鼓楼医院的郭保生、蒋青与石云团队,发现了骨细胞分泌的硬化蛋白(Sclerostin)与大脑衰老和β-淀粉样蛋白(Aβ)之间的关系。他们发现,这种骨硬化蛋白可以穿过老龄小鼠的血脑屏障,高水平的骨硬化蛋白导致Wnt-β-catenin通路失调,加速Aβ的产生和积累,损害老龄小鼠的突触可塑性和记忆力。
研究发表在《自然·代谢》上。

骨硬化蛋白主要由成熟的骨细胞分泌,在骨代谢过程中起到调节作用,也是Wnt-β-catenin通路的拮抗剂。骨硬化蛋白水平升高常见于骨质疏松患者,其他疾病,比如2型糖尿病、肝病、肾脏疾病等患者也可以观察到血清骨硬化蛋白水平较高,还会随年龄增长而逐渐升高,因此研究人员猜测,骨硬化蛋白失调可能对骨组织之外的器官产生影响,甚至有可能影响到大脑功能。
Wnt-β-catenin通路在成人神经系统中也发挥着重要作用,与突触可塑性和记忆有关,在衰老和AD进展期间,也可以观察到Wnt-β-catenin通路活性减弱,激活Wnt-β-catenin通路可以改善病理相关突触功能受损。在本次研究中,研究人员将22月龄和12月龄小鼠进行对比,发现骨硬化蛋白可以穿过22月龄小鼠的血脑屏障,引起大脑中的骨硬化蛋白水平显著增加,导致Wnt-β-catenin通路失调。

骨硬化蛋白在衰老过程中介导大脑Wnt信号信号失调
通过转基因技术构建骨硬化蛋白水平升高的小鼠模型(TG),可以发现,与野生型小鼠相比,12月龄的TG小鼠记忆和空间探索能力下降,皮层和海马区域棘突数量减少,18月龄时就表现出严重的突触损伤。
接下来,研究人员构建了骨硬化蛋白缺失的小鼠模型(cKO),18月龄的cKO小鼠表现出比野生型小鼠更好的记忆和空间探索能力;同样,降低老龄小鼠的骨硬化蛋白水平,也可以改善小鼠的认知和突触功能。
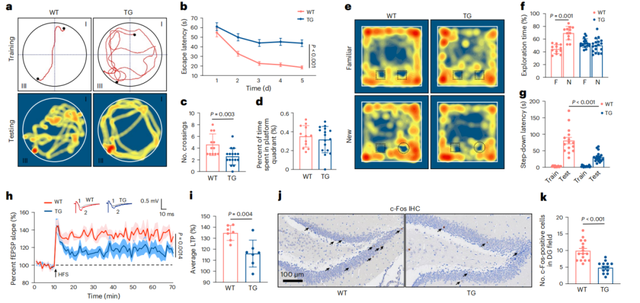
高水平骨硬化蛋白影响小鼠认知和突触功能
但是,骨硬化蛋白对AD进展的影响并不是通过破坏血脑屏障实现的,12月龄小鼠的血脑屏障并没有被明显破坏的痕迹。研究人员的下一个备选的猜测是骨硬化蛋白通过影响Aβ的产生途径参与AD进展。
果然,研究人员发现TG小鼠皮质和海马中β-catenin水平较低,BACE1水平较高,骨硬化蛋白通过抑制Wnt-β-catenin通路促进BACE1表达和Aβ形成。
在AD小鼠模型中,研究人员通过尾静脉注射上调骨硬化蛋白水平,注射2个月后,小鼠血清和脑组织中的骨硬化蛋白水平升高,皮质和海马均受到影响,Aβ40和Aβ42的浓度增加,Aβ沉积也明显增多,骨硬化蛋白通过促进Aβ产生加快了AD小鼠的疾病进展。
抗骨硬化蛋白给药可以改善老年小鼠和高骨硬化蛋白水平下AD小鼠的记忆受损,还可以减轻小鼠的骨密度下降和骨微结构恶化。

高水平骨硬化蛋白与老年人群和AD患者的认知功能障碍有关
在老年人群中,血清骨硬化蛋白水平与认知功能评分呈负相关,血清骨特异性碱性磷酸酶水平也根据根据认知功能评分不同而有明显区分,说明高水平血清骨硬化蛋白水平与老年人骨代谢紊乱和认知功能受损有关。同样,在AD患者中有观察到血清骨硬化蛋白水平与认知功能评分呈负相关,并且与血清Aβ水平呈正相关。
骨代谢紊乱和认知功能受损都是常见的衰老相关器官功能失调。在这项研究中,研究人员揭示了骨硬化蛋白对衰老和AD进展过程中认知功能的影响。骨细胞来源的硬化蛋白水平异常升高使大脑Wnt-β-catenin通路失调,加速病理条件下的认知功能下降。研究为骨细胞生物学与神经退行性疾病之间的联系提供了坚实的依据,对预防或治疗AD及其他年龄相关疾病具有广泛影响。
参考文献:Shi T, Shen S, Shi Y, et al. Osteocyte-derived sclerostin impairs cognitive function during ageing and Alzheimer’s disease progression[J]. Nature Metabolism, 2024: 1-19.
本文作者丨王雪宁
