*仅供医学专业人士阅读参考


肠道功能障碍是帕金森病(PD)的一种常见的运动前症状,并与疾病的快速进展有关。此前的研究发现,肠道微生物的失调影响PD的病理和症状,针对肠道微生物的干预措施,如粪菌移植(FMT),在PD动物模型中表现出对症状的改善和潜在的神经保护作用。
已经有一些随机临床试验显示出益生菌能够改善PD的便秘症状,至于FMT,只有一些小型的和无对照组的研究显示出运动和非运动症状的改善和安全性,但这类研究证据的强度不足。
因此,芬兰赫尔辛基大学医院的研究团队开展了一项双盲、安慰剂对照、随机临床试验,他们发现,FMT的安全性较好,但是相比安慰剂,6个月时,运动障碍协会统一帕金森病评定量表(I-III部分)评分的变化没有具有临床意义的改善。研究结果发表在《美国医学会杂志·神经病学》上[1]。

这项临床试验在芬兰的3家大学附属医院和1家地区医院进行,招募了有轻至中度运动和/或非运动症状、肠道微生物失调的PD患者,以2:1的比例随机分配至单次FMT组或安慰剂组,经结肠镜进行,参与者接受了聚乙二醇溶液全肠灌洗,未接受抗生素预处理。
试验的主要终点为随访第6个月时,运动障碍协会统一帕金森病评定量表(MDS-UPDRS)I-III部分(日常生活非运动症状体验、日常生活运动症状体验、运动功能)评分总和,第III部分运动功能在非用药状态下评估,即最后一剂左旋多巴给药后至少10小时和最后一剂多巴胺激动剂或单胺氧化酶B抑制剂给药后24小时。
在2020年11月至2022年5月之间,研究人员共筛选了229例PD患者,最终48例入组,47例接受了干预,46例完成了主要终点和12个月的随访,45例被纳入最终的意向治疗人群分析,FMT和安慰剂组分别有30例和15例。
在主要终点方面,FMT组和安慰剂组没有显著差异(评分总和差值为0.97,p=0.75)。在5个次要终点中,与安慰剂组相比,FMT组6个月时“起立-行走”测试所需的时间显著增加,12个月时非运动症状量表评分也显著增加,但6个月时左旋多巴等效日剂量(LEDD)显著减少,贝克焦虑量表(BAI)评分在1个月时显著下降,6个月时没有显著差异,蒙特利尔认知评估(MoCA)评分没有显著差异。
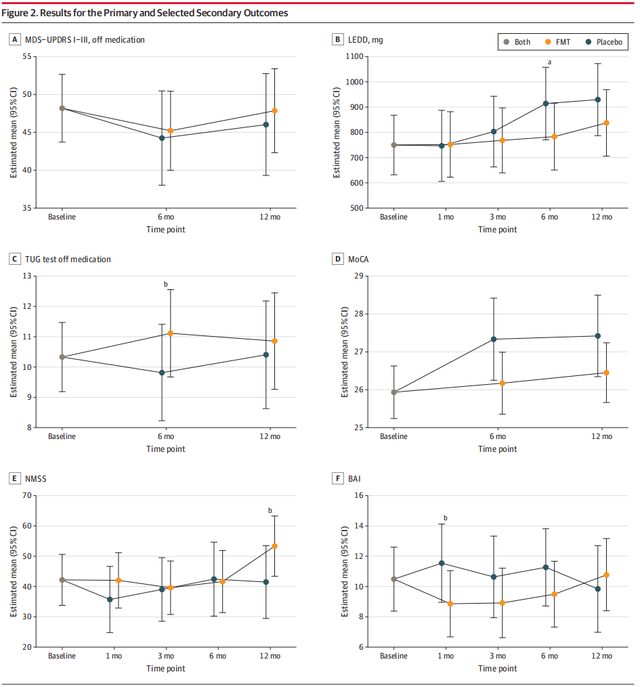
试验的主要和次要终点
6个月内,与FMT组相比,安慰剂组的完全排便和自主完全排便次数在多个时间点上显著增加。
除第12个月外,其余所有随访时间点上,FMT组的肠道微生物β多样性均显著高于安慰剂组。FMT组29例参与者中有7例(24%)在FMT 1个月后,肠道微生物失调状态得到有效转变,但在12个月时下降至只有1例(3%),安慰剂组中,这一比例在1个月时较低(13%,2/15),而在12个月时有所增加(33%,5/15)。

肠道微生物β多样性改善
FMT的安全性没有引起担忧,12个月内,FMT组和安慰剂组分别报告了105例和50例不良事件(AE),大多数与胃肠道功能障碍有关,在FMT组中更为常见(16[53%] vs. 1[7%]),除1例之外,均为轻至中度。共有3例严重AE,均发生在FMT组,研究人员判断与干预无关。
综上所述,FMT治疗PD是安全的,但PD症状没有出现有临床意义的改善。尽管肠道微生物的失调有所改善,但这并没有转化为临床或生物标志物的改善,甚至部分次要终点表现出恶化的迹象。
研究人员认为,这一阴性结果可能为未来的试验改进提供了重要参考,因为FMT在很多方面并没有达成共识,例如供体和受体的选择、粪菌制备的准备(有氧/厌氧、低温保护剂的浓度和移植量)、抗生素预处理和执行细节(移植至上/下消化道、单次/多次),即使是临床试验,最佳对照组(惰性安慰剂/自体粪菌移植)也尚未确定。
在同期配发的评论文章[2]中,评论人员肯定了这一点,并提出,未来,对FMT后肠道微生物组成与临床结果相关的交叉研究可能能够揭示与有益结果有关的肠道微生物,与益生菌和益生元临床研究相对照,可以确定共同的微生物特征和值得精准靶向的靶点,完善肠道微生物与PD之间的关联。
参考文献:
[1] Scheperjans F, Levo R, Bosch B, et al. Fecal Microbiota Transplantation for Treatment of Parkinson Disease: A Randomized Clinical Trial. JAMA Neurol. Published online July 29, 2024. doi:10.1001/jamaneurol.2024.2305
[2] Sampson TR. Fecal Microbiome Transplants For Parkinson Disease. JAMA Neurol. Published online July 29, 2024. doi:10.1001/jamaneurol.2024.2293
本文作者丨应雨妍
