

成果简介
近日,香港城市大学支春义教授、深圳大学郭瑛助理教授以及深圳先进技术研究院彭超副研究员(通讯作者)介绍了在酸性条件下利用具有低氢化活性的TiO2纳米片将硝酸盐选择性快速还原为氨的潜力。该研究表明,与铁酞菁杂化后的催化剂相比,TiO2纳米片催化剂通过增强对硝酸盐的吸附、抑制氢气的生成以及降低决速步骤的能垒,显著提高了氨的生成效率。随后,研究人员开发了一种碱-酸混合型锌-硝酸盐电池,其开路电压高达1.99 V,功率密度为91.4 mW·cm-2。 此外,该混合电池可用于环境硫回收,并可开发出同时进行肼/硝酸盐转换和发电的肼-硝酸盐燃料电池。这项研究证明了在酸性条件下利用硝酸盐还原合成氨,并为能源转换领域提供了新的可能性。
研究背景
氨(NH3)是化肥、制药和含氮化学品行业不可或缺的原材料。在 "氢能源 "和 "碳中和 "的背景下,NH3也成为一种理想的能源和氢载体,是一种具有高重力能量密度的交通燃料替代品。最近,用于合成 NH3的电化学硝酸盐还原反应(NO3-RR)受到了广泛关注。NO3- 在自然界,尤其是废水中具有良好的可获得性和丰富的含量。将 NO3- 转化为 NH3对处理含NO3-废水和 "变废为宝 "具有极大的吸引力。此外,由于 NO3- 在催化剂表面的吸附行为增强且活化能较低,NO3-RR 的 NH3产率和能耗分别远高于氮还原法和传统的 Haber-Bosch 工艺。因此,NO3-RR 对环境保护、绿色 NH3 生产和能源利用具有重要意义。
图文导读
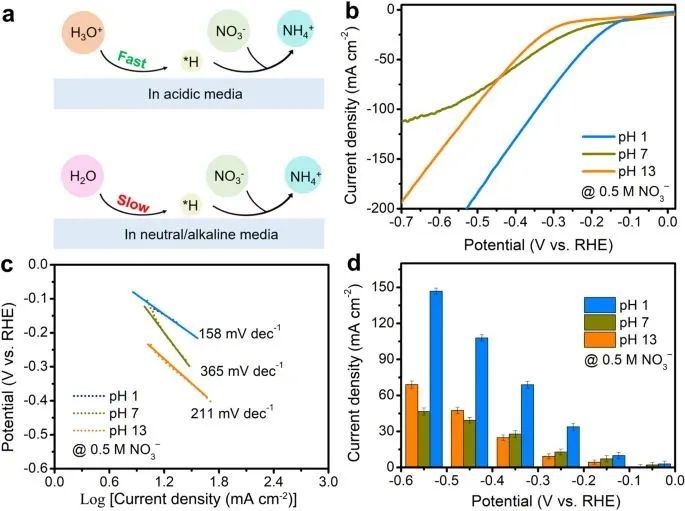
图1. 酸性介质可提高二氧化钛的 NO3-RR 动力学
根据碱性/中性介质中 NO3- + 6H2O + 8e- → NH3 + 9OH- 的反应方程式,NO3-还原反应涉及九个质子耦合电子转移,其中质子是通过额外的水解离步骤产生的(H2O → H* + OH*),这可能会导致过电势过大和动力学缓慢,从而限制 NO3-RR 的性能。 相反,与中性/碱性条件相比,在强酸性条件下直接还原硝酸盐具有独特的优势。TiO2 具有较差的 HER 活性和显著的耐腐蚀性,是一种适用于 NO3-RR的多功能电催化材料。作者首先探讨了TiO2 在酸性、中性和碱性条件下的 NO3-RR 性能。NO3-RR 在酸性介质(pH 值为 1)中的线性扫描伏安曲线显示出比在中性/碱性介质中更正的起始电位,而且在相同电位下,酸性介质中的电流密度总是高于中性和碱性介质中的电流密度。 然而,当电位较负时,碱性介质中的电流密度会超过中性介质中的电流密度,这是因为中性介质中的反应动力学速度较慢,塔菲尔斜率中显示的动力学速度较慢就是证明。TiO2 在不同电位和 pH 值下的 NH3 部分电流密度表明在相同的应用电位下,TiO2 在 pH 值为 1 时的 NH3 产率始终高于 pH 值为 7 和 pH 值为 13 时的产率,这表明酸性介质有助于更高的 NH3 产率。
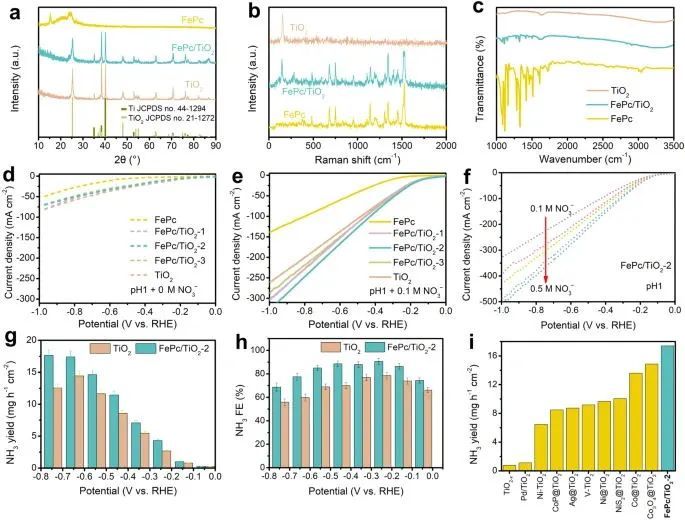
图2. TiO2 和 FePc/TiO2 的特性和 NO3-RR 电催化性能
由于 FePc 的含量较低,FePc/TiO2 的 X 射线衍射 (XRD) 显示出与 TiO2 相似的峰值。FePc/TiO2 的拉曼光谱显示了 FePc 和 TiO2的典型信号,傅立叶变换红外光谱的测量结果进一步证实了这一点。所有样品(包括 FePc、TiO2 和 FePc/TiO2-x)在不含 NO3- 的酸性介质(pH 值为 1)中都显示出较低的催化 HER 活性和较大的过电位, LSV 曲线验证了这一点,而催化电流密度则随着 NO3- 的存在而显著增加。与 TiO2 相比,FePc/TiO2-x显示出更高的电流密度,FePc/TiO2-2 显示出五种样品中最大的电流密度。 相比之下,FePc 在固定电位下的电流密度最小。随着 NO3- 浓度的增加,FePc/TiO2-2 的电流密度会进一步提高。在各种电位下,FePc/TiO2-2 的 NH3 产率和 FE 都比 TiO2 大。FePc/TiO2-2 比大多数已报道的基于 TiO2 的催化剂具有更高的 NH3 产率。虽然 FePc/TiO2-2 与最先进的 NO3-RR 电催化剂在高浓度 NO3- 高达 1 M 的碱性介质中的性能仍有差距,但可以肯定的是不含贵金属的 FePc/TiO2-2 在酸性介质中表现出更高的 NH3 合成性能。

图3.NO3-RR 电解过程中的 FePc/TiO2 分析
然后,作者分别在 -0.45 V 的电压下对 0.5 M 15NO3- 和 14 NO3-电解质进行电解,收集电解质后进行进一步分析。在核磁共振光谱中,15NH4+ 和 14NH4+ 分别出现了典型的双峰和三峰。此外,核磁共振方法最终得到的 NH3 产率和 -0.45 V 时的 FE 值分别为:14 NO3- 11.2 mg·h-1 cm-2 和 85.0%,15 NO3- 11.8 mg·h-1·cm-2 和 88.7%,与紫外可见光的结果接近,这表明测定 NH3 的实验数据是可靠的。 随着反应时间的延长,-0.25 V 时的最大 NH3 FE 值保持稳定。在不同电位下电解后,FePc/TiO2-2 的 XRD 图谱显示出与原始图谱几乎相同的衍射峰,表明 FePc/TiO2-2 具有良好的结构稳定性。随着电位变负,Ti 2p 区中 Ti4+ 的典型峰值略微向较小的结合能移动,这表明在 NO3-RR过程中可能会产生更多低价态的 Tix+。
在 N 1 s 光谱中,电解过程中观察到一个 408.5 eV 附近的新峰,该峰归属于吸收的 NO3-,以及 397 eV 附近的峰,该峰归属于表面 NH3 物种。 不过,随着电位变负,FePc 中分配给 Fe-N 的峰值会变弱。原位傅立叶变换红外光谱也被用来检测NO3-RR电解过程中吸附在催化剂表面的反应中间产物。当电位从 0 V 下降到 -0.55 V 时,FePc/TiO2-2 出现了几个峰,且强度增加。1634 cm-1 处的特征峰归因于薄层溶液中 NO3-RR所吸附水的弯曲振动,或由于峰的重叠而产生的 NO 中间体。1537 cm-1 处的波段可能是 NH2 的弯曲振动,而 1515 cm-1 处的波段则是 NO 的振动峰。 同时,以 1243 cm-1 为中心的吸收带则归因于 NO2 基团的对称和非对称伸缩振动。1150 cm-1 和 1100 cm-1 附近的吸收带分别是羟胺(NH2OH)的 H-N 伸展振动和生成的 NH3。在 FePc 上也观察到了类似的峰值。这些观察结果揭示了以下可能的 NO3-RR 途径:NO3- → *NO3 → *NO2 → *NO → *NOH → *NH2OH → *NH3。
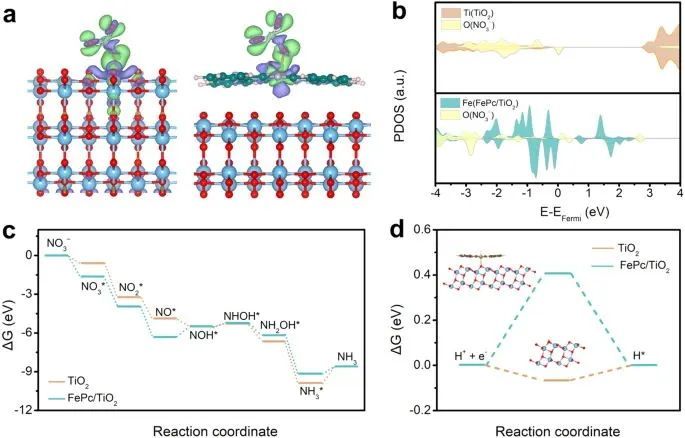
图4. 二氧化钛和 FePc/TiO2 上 NO3-RR 反应途径的理论计算
电荷密度差分析表明NO3- 和 Fe 位点之间存在明显的电荷转移。状态密度分析进一步证实了这一点,与 Ti-NO3 相比,Fe-NO3 的 d-p 轨道在费米级以下更负的能级上有很强的重叠,这表明 Fe-NO3 中的共价键成分更强。值得注意的是,FePc/TiO2 催化剂对 HER表现出惰性活性,证明了其卓越的抗 HER 能力。
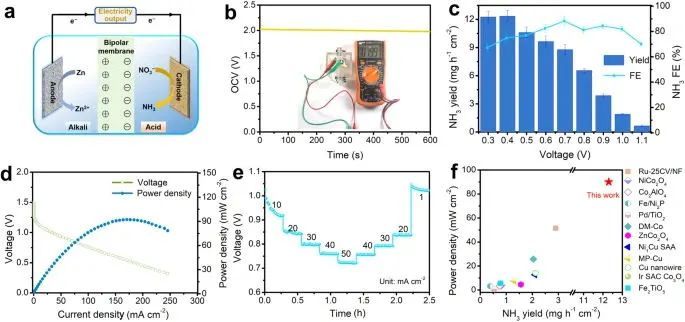
图5. 高压 Zn-NO3-电池,可同时将 NO3-转化为 NH3 并供电
作者随后组装了这样一个 AAHZNB 电池,以 FePc/TiO2-2 作为阴极(在酸性电解液中),以 Zn 板(在碱性电解液中)作为阳极。双极膜用于分隔阴阳极室。Zn-NO3- 电池可提供 1.99 V 的稳定 OCV,高于迄今为止报告的所有 Zn-NO3- 电池值。AAHZNB 在放电过程中,0.7 V 时的峰值 FE 为 88.2%,0.4 V 时的 NH3 产率高达 12.3 mg·h-1·cm-2。重要的是,AAHZNB 的峰值功率密度高达 91.4 mW·cm-2。 此外,团队还测试了 AAHZNB 的倍率性能。不同电流密度下的阶梯形放电曲线显示每一步都表现出稳定的放电平台。在高达 50 mA·cm-2 的电流密度下放电后,电压在 40、30 和 20 mA·cm-2的电流密度下都能很好地恢复,这表明 AAHZNB 具有很高的稳定性。因此,作者认为FePc/TiO2-2 所采用的 AAHZNB 可以达到 91.4 mW·cm-2的最大功率密度和 12.3 mg·h-1·cm-2的 NH3 产率,是目前所报道的 Zn-NOx- 电池中最高的。

图6. 用于环境硫回收的 AAHZNB 和用于发电和合成 NH3的 N2H4-NO3- 燃料电池
由于肼(N2H4)的氧化电位较低,还可以用它来替代硝酸电池中的锌阳极,实现燃料电池同时处理污染和发电。一个由阴极析氢反应和阳极硫氧化反应(SOR)组成的电解槽,该电解槽以商用 Pt/C 作为双功能催化剂,电流密度为 35.6 mA·cm-2。随着电解的进行,在 300 纳米处观察到紫外可见吸收带逐渐上升,这表明在电解过程中在无溶液中生成了短链 S22-。以 FePc/TiO2-2 为阴极的N2H4-NO3- 燃料电池示意图。作者使用商用 Pt/C 作为阳极催化剂,发现与 Ag/AgCl 相比,起始电位约为 -1 V,在 1 M KOH + 0.3 M N2H4 中电流密度达到饱和。HzOR 的起始电位比 NO3-RR 更负,表明 N2H4-NO3- 燃料电池是可行的。组装好的 N2H4-NO3-燃料电池在 1 mA·cm-2 时的放电电压为 0.75 V,峰值功率密度为 11.5 mW·cm-2。在不同电压下放电时,NH3 FE 保持在 80% 左右。
文献信息
Zhang, R., Li, C., Cui, H. et al. Electrochemical nitrate reduction in acid enables high-efficiency ammonia synthesis and high-voltage pollutes-based fuel cells. Nat Commun 14, 8036 (2023). https://doi.org/10.1038/s41467-023-43897-6
