引用格式:中华预防医学会. 我国婴幼儿呼吸道合胞病毒感染被动免疫预防专家共识[J]. 中华流行病学杂志, 预发表. DOI: 10.3760/cma.j.cn112338-20240826-00527.


中华预防医学会
通信作者:徐爱强;冯录召;谢正德

摘 要
呼吸道合胞病毒(RSV)是严重威胁婴幼儿健康最常见的病毒性病原体,引起的疾病负担重。为了更好地指导和规范我国婴幼儿RSV相关疾病的被动免疫预防工作,中华预防医学会联合多学科专家组成专门工作组,借鉴国外RSV被动免疫预防的实施经验,以问题为导向,整合了现有的证据和最新进展,形成了我国婴幼儿RSV被动免疫预防专家共识,旨在从技术上回答有关RSV感染及其免疫预防特别是被动免疫预防的一些专业问题,以期为各级医疗机构、疾病预防控制机构和基层医疗机构专业人员的免疫预防实践提供参考。
【关键词】婴幼儿;呼吸道合胞病毒;特异性免疫;被动免疫;专家共识

前 言
呼吸道合胞病毒(respiratory syncytial virus, RSV)是婴幼儿最常见的呼吸道病原体之一,也是5岁以内儿童急性下呼吸道感染(acute lower respiratory tract infection,ALRTI)最常见的病毒性病原体之一。RSV自然感染无法获得持久免疫力,仍会反复感染[1],故特异性免疫预防至关重要。20世纪60年代,国外就已开始RSV疫苗研发,然而在临床试验阶段却发现接种福尔马林灭活的全病毒RSV疫苗的儿童在随后首次自然感染RSV时,导致增强的呼吸道疾病(enhanced respiratory disease,ERD)现象发生,使得后续60余年的RSV疫苗研发进展缓慢 [2]。近年来,随着RSV免疫相关基础理论的突破进展和研发技术的不断提高,国外用于成年人特别是孕妇接种的RSV疫苗和婴幼儿RSV长效单克隆抗体(RSV长效单抗)研发取得成功,其中一种婴幼儿RSV长效单抗进口产品已于2023年12月在我国获批上市,使我国婴幼儿在RSV流行季获得特异性被动免疫预防保护成为可能。
目前,部分国家已发布了针对RSV长效单抗在婴幼儿中使用的被动免疫指导策略。为了更好地指导和规范我国RSV相关疾病的被动免疫预防工作,中华预防医学会联合流行病学、免疫规划、病毒学、儿科学、感染病学等领域的专家组成专门工作组,自2022年开始,多次组织相关研讨,分析国内外RSV感染的现状与趋势,跟踪国外针对RSV相关疾病免疫预防的研究进展,借鉴国外免疫预防的实施经验,探究我国今后一个时期内婴幼儿RSV被动免疫预防的策略。在参照国际上临床实践指南和专家共识撰写标准和流程的基础上,以问题为导向,整合了现有的证据和最新进展,形成了我国婴幼儿RSV被动免疫预防专家共识,旨在从技术上回答有关RSV相关疾病及其免疫预防特别是被动免疫预防的一些专业问题,以期为各级疾病预防控制和医疗机构、基层医疗机构专业人员的免疫预防实践提供参考。根据GRADE(Grading of Recommendations Assessment,Development and Evaluation)分级原则,本共识的证据等级分为高质量A(进一步研究不大可能改变对该评估结果的信心)、中等质量B(进一步研究有可能对该评估结果的信心产生重要影响)和低质量C(进一步研究很有可能影响该评估结果,且该评估结果很可能改变)3个级别;推荐强度分为强推荐1(充分考虑到证据的质量、接种的收益和不良反应,接种后产生好的效果,有较高的成本效益比)和弱推荐2(证据价值参差不齐,推荐意见存在不确定性,或推荐的意见可能会有较差的成本效益比等,更倾向于较低等级的推荐)2个级别。本专家共识并非强制性要求,且随着今后研究进展和新证据的出现将不断更新。
一、
婴幼儿RSV感染免疫预防的重要性和必要性
技术问题1.
为什么尽早对婴幼儿RSV感染实施免疫预防尤为重要?
专家共识1.
婴幼儿特别是1岁以内婴儿感染RSV后引发重症或导致长期不良影响的风险高,且缺乏特异性的抗RSV治疗药物可用,非药物干预措施对该人群效果不理想,有必要对婴幼儿群体尽早实施针对RSV的免疫预防措施。(A1)
RSV是世界范围内5岁以下儿童呼吸道感染最常见的病原体之一,严重危害儿童健康。据估计,2019年全球5岁以下儿童中,RSV相关ALRTI的发病人数达3 300万、住院人数达360万、院内死亡人数达2.63万例,可归因于RSV的总死亡人数共有10.14万例[1]。其中,1岁以下婴儿因免疫系统和气道发育尚不成熟,承受着最沉重的疾病负担,在因RSV相关ALRTI发病、住院和死亡的5岁以下儿童中,1岁以下婴儿占比分别约为40%、75%和82%[1,3-7]。尽管具体原因和机制尚有待明确,但大量研究显示:小月龄婴儿更易感染RSV,且感染后病情更为严重,新生儿感染RSV后更易发展为重症,其重症率可达32.3%;0~2月龄婴儿感染RSV后住院率是2岁以下其他年龄组的3.0~5.5倍,ICU住院率是其他年龄组的1.5~2.0倍,机械通气率是其他年龄组的4.0倍;且小于1月龄新生儿RSV相关死亡率也远高于1岁以下婴儿[8-10]。
几乎所有婴幼儿都感染过RSV,即使是出生健康的婴幼儿,一旦感染RSV也有较高发病风险。我国北京地区2011年血清流行病学研究结果显示,超过71%的小于6月龄婴儿感染过RSV,超过84%的婴儿在1岁前感染过RSV [11];国外有报道显示,超过95%的婴幼儿在2岁前感染过RSV [12]。大多数因RSV感染住院的婴儿是无基础疾病的婴儿,研究显示RSV住院患儿中92.7%为足月出生且无任何基础性疾病的婴幼儿[13]。新生儿重症监护室、产后月子中心、托儿所、幼儿园等场所中,容易发生聚集性疫情,婴幼儿RSV感染率可达23.8%~76.2% [14-17]。此外,婴儿期RSV感染还与后期的反复喘息和哮喘等的发生有关。一项Meta分析显示 [18],相较于未感染过RSV的儿童,婴儿期曾感染RSV儿童反复喘息的风险增加约2倍。一项量化生命早期RSV住院治疗与随后哮喘诊断之间联系的Meta分析显示,婴儿期感染RSV接受住院治疗的儿童,哮喘风险增加约3倍 [19]。一项回顾性研究探索RSV感染对医疗资源负担长期影响的结果显示,感染过RSV的婴儿在感染后的5年内每年就诊次数增加9次以上,每年因呼吸系统事件就诊次数增加3次以上,每年因哮喘/喘息事件就诊次数增加1次以上[20]。
RSV的传播途径主要为呼吸道飞沫传播和接触传播,特定条件下可通过气溶胶传播 [21]。对于大龄儿童、青少年和成年人可采取标准的手卫生、减少外出次数、保持社交距离、佩戴口罩等非药物干预手段,降低RSV感染风险。但是对于婴幼儿难以有效实施上述预防手段,故RSV的特异性预防显得尤为重要。
我国目前尚未将RSV相关疾病纳入法定报告传染病,也缺乏全国性流行病学监测和实验室检测的数据,但一些基于疾病预防控制中心(CDC)长期监测数据的研究显示,RSV也是我国婴幼儿呼吸道感染最重要的病原之一 [22-23]。中国CDC一项超过10年(2009-2019年)急性呼吸道传染病(acute respiratory infection,ARI)监测结果显示:RSV是5岁以下儿童ARI患者中最常见的病原体(占25.7%),其次为鼻病毒(占17.4%)、副流感病毒(占15.8%)、流感病毒(占14.2%)等;在儿童肺炎患者中,RSV阳性率同样位居首位(占28.1%)[2]。2009-2023年我国16个省份开展的ARI监测报告显示:ARI病例中RSV阳性检出率为10.83%,其中87.95%为5岁以下儿童,且小于6月龄患儿的检出率最高(25.69%)[24]。此外,2023-2024年冬春季,我国多地出现多种呼吸道病原叠加或交替流行的现象,监测数据显示,RSV在病原流行强度和导致的病例报告数据中均居于高位 [25-27]。因此,在我国对婴幼儿尽早实施针对RSV的免疫预防措施十分重要和必要。
二、
国外婴幼儿RSV感染相关疾病免疫预防的进展与经验
1. 国外婴幼儿RSV相关疾病免疫预防的进展:
技术问题2.
为什么RSV被动免疫手段成为婴幼儿RSV免疫预防的重点策略之一?如何认识该被动免疫手段的预防价值?
专家共识2.
根据婴幼儿早期感染RSV的特点和新批准上市的RSV长效单抗的作用机制,可在生命早期为婴幼儿提供较为及时、安全的被动免疫保护,预防RSV相关下呼吸道感染。(A1)
RSV免疫预防手段包括主动免疫和被动免疫。截至2024年1月,全球已获批上市3种预防婴幼儿RSV相关疾病的疫苗或单抗,包括1种母体免疫疫苗(通过母体接种疫苗,再将抗体通过胎盘传递给胎儿)和2种单抗(通用名分别为帕利珠单抗、尼塞韦单抗),另有10余种疫苗/单抗仍处于研发阶段 [28]。长效尼塞韦单抗已于2023年12月正式获得国家药品监督管理局批准,是我国首个获批上市的预防婴幼儿RSV相关下呼吸道疾病的生物制品。国内研发企业也在积极开展婴幼儿RSV疫苗和单抗的自主研发,目前已有一种国产疫苗递交临床试验申请 [29],一种长效单抗进入Ⅲ期临床阶段 [30],有望在未来为我国婴幼儿RSV免疫预防提供更加丰富的产品。
RSV疫苗研发在20世纪60年代就已开始,但因接种福尔马林灭活的全病毒疫苗的儿童在自然感染RSV后诱发了ERD,导致80%的接种疫苗者住院,最终造成2名儿童死亡,这一严重的不良反应事件使得后续RSV疫苗的研发长期进展缓慢 [31-32]。后续研发过程中发现,婴幼儿尤其是小月龄婴儿RSV疫苗研发受多种因素制约,如婴幼儿免疫系统不成熟,小月龄(4~6月龄以下)婴儿接种RSV疫苗后难以产生充足、持久的免疫应答,疫苗安全性等,均导致疫苗研发进展缓慢 [33-35]。经过60多年的坎坷探索,RSV疫苗研发之路终于迎来曙光。2017年,世界卫生组织(WHO)疫苗产品研发咨询委员会确定了两个婴幼儿RSV疫苗的优先研发方向:一是研发用于妊娠中后期母体免疫的疫苗,通过胎盘抗体转移来预防新生儿和婴幼儿的严重RSV相关疾病;二是研发用于儿童免疫的疫苗,预防婴幼儿的RSV相关疾病 [31]。近年来,通过胎盘抗体转移来预防新生儿严重RSV相关疾病的母体免疫疫苗研发取得成功,于2023年在欧美等国家获批上市,暂未引进中国。在儿童疫苗研发方面,我国目前有一款婴幼儿鼻喷RSV减毒活疫苗进入临床Ⅲ期阶段,可为6月龄及以上婴幼儿提供免疫保护 [36],尚无用于6月龄以下婴幼儿的疫苗进入临床Ⅲ期阶段 [37]。
婴幼儿RSV疫苗在国内尚未获批,为降低RSV相关疾病在婴幼儿群体中的沉重疾病负担,除传统的疫苗接种外,WHO积极鼓励推进预防用RSV单抗的研发和使用,以填补儿童特别是婴幼儿群体免疫预防的空白,并于2021年发布了《世界卫生组织推荐用于呼吸道合胞病毒感染被动免疫理想的单克隆抗体的产品特性》 [38],旨在促进开发高质量、安全、有效的RSV单抗,预防全球婴幼儿严重RSV疾病和RSV相关死亡。现代生物技术的发展,特别是在解决了单抗全人源化和长效性问题,为被动免疫理想的RSV单抗研发奠定了基础。全人源化单抗全由人类的抗体基因编码表达,兼具高亲和力、高特异性、低免疫原性等优点,已成为全球各国研发的主流趋势。目前,尼塞韦单抗是全球范围内首个获批的预防用RSV长效单抗,还有两种长效预防用单抗正在开展临床研究,有望在未来几年获批上市。
2023年发表的临床研究结果显示:尼塞韦单抗可有效降低76.8%(95%CI:49.4%~89.4%)的RSV相关下呼吸道感染(lower respiratory tract infection,LRTI)住院率、78.6%(95%CI:48.8%~90.1%)的严重RSV相关LRTI发病率和76.4%(95%CI:62.3%~85.2%)需接受医疗护理的RSV相关LRTI发病率 [39];尼塞韦单抗的安全性良好,各项指标与对照组的生理盐水相似。2024年,西班牙加利西亚大区将尼塞韦单抗纳入儿童免疫规划后开展了安全性和有效性评价,初步结果显示:11 000余名婴幼儿在接种后均无严重不良反应报告,且接种人群的累计住院率较前几个RSV流行季的中位数下降约90% [40]。同年,卢森堡的一项研究报道了产科新生儿接种RSV长效单抗的数据,其免疫覆盖率约为84%(范围66%~94%),RSV长效单抗的使用可显著减少RSV相关人均住院时长(3.2 d比5.1 d,P<0.001),婴幼儿群体总体住院时长由2022年的1 984 d降至2023年的771 d(P<0.001),显著降低了医疗资源占用;从人群保护效果角度,大多数严重RSV相关LRTI发生于未接种RSV长效单抗的人群 [41]。2024年3月,美国CDC发布了尼塞韦单抗在美国上市后的首个真实世界研究结果,该研究共纳入了699名小于8月龄的婴儿,研究结果显示:尼塞韦单抗的使用对RSV感染相关住院的保护效果为90%(婴幼儿出生后的第一个RSV流行季) [42]。美国新疫苗监测网络(the new vaccine surveillance network,NVSN)的监测研究数据显示:尼塞韦单抗预防RSV感染相关住院的保护效果约为91%,在VISION网络(Virtual SARS-CoV-2, Influenza and Other respiratory viruses Network)中报告的保护效果达98%;尼塞韦单抗对预防RSV相关ARI就诊的保护效果为89% [43]。上述研究结果证实了尼塞韦单抗在真实世界研究中的有效性和安全性。
2. 全球部分发达国家婴幼儿RSV相关疾病被动免疫策略与实施:
技术问题3.
为什么一些发达国家纷纷引入RSV长效单抗对婴幼儿开展接种,甚至有的国家已将其纳入到儿童国家免疫规划之中?
专家共识3.
目前儿童出生后无预防RSV相关疾病的疫苗可用,且用于婴幼儿的疫苗近期难有重大突破。对于罹患重症风险最高的小龄婴幼儿尽早提供有效保护是预防RSV相关下呼吸道疾病的首要目的,RSV长效单抗被动免疫具有安全有效的特点,且在新生儿出生之后的首个流行季即可提供接种,而纳入儿童国家免疫规划或结合预防接种体系推动实施可实现更好的可及性和公共卫生价值。(A2)
现有预防婴幼儿RSV相关下呼吸道疾病的免疫手段有两种,一是主动-被动免疫,即孕妇在孕后期接种已上市的RSV疫苗获得免疫力后,再通过胎盘将特异性中和抗体传递给胎儿,以预防新生儿和小月龄婴幼儿RSV相关疾病;二是被动免疫,即对小月龄婴幼儿直接接种特异性RSV长效单抗,特别是即将进入或出生在第一个RSV流行季的新生儿和婴儿在出生后或流行季来临前尽快完成长效单抗的接种。
RSV长效单抗作为一种非疫苗类的预防用生物制品,各国在注册审批和使用管理等方面的政策存在差异,为其制定适合于当地实际情况的使用策略是许多国家亟待解决的公共卫生议题。对此大部分发达国家经历了一系列开放且审慎的探索过程。以美国为例,美国CDC首先总结了将RSV长效单抗纳入免疫策略需考虑和应具备的相关因素和条件,包括能够解决危害公众健康、引起沉重负担的传染病问题;预防接种单位可操作性(从接种方式、储运、接种次数等方面评估能够依照常规预防接种方式实施);国家免疫规划可负担的价格水平。在此基础上,对于无疫苗可用或需要在短时间内迅速为高风险婴幼儿人群提供高水平免疫保护的情况下,RSV长效单抗的价值则更为显著。针对将RSV长效单抗纳入儿童免疫规划的决议,美国免疫实践咨询委员会(Advisory Committee on Immunization Practices,ACIP)在该产品正式获得监管部门上市审批前约一年半成立了专门的RSV儿童免疫工作组,此后围绕RSV长效单抗被动免疫的必要性、安全性、有效性、可操作性及公共卫生价值等多个角度开展了系统性的论证,并最终形成将其纳入儿童免疫规划的循证决策。
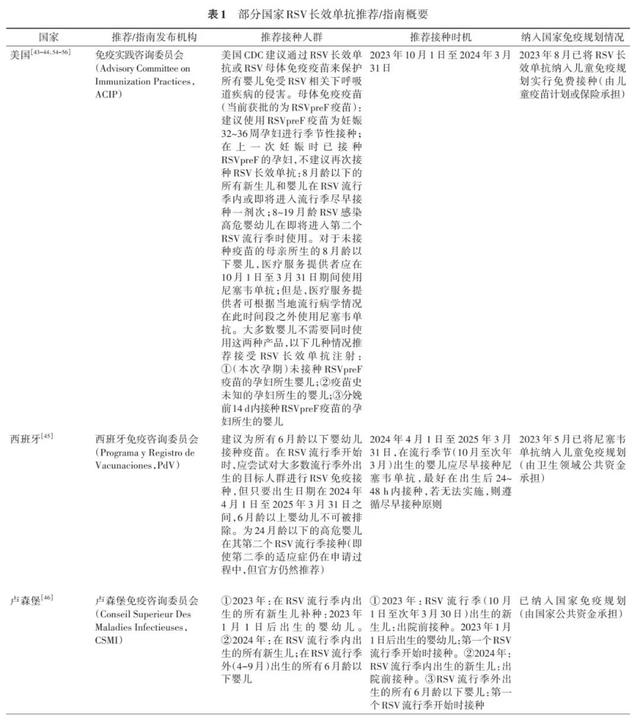
截至2024年3月,包括美国 [44]、西班牙 [45]、卢森堡 [46]、奥地利 [47]、智利 [48]、瑞典 [49]、爱尔兰 [50]、比利时 [51]、荷兰 [52]、瑞士 [53]等10余个国家通过国家免疫咨询专家委员会(National Immunization Technical Advisory Groups,NITAGs)推荐尼塞韦单抗用于婴幼儿群体的RSV被动免疫预防,并为其制定了免疫指导意见,从而保障预防用RSV长效单抗面向健康婴幼儿群体的可及性(表1)。美国和西班牙还率先将其纳入儿童免疫规划实行免费接种。

三、
我国婴幼儿RSV长效单抗被动免疫制剂应用的主要技术要点
技术问题4.
现阶段我国RSV长效单抗被动免疫的接种对象有哪些人群?
专家共识4.
RSV长效单抗的接种对象主要为婴幼儿人群,现有RSV单抗主要针对即将进入或出生在第一个RSV流行季的新生儿和婴儿,以提供预防RSV相关下呼吸道疾病的被动免疫保护。(A1)
RSV在婴幼儿特别是1岁以下婴儿中的疾病负担尤为沉重,且无论是健康婴儿,还是早产、患先天性基础疾病等特殊健康状况婴儿,均面临感染RSV风险,大多数因RSV感染住院的婴儿为足月出生的健康婴儿 [58]。一项纳入全球481项研究的Meta分析数据显示:2019年全球范围1岁以下(0~12月龄)RSV相关ALRTI发病率为94.6/1 000人年(95%CI:70.8/1 000人年~131.6/1 000人年),远高于5岁以下的48.8/1 000人年(95%CI:37.4/1 000人年~65.9/1 000人年)[1]。一项纳入来自5个国家近万名健康足月儿的欧洲前瞻性出生队列研究数据显示:在1岁以下健康足月儿中,26.2%(95%CI:24.0%~28.6%)出现症状,14.1% (95%CI:12.3%~16.0%)因RSV感染就诊,1.8% (95%CI:1.6%~2.1%)因RSV感染住院 [59]。我国一项基于2009-2023年16个省份覆盖全年龄组的监测数据显示,急性呼吸道感染病例中RSV检出率为9.33%,并呈现随年龄增加而减少趋势,6月龄以下组患儿中RSV检出率最高为25.69%,其次为6月龄至1岁以下组为18.31%,说明1岁以下尤其是6月龄以下婴儿是RSV感染的高发人群 [24]。法国一项监测数据显示:5岁以下儿童中,每年有40 000~45 000例患儿因RSV毛细支气管炎住院,其中,69%为1岁以下婴儿 [60]。一项基于2020-2021年我国河南省前瞻性病例系列研究数据显示:5岁以下儿童因RSV住院造成了巨大的经济负担,其中1岁以下婴儿的经济负担尤为沉重 [61]。
目前我国已批准上市了用于预防婴幼儿RSV相关LRTI的特异性RSV长效单抗,应按照产品说明书要求,并结合国际指南推荐及实践经验,尽快开展探索性使用研究,建议即将进入或出生在第一个RSV流行季的新生儿和婴儿在出生后或流行季来临前尽快完成RSV长效单抗的接种。
技术问题5.
为什么RSV长效单抗被动免疫更加重视对受种者接种时机的要求?
专家共识5.
考虑到接种RSV长效单抗后的免疫持久性,在RSV感染流行季前或流行季内接种RSV长效单抗,以确保整个流行季内维持有效的抗体水平。不仅可以保护受种者个体免遭RSV感染疾病的痛苦,甚至在接种覆盖率达到一定水平时,可能发挥更大的预防感染的免疫屏障作用,建议符合条件的婴儿应尽早接种。(A2)
目前,已批准上市的RSV长效单抗应用了YTE位点突变技术,即将IgG抗体Fc结构域中的3种氨基酸(M252Y、S254T和T256E)进行替换,在较低的pH下增加了对新生儿Fc受体(neonatal fc receptor, FcRn)的亲和力,从而使抗体实现再循环。与无YTE的单抗相比,半衰期延长3~4倍,至(71.4±11.4 )d;临床保护时效至少为5个月 [62];保护性的免疫抗体水平可超过6个月 [63-65]。西班牙儿科协会认为该RSV长效单抗的保护时长可能达11个月 [66],基本上可覆盖我国大部分地区RSV流行季的时间范围。
与北半球其他国家和地区RSV流行季情况类似,我国RSV流行季主要为冬季和春季,部分南方省份受地理位置、湿度和温度的影响,可能会在夏季出现小高峰。一项纳入了157项研究、超过20个省份研究数据的Meta分析显示:我国大部分省份RSV流行季发生在当年11月至次年3月,中位流行持续时间约为4.6个月 [67]。2009-2023年中国16个省份急性呼吸道感染病例监测数据显示,我国RSV流行主要以冬、春季为主,北方流行季节通常为10月至次年3月,南方在夏季还会有小高峰 [24]。一项在重庆市进行的纳入6 991例患者并历时10年的回顾性研究显示,重庆地区RSV流行季大致为当年10月至次年3月,并在6月出现小高峰 [68]。深圳市的一项研究对2019年3月至2023年12月9 278份呼吸道样本进行了检测,发现RSV的流行季节以夏季和初秋(9月)为主,其中2022年冬季RSV阳性率显著升高[69]。
综上所述,从全国层面来看,建议按照典型的RSV流行季开展RSV长效单抗接种工作,以确保重点人群及时得到保护,具体要求:①在流行季内出生的婴儿于出生后尽快接种RSV长效单抗;②在流行季外出生的婴儿于流行季前,即10-11月尽快完成RSV长效单抗的接种;③未能按照推荐时间完成抗体免疫的婴儿,建议在RSV流行季内尽快完成补种。
技术问题6.
RSV长效单抗可以像普通疫苗一样在接种门诊开展接种吗?
专家共识6.
各地应结合国际指南推荐及实践经验,积极创新探索,制定适合当地实际情况的试点实施方案,依法依规强化管理,以便为更多的婴幼儿提供便利、可及的RSV被动免疫预防服务。(A2)
如表1所述,一些发达国家已对婴幼儿实行RSV长效单抗被动免疫接种策略,美国、西班牙等国家还将其纳入国家免疫规划实行免费接种。以西班牙为例,2023年在批准将RSV长效单抗纳入儿童免疫规划时,由西班牙免疫咨询委员会发布推荐意见 [45]:在2023/2024年RSV流行季期间,通过医院或初级保健机构实施被动免疫接种计划,并敦促医疗卫生机构在RSV流行季开始时为在RSV流行季外出生的目标人群接种长效单抗(目标人群为2024年4月1日至2025年3月31日出生的所有婴儿,6月龄以上婴儿不能作为排除标准);对于在季节内(10月至次年3月)出生的婴儿应尽早接种(最好在出生后24~48 h内接种),若无法在48 h内接种,则遵循尽早接种原则。同时,指南中强调已接种RSV长效单抗的婴幼儿须在当地疫苗接种信息系统(或登记册)中记录,以保障免疫项目监测与评价工作的开展。2024年最新的研究报道,西班牙最早实施RSV长效单抗纳入儿童免疫规划的加利西亚自治区对该项目开展了监测和效果评估,结果显示接种覆盖率达到91.7%;未发现与长效单抗接种相关的严重不良事件;当地通过该项目实施,RSV相关ALRTI住院率降低了82% [70]。
对于RSV流行季内出生的婴儿,建议在产科出院前,由医生、助产士或护士根据相关指导进行接种;在RSV流行季外出生的婴儿,建议逐步在基层医疗卫生机构由儿童保健医生、全科医生或儿科医生和预防接种医生进行接种。
目前,上海市药品监管、卫生健康、疾病预防控制等多部门共同协作,结合当地工作实际,制订了RSV被动免疫制剂应用试点工作方案并付诸实施,通过创新试点不断推动改进接种工作,同时强化对该类生物制品的全过程监管和管理,逐步探索形成疾病预防控制、药品监管等跨部门互动机制,严格把控使用的安全和规范 [71]。天津市通过多部门验证及专家论证出台针对PSV单克隆抗体接种的专业指导意见,规范了新型预防用生物制品的应用模式及管理。北京市及其他省份有关部门也在组织论证,积极探索制订符合当地实际情况的接种方案。
技术问题7.
RSV长效单抗可否与其他疫苗进行联合接种?
专家共识7.
国外临床试验结果和实践经验显示,RSV长效单抗可与常规儿童疫苗同时接种。我国今后应执行该产品说明书的规定,同时尽快积累我国的临床研究证据。(A2)
RSV长效单抗的作用机制在于高度特异性中和靶向病毒抗原位点,不依赖婴儿自身的免疫系统,理论上不会干扰其他疫苗的免疫应答 [62]。临床试验数据显示,尼塞韦单抗和常规儿童疫苗联合接种方案的安全性和免疫原性与单独接种相似,不会影响其他常规疫苗的免疫接种[62]。美国ACIP和多国国家免疫医学协会均认为,RSV长效单抗可与常规儿童疫苗同时接种 [45, 54]。根据我国有关规定和基层工作人员的习惯,在尚未得到国家有关部门批准时,RSV长效单抗应按照产品说明书规定执行,即与其他国家的多疫苗同时接种指导原则一致,但应使用不同的注射器并在不同部位进行接种 [62]。
技术问题8.
使用RSV长效单抗进行被动免疫接种时,还应注意其他哪些技术问题?
专家共识8.
RSV长效单抗属于预防用生物制品,开展被动免疫接种时应遵循国家的法律、法规等要求,具体储运使用管理和接种操作应执行说明书的规定。(A1)
RSV长效单抗作为生物制品类药品,在储存运输和使用过程中应确保全过程处于2 ℃~8 ℃冷链条件下,并全程做好监测记录,使用单位应做好出冷链管理和相关登记记录工作。接种前要做到充分的告知,询问健康状况和核查接种禁忌,并做到知情同意。在全科、儿科、新生儿科等临床医疗机构进行注射使用,应按照相关法律法规要求并遵医嘱使用;在接种
