对于ARDS患者来说,选择最合适PEEP水平,有利于开放萎陷的肺泡和预防相对正常/已开放的陷闭肺区过度膨胀。

图1 PEEP 与肺泡通气
· 一、PEEP的生理学效应 ·
ARDS根据病情的轻重大体分为相对正常肺区、实变肺区和陷闭肺区。
1)相对正常肺区:可保持完善的气体交换功能,约占TLC的30%,无须机械通气治疗;PEEP的实施只能加重其过度扩张和该区肺循环阻力的增加。
2)实变肺区:约占TLC的40%,常规通气治疗无效,是导致顽固性低氧血症的主要原因,随着病情改善,水肿减轻后机械通气才能逐渐发挥治疗作用。
3)陷闭肺区:介于相对正常肺区(或肺组织)和实变肺区(或肺组织)之间为陷闭肺区(或肺组 织),占TLC的20%~30%,其病理生理特点表现为吸气期扩张,进行通气和气体交换;呼气期完全回缩,不能进行通气和气体交换,称为动态陷闭,这时候存在导致间歇性分流和严重低氧血症、肺血管反射性收缩和局部肺循环阻力增高、切变力显著增大和肺损伤。

图2 陷闭肺区的肺泡-吸气期扩张,呼气期完全回缩
PEEP的应用不同肺区的生理效应并不一致,在陷闭肺区作用
1)扩张陷闭肺泡:可使呼气末肺容积增加,改善肺顺应性,从而降低驱动压力(Pplat-PEEP)。此外,陷闭的肺泡扩张后,也可减少肺内分流,改善氧合。
但在过高的PEEP水平也可能导致不良影响,如在相对正常肺区:
1)高胸内压,阻碍静脉回流,从而减少心输出量。
2)肺动脉毛细血管在压力增大时可能塌陷,导致肺血管阻力增大,从而增加右心室的后负荷。
3)PEEP过高时肺泡压可能高于肺毛细血管压;这可能导致肺毛细血管塌陷,从而减少相对于通气的灌注,导致肺泡死腔增大;
4)高PEEP水平也可能增加气压创伤的风险。

· 二、PEEP的滴定 ·
· 2.1 PEEP-FIO2表格·
使用PEEP-FIO2的组合来维持SpO2(88-95%)或PaO2 (55-80mm Hg)的目标。可复张性低的选用低PEEP-FIO2组合;可复张性高的选择高PEEP-FIO2组合。
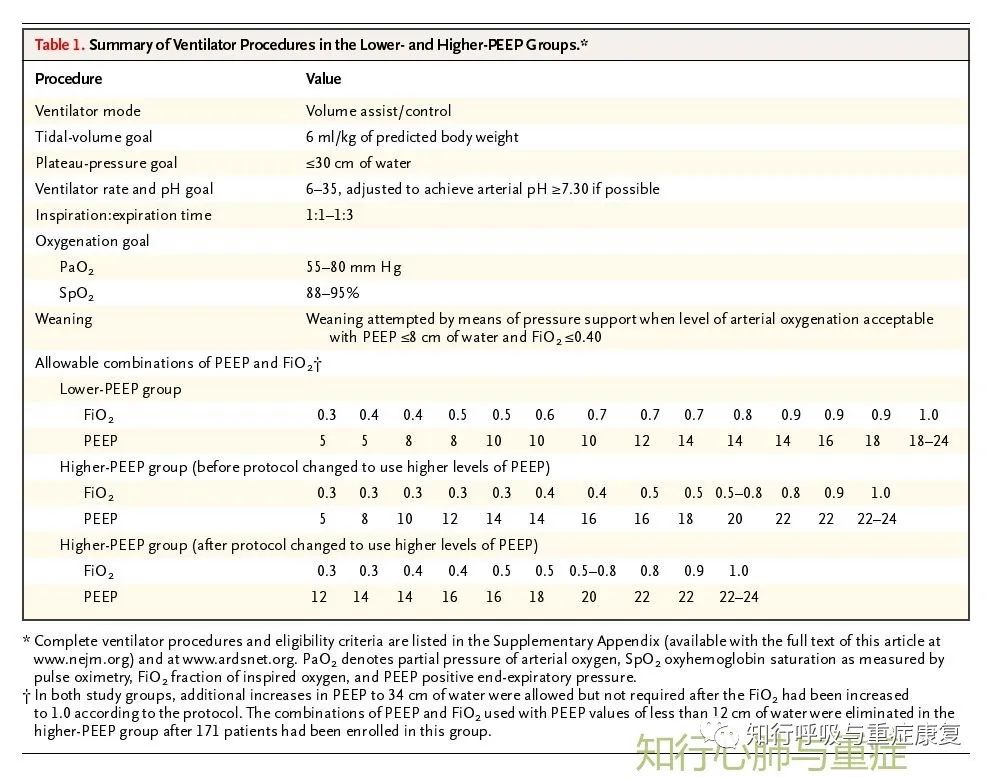
图3 PEEP-FiO2表
· 2.2 氧合情况·
理论上,如果陷闭的肺泡通过PEEP进行复张后,肺内分流的减少应能改善氧合。因此,临床通过设置不同水平的PEEP后根据其氧合情况来判断PEEP是否合适。常用的一种方法是肺复张后设置高水平PEEP(20-25cmH2O),然后以2cmH2O降低PEEP,同时测量氧合情况,如果SPO2下降>2%或PaO2下降>10%或氧合指数下降>5%。则PEEP+2cmH2O为最佳PEEP。
· 2.3 静态顺应性·
基于递增或递减PEEP滴定并选择具有最高顺应性的PEEP水平。在每次调整PEEP值时,监测Pplat和潮气量,通过以下公式计算静态顺性:Cst(ml/cm/H2O)=VT/(Pplat-PEEP),当Cst值达到最大时所对应的PEEP为最佳PEEP。
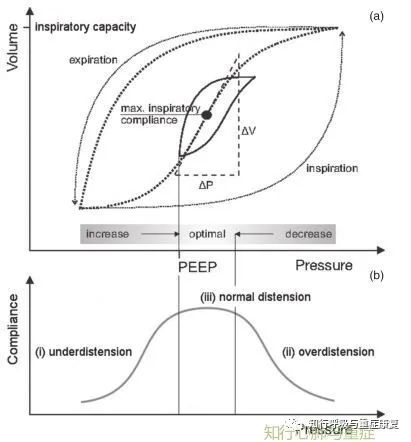
图4顺应性与PEEP
图4-a曲线中,肺容积增长最快的点即被认为肺顺应性最好的点。
·2.4 压力-容积曲线 ·
压力-体积(P-V)曲线显示了肺部充气和放气时体积和压力之间的关系,Amato等利用一种基于P-V曲线和上下拐点滴定PEEP的方法,较低的拐点被认为代表大量肺泡复张的压力,建议将PEEP设置在高于该压力2cmH2O的位置。P-V曲线上的上拐点可能表明肺泡过度膨胀,或者它代表着肺泡复张的结束。
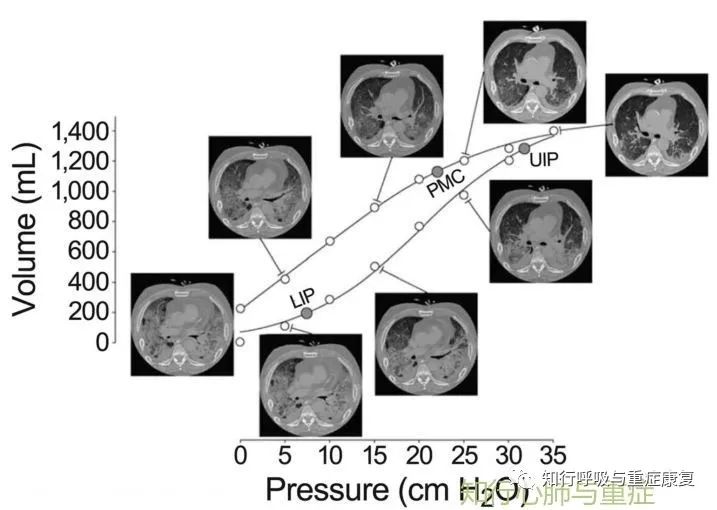
图5 P-V曲线的上拐点与下拐点
低流速P-V环下,下拐点之后,肺容积迅速增大,代表肺泡大量复张,上拐点曲线变平缓,表明肺泡大量复张的情况已结束,再增加PEEP可能会导致过度膨胀。
· 2.5 牵张指数·
牵张指数是容量控制恒定流速下机械通气的压力-时间曲线的形态与肺顺应性的关系。
1)曲线线性增加(牵张指数=1)提示肺泡恢复稳定扩张。2)如果肺泡全部扩张后顺应性降低(曲线向下凹,牵张指数>1)提示过度膨胀,建议降低PEEP或/和VT。3)如果存在大量可复张肺泡时顺应性增加(曲线向上凸,牵张指数<1)提示还有可复张的肺泡,建议增加PEEP。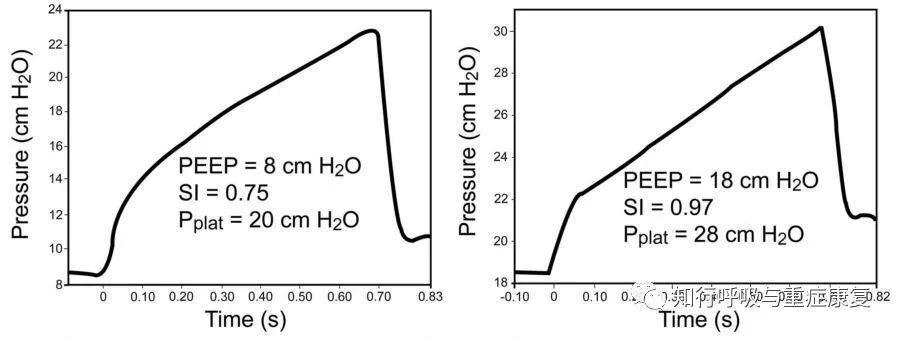
图6 压力-时间曲线
左图PEEP随着时间的推移压力增长的较为平缓,提示肺顺应性增加,还有可复张的肺泡。
· 2.6 食道压·
ARDS患者胸壁顺应性可能降低。这可能导致胸内压增加,如果胸内压力相对肺泡压力高,就有肺泡塌陷的可能。因此,最好将PEEP设定为大于呼气末胸内压。在临床上,胸内压跟食道压成线性关系,因此,可使用食道压测压管估计胸内压,从而更精确地设定PEEP。

图7 食道压滴定PEEP(设置PEEP使呼气末转肺压为零)
· 2.7 肺部超声·
相对正常的肺区、实变肺区与陷闭的肺区在超声下显示为正常A线、异常的B线。通过超声可观察萎陷的肺泡在不同水平PEEP下复张情况,从而更精确的滴定PEEP。

图8 ARDS肺部超声图像
不足的是,对于正常复张还是过度膨胀,超声下均显示为A线,因此超声无法识别肺泡的过度膨胀。
· 2.9 电阻抗成像·
电阻抗成像(EIT)是一种无创、无辐射的监测工具,可对通气进行实时成像。电阻抗断层扫描使用高频和低振幅电流,通常通过胸腔周围的16或32个电极,获得肺的横截面图像。可能用于评估局部肺泡塌陷和过度扩张。
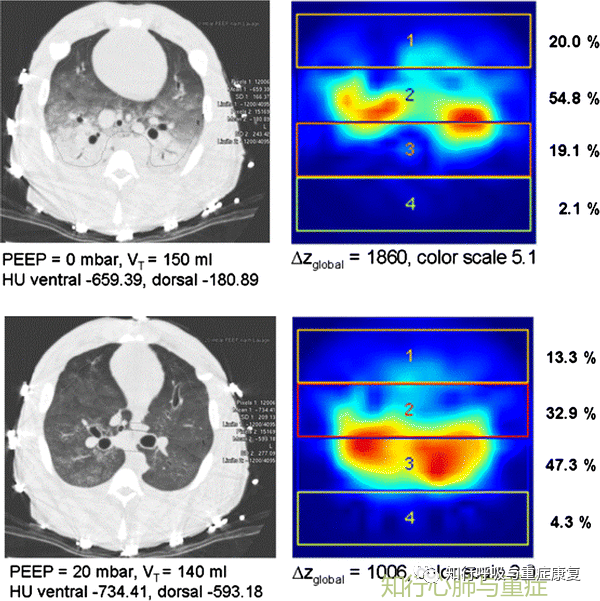
图9 不同PEEP水平下的EIT成像
详细内容在本公众号已详细整理→第139期胸部电阻抗断层成像(EIT)的原理、图像分析及临床应用,在此不再赘述。
· 参考文献 ·
[1]Hess, Dean R. “Recruitment Maneuvers and PEEP Titration.” Respiratory care vol. 60,11 (2015): 1688-704. doi:10.4187/respcare.04409
[2]Sahetya, Sarina K. “Searching for the optimal positive end-expiratory pressure for lung protective ventilation.” Current opinion in critical care vol. 26,1 (2020): 53-58. doi:10.1097/MCC.0000000000000685
[3]Kacmarek, R M, and J Villar. “Management of refractory hypoxemia in ARDS.” Minerva anestesiologica vol. 79,10 (2013): 1173-9.
[4]Brower, Roy G et al. “Higher versus lower positive end-expiratory pressures in patients with the acute respiratory distress syndrome.” The New England journal of medicine vol. 351,4 (2004): 327-36. doi:10.1056/NEJMoa032193
[5]Pettenuzzo T, Boscolo A, De Cassai A, et al. Higher versus lower positive end-expiratory pressure in patients without acute respiratory distress syndrome: a meta-analysis of randomized controlled trials. Crit Care. 2021;25(1):247. Published 2021 Jul 15. doi:10.1186/s13054-021-03669-4
[6]Bello, Gabriela, and Pablo Blanco. “Lung Ultrasonography for Assessing Lung Aeration in Acute Respiratory Distress Syndrome: A Narrative Review.” Journal of ultrasound in medicine : official journal of the American Institute of Ultrasound in Medicine vol. 38,1 (2019): 27-37. doi:10.1002/jum.14671
[7]Pintado, María-Consuelo et al. “Individualized PEEP setting in subjects with ARDS: a randomized controlled pilot study.” Respiratory care vol. 58,9 (2013): 1416-23. doi:10.4187/respcare.02068
[8]Akoumianaki, Evangelia et al. “The application of esophageal pressure measurement in patients with respiratory failure.” American journal of respiratory and critical care medicine vol. 189,5 (2014): 520-31. doi:10.1164/rccm.201312-2193CI
[9]Chiumello, Davide et al. “Bedside selection of positive end-expiratory pressure in mild, moderate, and severe acute respiratory distress syndrome.” Critical care medicine vol. 42,2 (2014): 252-64. doi:10.1097/CCM.0b013e3182a6384f
