转自:医学界
聚焦泌尿系统肿瘤前沿进展。
2024年欧洲肿瘤内科学会(ESMO)年会已在西班牙巴塞罗那圆满落幕,泌尿系统肿瘤领域的研究进展备受瞩目。作为全球常见的泌尿系统肿瘤,肾癌的发病率和死亡率逐年上升,且其独特的生物学特性和治疗复杂性,尤其是对传统放化疗不敏感,使其成为研究探索的热点领域。尿路上皮癌领域,以铂类为基础的化疗是局晚期或转移性尿路上皮癌的一线标准治疗,但疗效有限且难以耐受,亟需探索更多新型疗法。围绕今年ESMO年会肾癌和尿路上皮癌领域最新进展,“医学界”特别邀请北京大学第一医院范宇副教授为国内学者分享治疗的前沿动向。
靶免联合方案新辅助治疗肾癌伴静脉癌栓患者,癌栓降级率达44%
局部进展性肾癌或者晚期肾癌常常伴随静脉癌栓的形成,这类患者由于肿瘤体积巨大或癌栓位置过高,或因手术风险较大等原因不适合首选手术治疗,而需要在手术前进行新辅助治疗使肿瘤、癌栓缩小,从而降低手术风险,延长患者生存时间。鉴于靶免联合治疗在晚期肾癌中的疗效,研究者们开始探索是否能将靶免联合治疗方案应用于肾癌新辅助治疗领域。
一项由中国人民解放军总医院张旭院士、马鑫教授及顾良友教授团队牵头开展的特瑞普利单抗联合阿昔替尼新辅助治疗肾癌伴下腔静脉癌栓的NEOTAX研究(1701P)[1],在ESMO大会的壁报专场上公布了研究成果。这一研究旨在探索特瑞普利单抗联合阿昔替尼新辅助治疗肾透明细胞癌(ccRCC)伴下腔静脉癌栓(IVC-TT)患者的疗效和安全性。研究纳入29例ccRCC伴Ⅱ-Ⅳ级IVC-TT(cT3b/c)、cN0/1、cM0/1、拟行根治性肾切除术联合下腔静脉癌栓取出术的患者,接受特瑞普利单抗(240mgIVQ3w)联合阿昔替尼(5mgPOBID),持续4周期。主要研究终点是IVC-TT降级率,次要研究终点包括手术策略和癌栓高度变化百分比、缓解率、手术并发症发生率、无进展生存期(PFS)、安全性以及生物标志物分析。
数据分析截止日期为2024年2月1日,其中25例接受研究治疗并纳入分析。研究结果表明,入组患者治疗12周后,有44.0%(11/25)的患者癌栓降级(图1左)。24/25(96.0%)的患者癌栓高度有不同程度的减少,癌栓高度变化的中位数为-2.3cm(图1右)。
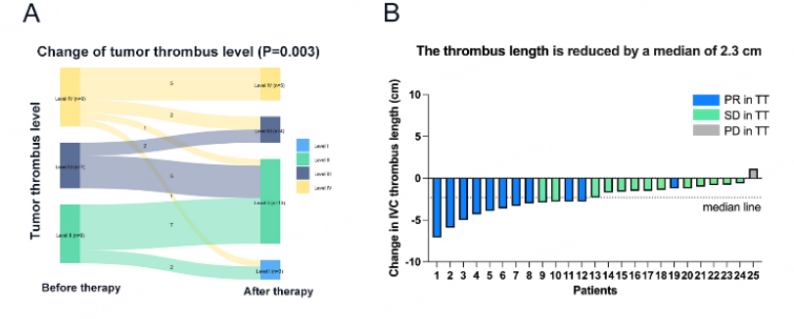
手术决策改变比为61.9%(13/21)。9例(36.0%)患者出现肿瘤进展,其中7例在术后进展(图2左)。1年和2年无进展生存(PFS)率分别为89.1%和54.8%(图2右)。

安全性方面,大多为1级或2级治疗相关不良事件(TRAEs),未出现4-5级的TRAEs。7例(28.0%)患者发生3级TRAEs,主要为高血压(8.0%)和蛋白尿(8.0%)。
Ⅱ期NEOTAX研究结果表明,特瑞普利单抗联合阿昔替尼新辅助治疗肾癌伴静脉癌栓患者的总体癌栓降级率可观,从而缩小手术范围,降低手术难度,为靶免联合方案新辅助治疗用于肾癌伴静脉癌栓领域增添了循证医学证据。
今年,特瑞普利单抗联合阿昔替尼探索了在肾癌领域的新辅助治疗。早在去年,该组合就已探索了在肾癌领域的一线治疗应用。由北京大学肿瘤医院郭军教授牵头的RENOTORCH研究[2]填补了我国晚期肾细胞癌靶向联合免疫治疗领域的空白。研究结果显示,特瑞普利单抗联合阿昔替尼组中位PFS达到18.0个月,舒尼替尼单药组为9.8个月,疗效近乎翻倍,HR=0.65([95%CI:0.49~0.86],P=0.0028)。从PFS数值来看,特瑞普利单抗联合阿昔替尼方案刷新了肾癌免疫靶向双药治疗PFS获益数值纪录。
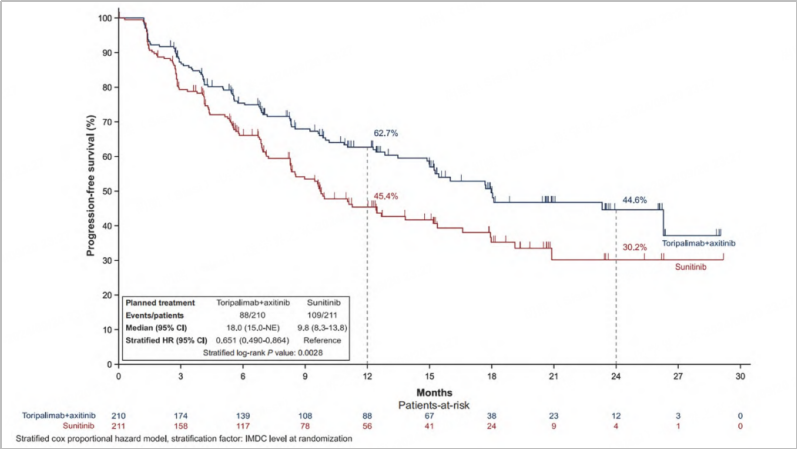
在安全性方面,特瑞普利单抗联合阿昔替尼组和舒尼替尼组发生≥3级治疗相关的不良事件(TEAEs)(71.2%vs67.1%)、导致停止治疗的TEAEs(5.8%vs8.1%)发生率相似。与国外同类型研究的间接比较之下,RENOTORCH研究中特瑞普利单抗联合阿昔替尼的安全性数据毫不逊色。基于RENOTORCH研究结果,阿昔替尼+特瑞普利单抗获得了《CSCO肾癌诊疗指南2024》[3]、2024版《ESMO肾细胞癌指南》[4]的高级别推荐。
此外,2024年ESMO年会还公布了另一个靶向联合方案,即安罗替尼联合PD-L1单抗TQB2450对比舒尼替尼一线治疗晚期肾透明细胞癌的随机对照多中心Ⅲ期临床研究,结果显示安罗替尼联合TQB2450能够显著改善晚期肾透明细胞癌的中位PFS[5]。
盘点尿路上皮癌领域其他研究热点,ADC成绩引人瞩目
除了靶免联合治疗为肾癌领域带来的突破性进展,尿路上皮癌作为常见泌尿系统肿瘤之一,新型抗体偶联药物(ADC)在尿路上皮癌的治疗进展也备受瞩目,在今年ESMO大会上多款ADC药物报告了其在尿路上皮癌中的研究进展。如针对EGFR和HER3靶点的双抗ADCBL-B01D1在尿路上皮癌中的Ⅱ期研究数据(1959O)[6]以口头报告形式公布,结果显示23名接受2.2mg/kg剂量治疗的患者可评估疗效,客观缓解率(ORR)为43.5%,确认客观缓解率(cORR)为34.8%,中位PFS为5.5个月。对于既往接受过一线化疗的患者,ORR为90%,cORR为80%,未达到中位PFS。
针对HER2靶点的维迪西妥单抗(DV)联合特瑞普利单抗用于晚期尿路上皮癌的Ⅰb/Ⅱ期长期生存随访结果(1979P)[7]以壁报形式公布。此外,靶向Nectin-4的ADC药物取得了里程碑式的突破。维恩妥尤单抗是直接作用于Nectin-4的一种同类首创ADC,用于治疗既往接受过PD-1/PD-L1抑制剂和含铂化疗治疗的局部晚期或转移性尿路上皮癌患者适应证已于2024年8月获得国家药品监督管理局批准上市,也是首个在国内获批的Nectin-4靶向ADC,丰富了我国尿路上皮癌患者的治疗选择。
维恩妥尤单抗在中国的上市申请是基于一项在中国开展的单臂、开放标签、多中心的Ⅱ期桥接EV-203研究[8],共招募了40例中国患者,主要终点是独立审查委员会(IRC)确认的ORR。研究结果表明,IRC确认的ORR为37.5%,中位PFS为4.67个月;研究者评估的ORR为42.5%,中位PFS为4.24个月。在安全性方面,大多数TRAEs为1-2级,整体安全性及耐受性良好。维恩妥尤单抗的获批上市为我国尿路上皮癌带来了新的治疗方案和希望。
多年来,以铂类为基础的化疗是尿路上皮癌的标准一线疗法,但由于获益有限、含铂化疗不耐受等原因,临床迫切需要新的突破性一线治疗方案。EV-302研究[9]则探索了维恩妥尤单抗联合帕博利珠单抗用于一线治疗的有效性和安全性,结果显示该联合方案在OS和PFS方面均显著优于化疗,奠定了晚期尿路上皮癌一线治疗的新标准,美国食品药品监督管理局(FDA)已于2023年12月批准EV联合帕博利珠单抗用于一线治疗局部晚期或转移性尿路上皮癌,期待随着更多创新ADC药物的不断涌现,为尿路上皮癌患者带来更好、更精准的治疗方案。
·总结·
靶免联合疗法为晚期肾癌带来了显著突破,延长了患者的生存期并优化了治疗效果,标志着肾癌一线治疗进入多元化时代。未来的探索将聚焦于精准治疗,通过优化生物标志物和新的联合方案提升疗效。与此同时,ADC药物在尿路上皮癌领域展现出强大潜力,精准递送药物提高了复发及难治性患者的疗效,未来的发展方向将包括靶点优化及更广泛的应用。未来,随着更多临床研究的开展和适应症的拓展,继续推动泌尿系统肿瘤的精准治疗向前迈进。
专家简介

范宇副教授
北京大学第一医院临床药物实验机构副主任
泌尿外科副主任医师副教授博导
主要研究方向:前列腺增生与免疫炎症反应;前列腺癌主动监测;泌尿肿瘤的的表观遗传学
参与多项国际多中心、国内多中心的II期、III期泌尿肿瘤新药、新器械临床试验。先后多次在EAU及AUA作大会发言
发表SCI论文30余篇
主持国自然面上1项,院级课题2项,参与国家及省部级课题9项
获国家实用新型专利1项,发明专利1项,国家软件著作权1项
参考文献:
[1]LiangyouGu,etal.NEOTAX:APhaseIItrialofneoadjuvanttoripalimabplusaxitinibforclearcellrenalcellcarcinomawithinferiorvenacavatumorthrombus.ESMO2024.1701P.
[2]YanXQ,YeMJ,ZouQ,etal.Toripalimabplusaxitinibversussunitinibasfirst-linetreatmentforadvancedrenalcellcarcinoma:RENOTORCH,arandomized,open-label,phaseIIIstudy.AnnOncol.2024Feb;35(2):190-199
[3]CSCO肾癌诊疗指南2024
[4]PowlesT,AlbigesL,BexA,etal.Renalcellcarcinoma:ESMOClinicalPracticeGuidelinefordiagnosis,treatmentandfollow-up.AnnOncol.2024Aug;35(8):692-706.
[5]XinanSheng,etal.Anlotinibincombinedwithanti-PD-L1antibodyBenmelstobart(TQB2450)versussunitinibinfirst-linetreatmentofadvancedrenalcellcarcinoma(RCC)-Arandomized,open-label,phaseIIIstudy(ETER100).ESMO2024.LBA76
[6]DingweiYe,etal.BL-B01D1,anEGFRxHER3bispecificantibody-drugconjugate(ADC),inpatientswithlocallyadvancedormetastaticurothelialcarcinoma(UC).ESMO2024.1959O.
[7]LiZhou,etal.Disitamabvedotin(DV)plustoripalimab(T)inunresectablelocallyadvancedormetastaticurothelialcarcinoma(la/mUC):Long-termoutcomesfromaphaseIb/IIstudy.ESMO2024.1979P.
[8]SimingL,etal.EV-203:Phase2trialofenfortumabvedotininpatientswithpreviouslytreatedadvancedurothelialcarcinomainChina.JClinOncol.2023;41(16):e1657.
[9]PowlesTB,etal.EV-302/KEYNOTE-A39:Open-label,randomizedphase3studyofenfortumabvedotinincombinationwithpembrolizumab(EV+P)vschemotherapy(chemo)inpreviouslyuntreatedlocallyadvancedmetastaticurothelialcarcinoma(la/mUC).ESMO2023.LBA6.
(转自:医学界)
