近日,国内首款渐冻症精准治疗药物获批上市的消息,引发社会关注。齐鲁晚报·齐鲁壹点记者专访研发方跨国药企渤健生物,对方表示,托夫生注射液的获批上市标志着我国正式迈入渐冻症对因治疗的新时代。
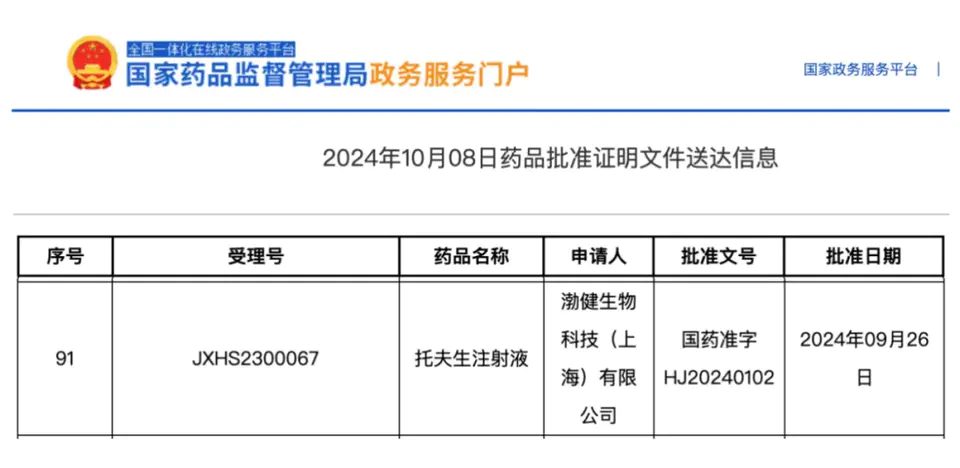
10月8日,国家药品监督管理局官网显示,渤健生物科技(上海)有限公司的托夫生注射液在我国获批上市,该药用于治疗SOD1基因突变的成人肌萎缩侧索硬化症(即ALS,俗称“渐冻症”),也是目前唯一一款针对该类人群的对因治疗药物。
渐冻症,是一种罕见、进行性、致命的神经退行性疾病,具体累及上/下运动神经元及其支配的躯干、四肢和头面部肌肉,表现为进行性加重的肌无力、肌萎缩和肌束颤动等。有数据显示,目前国内有超过4万例渐冻症患者,其中携带SOD1基因突变的患者超1200例。
渤健生物表示,SOD1-ALS是一种具有致死性,且超罕见的ALS。目前,已知由SOD1基因突变引起的ALS约占所有ALS的2%,患者迫切需要针对明确靶点的精准治疗药物。托夫生注射液是中国首个获批的用于治疗SOD1-ALS成年患者的疾病修正药物,极大地填补了未满足需求,标志着我国正式迈入ALS对因治疗的新时代。
渐冻症药物研发难度大。渐冻症患者、京东集团原副总裁蔡磊曾表示,过去几十年,中国没有一家大型药企从事渐冻症的药物研发,因为做这件事无异于拿钱“打水漂”。他参与推进的用于治疗渐冻症的药物已达到100款,其中推进到试验最终结果的有30至40款,全部失败,其余的几十款正在向前推进。
Insight数据库显示,在托夫生注射液获批前,国内获批用于治疗渐冻症的药物只有利鲁唑和依达拉奉,治疗效果均有限。
这款药的作用机制有何不同?渤健生物表示,托夫生注射液是一种反义寡核苷酸药物(ASO),可通过减少SOD1蛋白合成,减少毒性SOD1蛋白的蓄积,从而减轻运动神经元的损伤,减缓疾病进展。
据悉,托夫生注射液于2023年4月在美国获批上市。有报道称,托夫生注射液在未完成三期临床试验的情况下,就被美国食品药品监督管理局(FDA)以“药物被证明对替代终点有影响,该终点很可能预测患者临床获益”为理由加速审批。
目前,该药物在国内未查到注册的临床试验,药物疗效因此受到关注。
渤健生物表示,此次获批是基于据一项在携带SOD1突变的ALS成人受试者中评估托夫生注射液给药的随机、双盲、安慰剂对照的III期临床研究VALOR。研究结果显示,托夫生注射液具有延缓疾病进展的趋势。
记者查询发现,今年3月21日,托夫生注射液在位于海南乐城先行区的瑞金海南医院实现首针注射。此后,又有数位患者在海南接受了首批用药。
什么时候患者能够真正用上这款药?渤健生物称,正积极与各方沟通,全力推进托夫生的商业上市,确保中国患者尽早使用到该创新产品。
有资料显示,目前,托夫生注射液还在开展相应的研究。渤健生物预计将招募约150名具有SOD1基因突变但没有渐冻症的参与者,以评估该药物是否可以延迟渐冻症的出现。这项研究预计于2027年完成。
该药的国内定价,是很多人关心的问题。对此,渤健生物表示,托夫生注射液在中国的售价将在商业上市期公布。
资料显示,托夫生注射液在海外的售价为14230美元,患者第一年需注射14剂,治疗费用总计为199200美元(约为140万元人民币)。
下一步将如何提高药物可及性?渤健生物称,将与各方继续保持积极沟通,共同探讨及推进多方共付机制及罕见病创新生态系统的打造,以不断提升包括托夫生注射液在内的罕见病创新产品在我国的可及性。
(大众新闻·齐鲁壹点记者李静)
