转自:生物谷
近日,四川大学华西医院肿瘤中心陈念永教授、郭刚研究员团队在材料与化学领域的顶级期刊《AdvancedFunctionalMaterials》上发表题为“Bacteria-MediatedBismuth-BasedNanoparticlesActivateToll-LikeReceptorsforBreastCancerPhotothermalImmunotherapy”的论文。团队研究开发了一种具有肿瘤靶向特性的细菌纳米马达Bif@PBi-R。
负载R848的铋基纳米粒子(Bi-RNPs)通过多巴胺粘附与厌氧双歧杆菌结合。Bif@PBi-R旨在将携带R848的铋基纳米粒子(Bi-RNPs)特异性地输送到肿瘤区域,以激活抗肿瘤免疫疗法。

免疫治疗是一种利用机体免疫系统消除肿瘤的治疗策略,目前已成为癌症研究的重点,包括免疫检查点阻断疗法、过继细胞免疫治疗和免疫佐剂疗法在内的多种肿瘤免疫治疗策略正在快速发展。Toll样受体(TLR)激动剂作为免疫佐剂疗法的一种,Toll样受体(TLR7/8)的小分子激动剂是抗原提呈细胞(APCs)的有效激活剂,可促进肿瘤细胞吞噬作用和细胞毒性T淋巴细胞(CTLs)的浸润。
因此,TLR7/8激动剂可以诱导先天性和适应性免疫反应,使其成为肿瘤免疫治疗的多功能免疫刺激佐剂。瑞喹莫德(R848)是一种属于TLR7/8激动剂家族的小分子免疫调节剂。然而,这些疏水性小分子TLR7/8激动剂在局部给药后表现出较差的药代动力学特征,导致部位特异性活性丧失。因此,迫切需要有效的药物递送系。
本研究将R848负载到多孔Bi纳米颗粒中,以增强疏水性和延长循环时间。铋(Bi)是一种无毒且丰富的金属材料,在近红外区域具有很强的吸收能力和高的光热转换效率。因此,将光热疗法(PTT)整合到方法中,消除癌细胞并释放肿瘤相关抗原(TAAs)。这些TAAs被呈递给细胞毒性T淋巴细胞(CTLs),激活抗癌免疫治疗。
由于大多数纳米颗粒主要依赖于增强渗透性和滞留效应(EPR)来穿透肿瘤组织,缺乏主动靶向能力,而厌氧细菌的缺氧趋向性具有可以选择性地积累在缺氧的肿瘤微环境的特性,促进纳米药物在肿瘤部位的积累,两者协同作用可以实现消除恶性肿瘤的有效治疗效果。
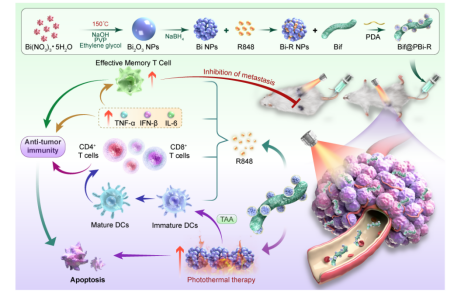
如图2所示,本研究利用婴儿双歧杆菌作为递送载体,通过将Toll样受体7/8(R848)的小分子激动剂和光热剂(铋纳米颗粒,BiNPs)结合,构建了一种细菌纳米马达,命名为Bif@PBi-R。通过多巴胺的粘附,负载R848的BiNPs(Bi-RNPs)被结合到细菌表面。聚多巴胺(PDA)具有优异的生物相容性、高pH敏感性和良好的生理稳定性。Bif@PBi-R保持了细菌的肿瘤靶向特性,并表现出良好的光热特性。
Bif@PBi-R靶向肿瘤的缺氧区域,将铋纳米颗粒(BiNPs)递送到肿瘤部位。在近红外(NIR)照射下,BiNPs增强了PTT的效率,并释放肿瘤相关抗原(TAA),激活免疫反应。此外,释放的R848促进TLRs的激活,导致APC共刺激分子表达增加和促炎细胞因子的分泌,从而增强全身免疫反应。这些作用协同增强抗肿瘤免疫反应。此外,Bif@PBi-R诱导长期免疫记忆,从而预防肿瘤复发和转移。这种生物活性药物递送系统为抗肿瘤免疫治疗和靶向治疗提供了一个新的治疗平台。
我院郭刚研究员、陈念永教授及石河子大学韩博教授为共同通讯作者,2023级博士肖苏苏、2024级博士冯晨倩及2023级博士后母敏为共同第一作者。
