转自:上观新闻
近日,国家传染病医学中心主任、复旦大学附属华山医院感染科主任张文宏教授与复旦大学附属华山医院感染科王森副主任医师作为通讯作者,艾静文副研究员为第一作者与共同通讯作者,郭晶鑫、林可、蔡建鹏、张昊澄及朱峰作为共同第一作者,在《国家科学评论》(NationalScienceReview,NSR,中科院一区,影响因子16.3分)发表题为“Integratedmulti-omicscharacterizationacrossclinicallyrelevantsubgroupsoflongCOVID”(《基于多组学联合分析的长新冠临床亚分型特征》)的论文。
该研究通过大规模的蛋白转录组及代谢组学的联合分析,确定了长新冠不同临床亚型的多组学免疫代谢特征,找到了诊断生物标志物和潜在治疗靶点。研究创新性描绘了长新冠不同临床亚型之间的同质性及异质性的免疫代谢特点,为长新冠的临床诊治新思路提供了坚实的基础。

研究背景
新冠病毒目前仍呈常态化流行,长新冠等症状可长期影响部分患者生活质量,带来较大公共卫生与社会经济负担。
新型冠状病毒感染目前已呈常态化流行,尽管病毒感染症状通常只持续2-3周,但自2020年来,多个报道提示10%左右患者在急性期之后会经历持续数月的呼吸困难、疲劳和脑雾等症状[1,2],世界卫生组织定义其为新冠感染后综合征,即长新冠。据报导,全球罹患长新冠的患者数量仍持续增加。长新冠症状可累及多个器官或系统,造成患者心理和精神障碍对于部分患者更可严重影响患者日常生活,并导致其劳动力的丧失,造成了巨大的公共卫生压力与社会经济负担。
本研究团队自2022年启动了完整的长新冠多中心前瞻性队列研究。通过对21826名首次感染新冠的患者的流行病学及临床特征分析,发现8.89%的患者在感染后6个月报告了长新冠症状,且其中约20-30%左右患者的症状可在一年的时候持续存在[3]。因此,揭示这些长新冠症状的发生和持续背后的免疫机制具有较大研究价值[3](EmergMicrobesInfect,2023)。
免疫系统炎症活化可参与长新冠免疫损伤作用,但机制不明
目前国际上普遍认为机体炎症活化及免疫失调是长新冠的主要免疫致病机制之一。其中,天然免疫及体液免疫通路的异常活跃在不同研究中各有报道[4-8]。但和临床表型存在显著异质性一样,长新冠患者的免疫亚型也存在明显异质性[9-13],这为研究者深入理解疾病的致病机制造成了一定阻碍。按照患者主要呈现的临床症状区分,长新冠可分为神经长新冠、肺部长新冠、心血管系统长新冠以及系统性长新冠等。解析长新冠不同临床亚型的同质性和异质性免疫致病机制将有助于探索不同长新冠患者的特异性治疗方案,并最终协助探索长新冠患者的精确管理。
研究内容
在此之前,团队已经发现长新冠患者中间存在天然免疫通路的活化,且这些患者的临床炎症检测相关指标与长新冠临床和心理症状呈正相关(JTranslMed,2024)。同时本研究团队对免疫治疗及抗病毒治疗对长新冠发病的影响进行了初步探讨(ClinMicrobiolInfect,2024)。
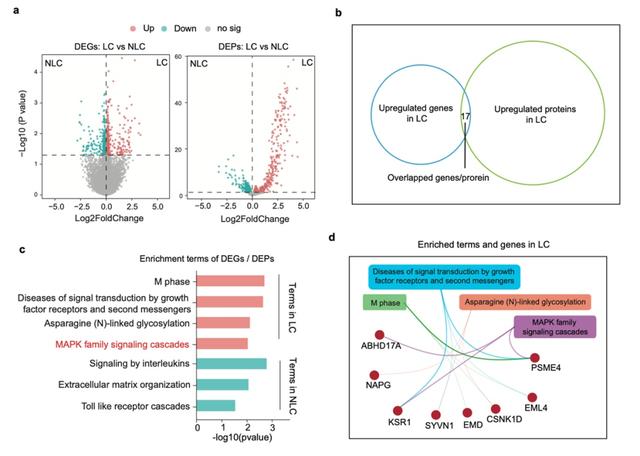
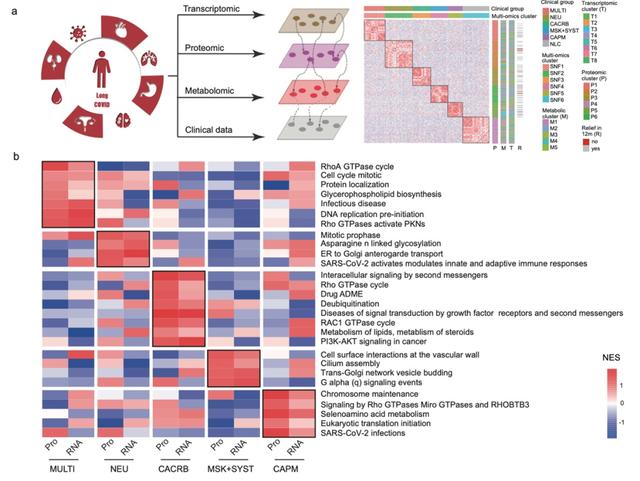
在本研究中,研究团队通过包括转录组学、蛋白质组学和代谢组学在内的多组学整合分析发现,长新冠患者整体呈现MAPK通路激活增高,而康复的长新冠患者则表现出该反应的下调(图1)。长新冠的异质性特征在不同亚组中表现为多组学特异性标志:多系统(MULTI)症状亚组表现为甘油磷脂和醚类脂质代谢增强,神经(NEU)亚组表现为糖蛋白合成代谢增加,心脑(CACRB)亚组表现为丙酮酸代谢增加和巨噬细胞极化受抑,肌肉骨骼+系统性(MSK+SYST)亚组表现为甘油磷脂代谢增高,而心肺(CAPM)亚组则表现为NF-κB信号通路受抑。ABHD17A、CSNK1D、PSME4和SYVN1可被选为诊断长新冠的潜在生物标志物,而CRH(MULTI)、FPGT(NEU)、CBX6(CACRB)和RBBP4(CAPM)则是各个相应亚组的血清特异性蛋白(图2)。该研究提供了长新冠同质及亚组之间异质性的的病理生理解释,为未来的诊断和治疗干预奠定了基础。
讨论和解读
本研究报道了长新冠患者总体及不同临床亚型的大规模蛋白基因组学特征,涵盖转录组学、蛋白质组学、代谢组学和磷酸化蛋白质组学分析。这些数据为进一步揭示临床表现同质性和异质性背后的免疫特征提供了宝贵的资源,并促进针对特定亚组的免疫治疗潜力探索。
从全球来看,长新冠症状在人群中表现出显著的临床和免疫异质性。本研究中,所有长新冠患者无论亚组类别均表现出MAPK激活水平升高,而MAPK激活较强的患者症状持续时间更长,最长可达12个月。本研究提供的信息再次提示长新冠的诊疗需要个体化的探索,临床需要通过分子生物学等手段,找到亟需干预的患者,而不是针对所有自诉临床症状的患者进行干预。
尽管全球科学界已初步达成共识,认为免疫失调是长新冠症状的主要潜在原因之一,但较少有研究关注长新冠不同亚组之间共同的免疫特征。本研究进一步通过结合转录组学、蛋白质组学和磷酸化蛋白质组学数据的多组学分类,识别了长新冠的5个独特免疫代谢亚组,与临床亚型相一致。本研究还发现,肌肉骨骼+系统性(MSK+SYST)亚组和神经(NEU)亚组的一年缓解率低于其他亚组,提示这些症状的患者可能需要更长的恢复期。这一发现与此前研究发现的生物过程恢复模式不同一致[13]。目前,阻碍进一步机制研究的一个障碍是缺乏长新冠动物模型。近期一项研究成功建立了肺部病毒感染后遗症的小鼠模型,这可能极大地推动未来对潜在治疗方法的探索[14,15]。
本研究基于大规模多组学队列,从临床以及综合转录组、蛋白质组和代谢特征方面全面描绘了长新冠的同质性和异质性,揭示了尚未完全通过临床表现分析捕捉到的长新冠各亚组的共有和独特分子与免疫机制,可能为开发个性化治疗策略开辟新路径,最终为临床实践带来益处。我们希望本文中描述的观察结果和分析结论,通过揭示患者间共享和个性化的免疫特征,为长新冠的发病机制、进展和治疗的深入研究提供丰富资源。
参考文献
[1]DavisHE,McCorkellL,VogelJM,TopolEJ.LongCOVID:majorfindings,mechanismsandrecommendations[J].NatRevMicrobiol.2023;21(3):133-46.
[2]SubbaramanN.UShealthagencywillinvest$1billiontoinvestigate‘longCOVID'[J].Nature.2021;591(7850):356.
[3]CaiJ,LinK,ZhangH,XueQ,ZhuK,YuanG,etal.Aone-yearfollow-upstudyofsystematicimpactoflongCOVIDsymptomsamongpatientspostSARS-CoV-2omicronvariantsinfectioninShanghai,China[J].EmergMicrobesInfect.2023;12(2):2220578.
[4]PhetsouphanhC,DarleyDR,WilsonDB,HoweA,MunierCML,PatelSK,etal.Immunologicaldysfunctionpersistsfor8monthsfollowinginitialmild-to-moderateSARS-CoV-2infection.NatImmunol.2022;23(2):210-6.
[5]SantaCruzA,Mendes-FriasA,Azarias-da-SilvaM,AndréS,OliveiraAI,PiresO,etal.Post-acutesequelaeofCOVID-19ischaracterizedbydiminishedperipheralCD8+β7integrin+Tcellsandanti-SARS-CoV-2IgAresponse.NatCommun.2023;14(1):1772.
[6].WoodruffMC,BonhamKS,AnamFA,WalkerTA,FalitiCE,IshiiY,etal.Chronicinflammation,neutrophilactivity,andautoreactivitysplitslongCOVID.NatCommun.2023;14(1):4201
[7].SchultheißC,WillscherE,PascholdL,GottschickC,KleeB,HenkesS-S,etal.TheIL-1β,IL-6,andTNFcytokinetriadisassociatedwithpost-acutesequelaeofCOVID-19.CellRepMed.2022;3(6):100663.
[8].SchultheißC,WillscherE,PascholdL,GottschickC,KleeB,BosurgiL,etal.Liquidbiomarkersofmacrophagedysregulationandcirculatingspikeproteinillustratethebiologicalheterogeneityinpatientswithpost-acutesequelaeofCOVID-19.JMedVirol.2023;95(1):e28364.
[9].TallaA,VasaikarSV,SzetoGL,LemosMP,CzartoskiJL,MacMillanH,etal.PersistentserumproteinsignaturesdefineaninflammatorysubcategoryoflongCOVID.NatCommun.2023;14(1):3417.
[10].LiewF,EfstathiouC,FontanellaS,RichardsonM,SaundersR,SwiebodaD,etal.Large-scalephenotypingofpatientswithlongCOVIDpost-hospitalizationrevealsmechanisticsubtypesofdisease.NatImmunol.2024;25(4):607-21.
[11].PelusoMJ,DeeksSG.MechanismsoflongCOVIDandthepathtowardtherapeutics.Cell.2024;187(20):5500-29.
[12].LiY,QinS,DongL,QiaoS,WangX,YuD,etal.Long-termeffectsofOmicronBA.2breakthroughinfectiononimmunity-metabolismbalance:a6-monthprospectivestudy.NatCommun.2024;15(1):2444.
[13].GuX,WangS,ZhangW,LiC,GuoL,WangZ,etal.ProbinglongCOVIDthroughaproteomiclens:acomprehensivetwo-yearlongitudinalcohortstudyofhospitalisedsurvivors.EBioMedicine.2023;98:104851.
[14].Li,C.A.-O.,Qian,W.A.-O.,Wei,X.A.-O.etal.Comparativesingle-cellanalysisrevealsIFN-γasadriverofrespiratorysequelaeafteracuteCOVID-19.
[15].Narasimhan,H.A.-O.,Cheon,I.S.,Qian,W.etal.Anaberrantimmune-epithelialprogenitornichedrivesvirallungsequelae.LID-10.1038/s41586-024-07926-8.
