转自:生物谷
在科技日新月异的当下,热点话题层出不穷。从人工智能的飞速发展,如ChatGPT引发的全球热议,人们惊叹于其强大的语言处理能力,仿佛看到了智能未来的曙光;到电动汽车领域,特斯拉的不断创新以及国内新能源车企的崛起,改变着人们的出行方式;再到基因编辑技术的突破,为攻克疑难杂症带来了希望。
然而,在这些热点背后,人类对于自身大脑的探索,始终是最为神秘且关键的领域。大脑,这一人体最为复杂的器官,蕴含着约860亿个神经元,其神经元之间的连接更是多达数万亿。正是这些神经元及其连接,构建了我们的思维、情感、记忆与意识。理解大脑的发育过程以及其中神经与血管的相互作用,一直是科学界的重大挑战。
而近期,约翰・霍普金斯大学研究团队的一项成果,犹如一颗重磅炸弹,在相关领域激起千层浪。他们首次构建出具有早期血管化特征的多区域脑类器官(MRBOs),这一突破使得我们能够动态解析多脑区协同发育与神经-血管互作,为大脑研究开辟了全新路径!

脑发育堪称一个高度协调的多区域、多谱系过程。在这个过程中,神经元与血管细胞之间的互作,对谱系维持、分化进程与功能形成有着至关重要的作用。打个比方,神经元如同一个个精密的信息处理单元,而血管细胞则像是为这些单元输送“能量粮草”的后勤部队,二者相互配合,才使得大脑这个“超级司令部”得以正常运转。
现有脑类器官虽已取得显著进展,能在体外模拟原代脑组织的三维结构、分子特性及发育过程,但大多聚焦于单一脑区,或者采用简化的血管模拟,难以展现多脑区协同发育与神经-血管微环境的复杂性。这就好比我们试图用一幅简单的草图去描绘一座宏伟复杂的城市,必然无法呈现其全貌。
约翰・霍普金斯大学的此次研究,目的明确,就是要突破这一困境,构建出更接近真实大脑发育情况的模型!
研究人员从诱导多能干细胞(iPSC)出发,首先利用双SMAD抑制进行神经诱导。对于内皮类器官,则通过WNT激活和BMP4刺激诱导为中胚层谱系,随后借助VEGFA和FGF补充实现血管命运分化。而中/后脑类器官(MHOs)的发育,则通过特定形态发生素组合(CHIR、BMP4、IWR1和SANT1)进行模式化。

图:通过整合单核分析技术,实现多谱系脑类器官发育的生成与分子特征分析
为了验证模型的整合效果,研究人员使用光片显微镜进行观察,确认了多区域脑类器官(MRBOs)的成功构建。进一步通过单核RNA测序分析,结果显示MRBOs中存在多个神经细胞群体和内皮细胞类型,证实了神经与血管组分的整合。特别值得注意的是,与人类胎儿大脑的细胞群簇对比显示,二者有80%的重叠,表明MRBOs在基因表达和生物学特性上具有高度相似性,可作为有效的体外研究平台。此外,不同实验系之间,细胞类型标记物的平均整体可重复性达到68.47%,证明了该模型在模拟神经发育过程方面具有良好的稳健性。
为了深入表征细胞异质性并评估不同脑区的整合情况,研究人员对多种类器官模型进行了系统的单核RNA测序分析。这些模型包括单独培养的大脑皮层类器官、内皮类器官、中/后脑类器官(MHO)、部分融合组装体(如大脑皮层+内皮、中/后脑+内皮、大脑皮层+中/后脑)以及完整的MRBOs。
分析共识别出九个不同的细胞簇。差异表达分析进一步突出了关键基因的表达,例如VEGFA(血管化标记物)、CUX1(皮层神经元标记物)和HOXB3(后脑标记物),表明区域性细胞的特异性身份在融合后得以保留。同时,不同组装体展现出独特的簇结构:例如,内皮-MHO融合体(Endo-MHO)包含七个簇(表达VEGFA、TCF4、HOXB3等标记),而内皮-皮层类器官和单独的MHO则各有六个簇。重要的是,所有簇之间显示出清晰的分离和最小的重叠,这有力地验证了MRBOs共培养方案在维持细胞类型特异性方面的准确性和特异性。
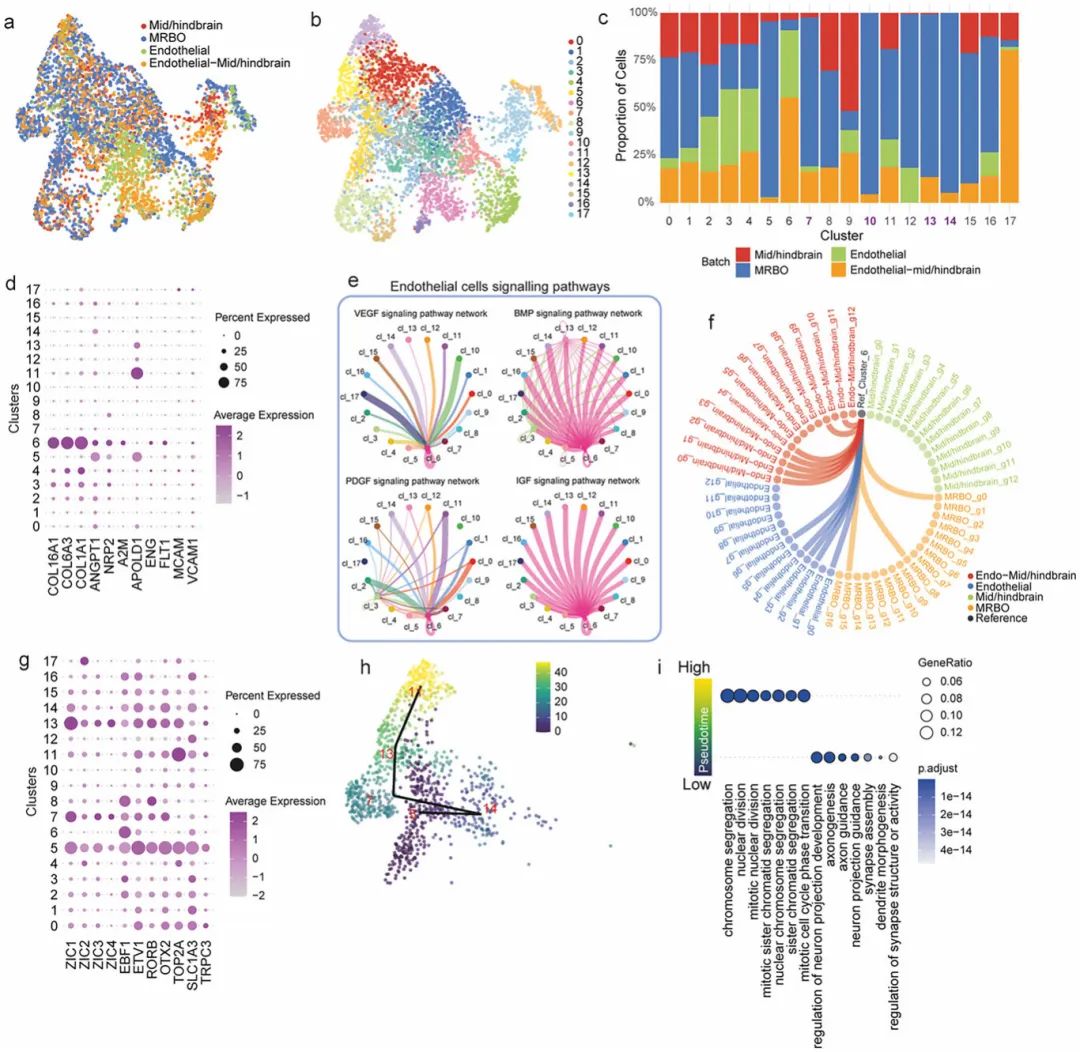
图:内皮细胞异质性及信号传导通路分析
在功能层面,研究人员观察了MRBOs在35至65天发育期间的神经电活动变化。结果显示,尖峰频率和爆发率显著上升,同时尖峰间隔(ISI)缩短,表明神经网络活动变得更加高频和同步。这些数据综合表明,MRBOs不仅实现了不同脑区的空间共存,更形成了功能上整合的神经网络,从而为研究发育性神经疾病提供了一个更具生物学相关性的模型系统。
研究还重点关注了血脑屏障(BBB)在MRBOs中的发育。通过整合MRBOs、内皮类器官、中/后脑类器官及其组合的转录组数据,研究人员识别出一个特异性内皮细胞簇(簇6),该簇高表达多种内皮标记,且仅在包含内皮组分的样本中出现。多模态证据共同确认,MRBOs中存在血脑屏障早期发育的分子与细胞标志。这一发现表明,该模型体系能够模拟血脑屏障的形成过程,为研究与血脑屏障功能障碍相关的疾病提供了新的体外研究视角和工具。
总结而言,约翰・霍普金斯大学开发的多区域脑类器官(MRBOs)模型,凭借其高度的区域特异性和细胞多样性,显著提升了体外模拟人类大脑复杂性的能力。该模型为深入研究大脑发育机制以及神经发育障碍(如自闭症、精神分裂症)的病理基础提供了强大平台,有望推动更精准诊断和治疗策略的开发。此外,对大脑发育机制的深入理解也可能为人工智能领域的设计提供启发。虽然这一成果代表了大脑研究领域的重要进展,但完全揭示大脑的奥秘仍需持续不断的探索。
参考文献:
KshirsagarA,MnatsakanyanH,KulkarniS,GuoJ,ChengK,OfriaLD,BohraO,SagarR,MahairakiV,BadrCE,KathuriaA.Multi-RegionBrainOrganoidsIntegratingCerebral,Mid-Hindbrain,andEndothelialSystems.AdvSci(Weinh).2025Jul8:e03768.doi:10.1002/advs.202503768.Epubaheadofprint.PMID:40625223.