
成果介绍
在阴离子交换膜燃料电池(AEMFCs)中,氢氧化反应(HOR)起着关键作用。在碱性条件下,HOR通过Tafel-Volmer或Heyrovsky-Volmer途径发生。值得注意的是,与酸性介质相比,在碱性介质中HOR动力学相当缓慢。例如,当电解液从酸转变为碱时,贵金属(如Pt、Pd和Ir)上的HOR活性下降约100倍。
加州大学尔湾分校忻获麟教授、广西大学刘熙俊教授等人首先通过建立用于HOR的单原子和双原子位点的催化活性与*H和*OH结合能的关系,以筛选最佳活性位点。结果表明,Ru-Ni双原子中心是最佳活性中心。在理论发现的指导下,随后合成了一种以掺杂N的多孔碳为载体的Ru-Ni双原子位点催化剂,该催化剂对碱性HOR表现出良好的催化活性、CO耐受性和稳定性,也优于对应的单位点催化剂。
原位扫描电化学显微镜研究证实了Ru-Ni双原子位点的HOR活性。此外,原位X射线吸收光谱和计算研究揭示了Ru和Ni之间的协同作用,促进了分子H2的解离,加强OH在双原子位点的吸附,从而增强了HOR动力学。相关工作以《Design of Ru-Ni diatomic sites for efficient alkaline hydrogen oxidation》为题在《Science Advances》上发表论文。
值得注意的是,几天前,忻获麟教授及其合作者也在《Nature Materials》上发表题为《A single-atom library for guided monometallic and concentration-complex multimetallic designs》的研究论文。在该文中,他们采用溶解-碳化法合成了基于37种单金属元素的单原子催化剂,并对其进行了表征和分析,建立了目前报道的最大的单原子催化剂库。
详情可见:忻获麟/罗俊/郑金成Nature Materials:从37种单金属SACs,到元素多达12种的多金属SACs!
图文介绍

图1 利用DASCs调节HOR反应中间体的能量学
通过DFT计算揭示催化剂的*H结合能(HBE,ΔG*H)与*OH结合能(OHBE,ΔG*OH)。在纯SACs上,结果显示ΔG*H和ΔG*OH在Ir、Rh和Ru SACs上较强,而在Ni、Pd和Pt SACs上较弱。考虑将这两种不同行为的金属进行结合,以构建DASCs,以优化ΔG*H和ΔG*OH,同时为*H和*OH的吸附提供活性位点。结果表明,Ru和Ni之间的异金属键合能有效地介导*H和*OH的吸附,接近最优的ΔG*H和ΔG*OH。
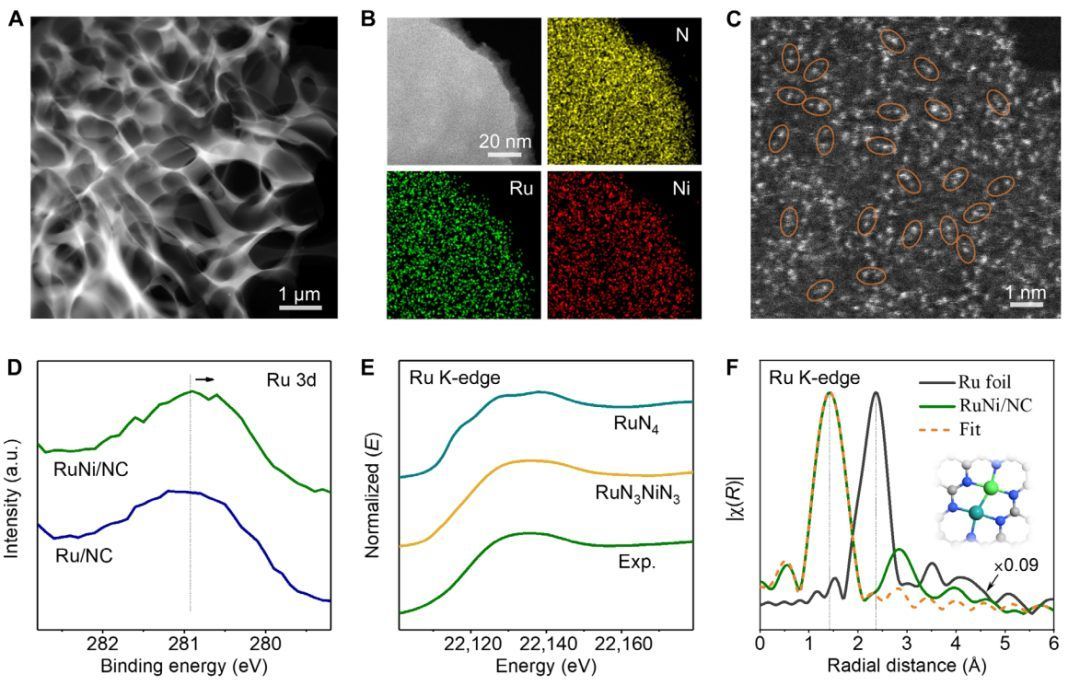
图2 RuNi/NC的结构表征
在理论预测的基础上,采用溶解-碳化法制备了N掺杂多孔碳负载的Ru-Ni双原子位点催化剂(RuNi/NC)。HAADF-STEM图像显示,RuNi/NC具有三维相互连接的碳框架,以及随机开放的多孔结构。原子分辨率HAADF-STEM图像显示,碳基底上分布着大量的Ru-Ni双原子对,原子间平均距离为2.4±0.12 Å。
XPS分析表明Ni的引入导致了RuNi/NC中Ru的电子发生变化。XAS分析及拟合结果表明,Ru、Ni的配位结构为RuN3NiN3。
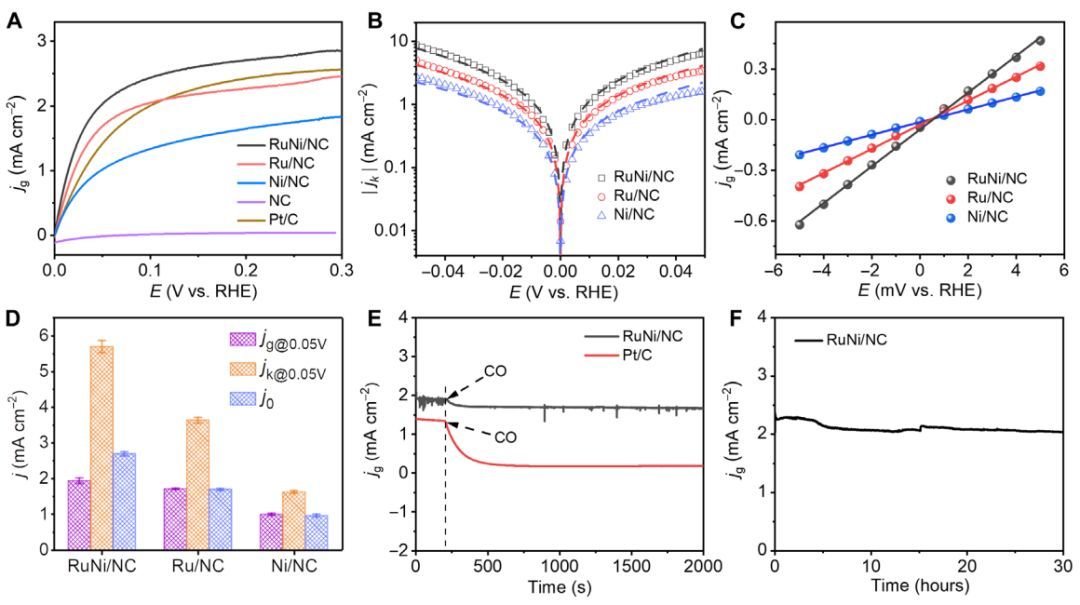
图3 HOR性能
在H2饱和的0.1 M KOH溶液中,考察了RuNi/NC、Ru/NC、Ni/NC和NC催化剂的HOR性能。HOR极化曲线可以看出,在整个电位范围内,RuNi/NC催化剂的电流密度高于其他催化剂,说明RuNi/NC具有良好的HOR活性。RuNi/NC的交换电流密度(j0)为2.69±0.06 mA cm-2,高于Ru/NC(1.69±0.03 mA cm-2)和Ni/NC(0.95±0.04 mA cm-2)。
进一步研究了在CO存在下RuNi/NC催化剂的HOR活性。在200 ppm的CO存在下,RuNi/NC催化剂在50 mV下的总电流密度仅衰减10%,远远优于Pt/C催化剂。耐久性试验也证实了RuNi/NC具有稳定的HOR活性和良好的CO耐受性。
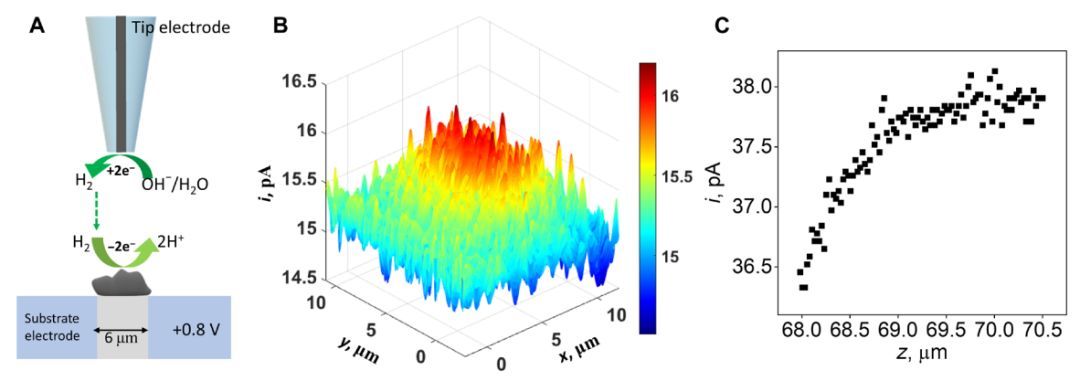
图4 SECM测定碱性溶液中RuNi/NC和NC催化剂的活性
利用扫描电化学显微镜(SECM)在尖端生成-基底收集(TG-SC)模式下,在pH为10的碱性0.1 M磷酸盐缓冲液(PB)中,测定了微米级RuNi/NC对HOR的催化活性。尖端H2O/OH-还原生成的H2扩散到基底中并被催化剂所氧化。在TG-SC图像中,由于RuNi/NC具有增强的HOR动力学,导致基底电流(~16 pA)高于背景电流(~15.3 pA)。
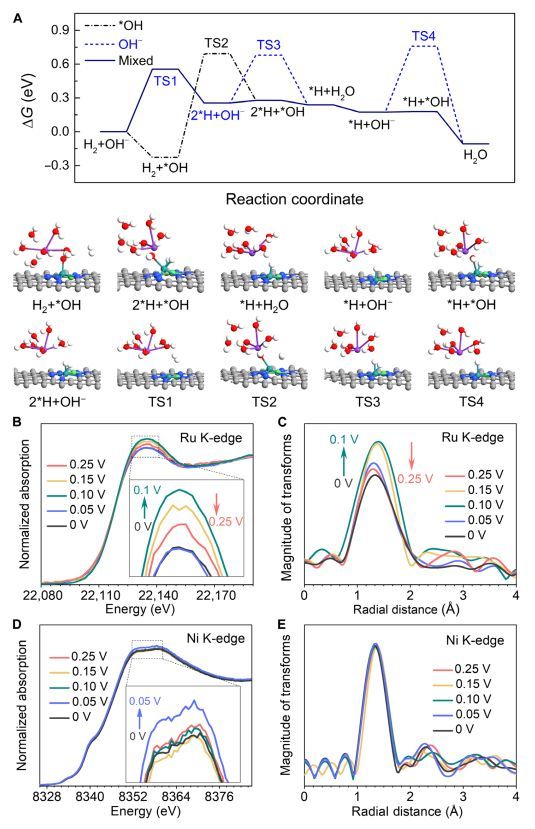
图5 RuNi/NC上的HOR机制
进一步进行了DFT计算,以探索H2的解离和H2O在*H和*OH/OH-之间的生成。考虑了OH-吸附和H2解离两种不同的顺序,即(i)OH-途径:H2直接解离为两个*H(Tafel步骤),吸附在Ru顶位点和Ru-Ni桥位点上,然后被吸附的*H与水溶液中的OH-结合(Volmer步骤);(ii)*OH途径:OH-先吸附在Ru位点上,然后H2解离成两个*H吸附在Ru顶部位点和Ru-Ni桥位点上,再吸附*H和*OH结合生成H2O,如图5A所示。
在本文,作者认为反应机制是一种混合途径:首先,在Ru-Ni DASC中,OH-留在水溶液中或吸附在Ru原子上时,H2解离为2个*H(考虑到TS2的ΔG比TS1大),然后OH-吸附在Ru位点上。第二个*H更容易与*OH结合,形成H2O。与SACs相比,Ru-Ni DASCs中的Ru和Ni原子不仅为H2解离的混合途径提供了活性位点,而且促进了*OH的吸附与H2O的生成,这对提高HOR性能有显著贡献。
然后,在H2饱和的0.1 M KOH电解液中,对RuNi/NC的Ru和Ni的K边进行原位XAFS测量,以验证所提出的反应机理。从图5B可以看出,Ru的K边XANES光谱的主峰从0到0.1 V升高,从0.1到0.25 V降低,说明Ru 5p轨道的未占据态从0到0.1 V发生增加,从0.1到0.25 V发生减少。Ru的K边FT-EXAFS光谱的第一壳层峰也有相同的变化趋势。增加的原因是*OH吸附在Ru上,减少的原因是*OH脱附导致水分子的释放。
相比之下,Ni的K边XANES光谱的强度仅从0到0.05 V发生增加,超过0.05 V后几乎恢复到原来的值(图5D),而Ni的K边FT-EXAFS谱的第一壳层峰几乎没有变化。分子H2解离和吸附在Ni顶点上是导致XANES谱峰增强的主要原因。这些结果与图5A中的DFT计算结果一致,支持本文所提出的机理。
文献信息
Design of Ru-Ni diatomic sites for efficient alkaline hydrogen oxidation,Science Advances,2022.
https://www.science.org/doi/10.1126/sciadv.abm3779
