大家好!今天我要向大家介绍一项关于生物相容性核壳微针传感器的研究——《Biocompatible Core–Shell Microneedle Sensor Filled with Zwitterionic Polymer Hydrogel for Rapid Continuous Transdermal Monitoring》发表于《ACS Nano》,该传感器填充两性离子聚合物水凝胶,用于快速连续透皮监测。这项研究为无创连续监测组织间液(ISF)中的生物标志物提供了一种创新的解决方案,具有重要的科学意义和应用前景。
*本文只做阅读笔记分享*
一、研究背景
(一)微针技术的优势与潜力
微针(MN)技术在生物监测领域具有巨大潜力,它能够以微创或无创的方式获取ISF,从而实现对临床相关生物标志物(如葡萄糖)的实时监测。ISF与血液浓度密切相关,且在皮肤表面附近易于获取,其含量约为血液的三倍,为生物标志物分析提供了理想的替代样本。例如,与传统的连续血糖监测方法相比,MN技术能够以更浅的深度穿透真皮,避免了神经末梢和毛细血管床的损伤,实现了无痛、微创的血糖监测。

(二)现有微针传感器的问题与挑战
然而,当前基于MN的电化学传感器仍面临诸多挑战。在传感层构建方面,存在生物分子泄漏、界面失效和非特异性吸附等问题。传统的MN传感器设计,如将传感组件置于MN尖端的方式,虽然实现了原位连续监测,但由于表皮插入和皮下摩擦,容易导致生物识别元件(如酶)的功能损失、潜在损伤和变性,从而影响传感器的准确性和稳定性。例如,一些MN传感器在长期使用过程中,酶活性下降,导致传感性能降低。此外,在电极材料选择和制备工艺上,也存在一些局限性,如金属化过程中的纳米晶界形成降低了电极的延展性,以及生物污损对传感器性能的影响等。
二、研究内容
(一)核壳微针传感器的设计理念
为解决上述问题,本研究提出了一种创新的核壳MN结构设计。利用空心MN内部通道封装两性离子聚合物水凝胶传感层,这种设计不仅将传感层与皮下组织物理隔离,减少了摩擦和损伤,还避免了额外保护涂层的使用,降低了分析物扩散的阻力。同时,水凝胶的填充充分利用了MN的三维结构,实现了生物识别元件的高密度负载,提高了传感器的传感能力。

(二)传感器的制备工艺
1、PLA空心微针的制备
采用拉伸光刻与溶液浇铸法制备PLA空心微针。首先,利用硅柱制作不同设计的超高纵横比SU-8MN模具。通过控制硅柱尺寸和拉伸速度,可获得具有不同直径和形状的MN。例如,在300-1000μm的硅柱尺寸范围和25-50μm/s的拉伸速度下,能制备出高成型率和一致性的SU-8MN。随后,将PLA/CHCl₃溶液浇铸在SU-8MN表面,待溶剂蒸发后,剥离得到PLA空心微针。通过调整温度可控制溶剂蒸发速率,进而调整微针的结构,如在较低温度下可形成更薄的尖端和更光滑的基底。
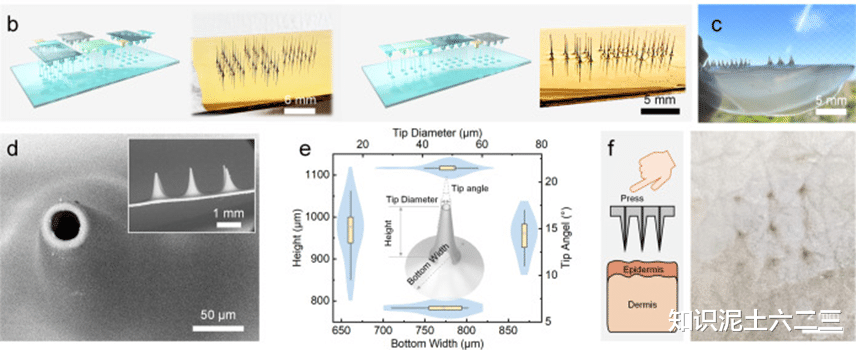
2、Au金属化
为使PLA空心MN具备电极功能,采用无氰化学镀Au工艺。先对PLAMN进行化学蚀刻,以增加表面面积和亲水性。然后,依次进行表面激活、敏化和镀Au步骤。激活过程使用带正电荷的表面活性剂,敏化则使用铂胶体,镀Au溶液中含有HAuCl₄和H₂O₂。在室温下,几分钟内即可在PLA表面形成光滑、连续且具有高导电性和柔韧性的Au涂层。镀后进行退火处理,可增强PLA与Au之间的连接,提高电极的稳定性。

3、含酶氧化还原两性离子聚合物水凝胶的构建
合成聚(MPC-co-MNHS)(PMS)共聚物,并通过与AFc反应形成具有氧化还原能力的PMMFc。接着,将PMMFc与GOD结合,制备出PMMFc-GOD水凝胶。该水凝胶具有良好的扩散效率和抗污性能,其独特的两性离子结构能够有效抵抗生物污损,同时为酶提供了稳定的微环境,有利于保持酶的活性。

(三)传感器性能测试与分析
1、电化学性能测试
通过CV和计时电流法研究PMMFc-GOD电极对葡萄糖的传感行为。在PBS缓冲液中,该电极对葡萄糖检测的线性范围为2-16mM,灵敏度约为5.48μAcm⁻²mM⁻¹。在连续监测实验中,电极在5mM葡萄糖溶液中能保持稳定的电流响应,超过12小时后仍能维持初始响应电流的87%以上,表明其具有良好的稳定性和可靠性。

2、抗污性能评估
利用阻抗分析(EIS)、CV测量和荧光观察等方法评估电极的抗污性能。EIS测试结果显示,PMMFc-GOD涂层电极的界面转移电阻(Rct)比PLA/Au电极低约一个数量级,且在牛血清白蛋白(BSA)存在的情况下,其Rct几乎保持不变,而PLA/Au电极则因蛋白吸附导致Rct显著增加。
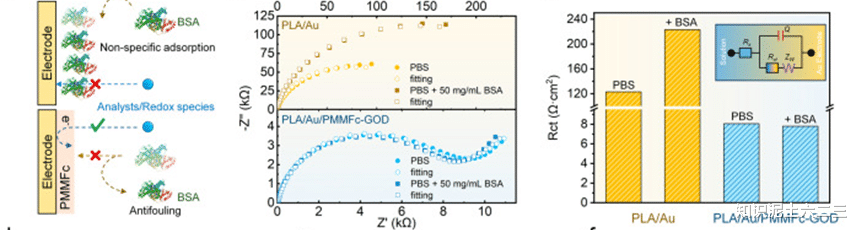
CV测量结果表明,在模拟蛋白污染物(50mg/mLBSA)存在时,PLA/Au电极的氧化还原电流在5分钟内迅速下降至初始值的65%,而PMMFc-GOD电极能保持稳定的高响应电流超过60分钟。荧光观察实验进一步证实,PMMFc-GOD水凝胶涂层能够有效抵抗蛋白质的非特异性吸附。

3、数值模拟分析
为深入了解葡萄糖在MN传感器内的扩散行为和电化学响应机制,进行了数值模拟。考虑了三种传感层组装情况:置于皮肤外(Design1)、位于MN上(Design2)和填充在MN通道内(Design3)。模拟结果显示,Design3在建立稳态浓度梯度方面速度最快,这得益于其更集中的水凝胶-真皮界面,能够更快地达到平衡且梯度更小。在模拟血糖上升过程中,传感器在真皮内(Design2和Design3)的响应时间比在皮肤外(Design1)更短,表明传感器与真皮直接接触有利于提高响应速度。此外,模拟还发现葡萄糖在真皮层中的扩散效率明显低于在水凝胶或间隙层中的扩散效率,这与实际生理情况相符,也进一步验证了该传感器设计的合理性。

4、传感器的实际应用评估
制备的MN传感器在Franz扩散池和猪皮肤上进行了实际应用测试。在Franz扩散池实验中,传感器的灵敏度达到7.70μAcm⁻²mM⁻¹,且在含有5mg/mLBSA的PBS缓冲液中,能够保持稳定的电流响应超过3天,展现出良好的抗污性能和稳定性。

在猪皮实验中,传感器的灵敏度为6.53nAcm⁻²mM⁻¹,且在9天的长期监测中表现出稳定的性能。

通过与平板传感器在缓冲液中的响应时间对比,发现MN传感器在缓冲液中的响应时间约为20秒,与数值模拟结果一致,且由于其结构优势,响应时间更短。

在猪皮上的实验虽然受到真皮层扩散屏障的影响,响应电流和灵敏度有所下降,但仍能在几分钟内达到稳定电流,与使用胶带剥离猪皮的体外葡萄糖扩散模型相当,且MN的插入有助于减少角质层引起的响应延迟,进一步证明了该传感器在实际应用中的可行性和有效性。

三、研究结论
本研究成功开发了一种基于核壳MN结构的透皮电化学传感器,该传感器通过优化设计和制备工艺,有效解决了传统MN传感器面临的稳定性和生物污损等问题。通过实验和数值模拟验证,该传感器在快速连续透皮监测ISF中的葡萄糖等生物标志物方面具有显著优势,表现出高灵敏度、快速响应、长期稳定性和优异的抗污性能。此外,传感器的生物安全性评估结果表明其具有良好的生物相容性,对细胞无毒副作用。在未来的研究中,将进一步优化传感器的无线信号转导和传输系统,实现多指标ISF生物标志物的同时监测,为可穿戴MN生物传感器在临床诊断和健康管理等领域的广泛应用奠定坚实基础。

四、一起来做做题吧
1、以下关于微针(MN)技术在生物监测领域优势的描述,不正确的是?
A.可实现无创或微创获取组织间液(ISF)进行实时监测。
B.MN结构设计灵活,应用广泛,包括ISF提取、生物传感等。
C.基于MN的酶电化学传感器灵敏度和选择性低,不具备商业化潜力。
D.MN能以较浅深度穿透真皮,避免损伤神经末梢和毛细血管床。
2、在PLA空心微针制备过程中,下列哪项操作与调整微针结构无关?
A.控制硅柱的尺寸。
B.改变拉伸速度。
C.调整浇铸PLA溶液的量。
D.控制溶剂蒸发的温度。
3、PLAMN进行Au金属化时,化学镀Au的过程不包括以下哪个步骤?
A.表面活化。
B.高温烧结。
C.敏化。
D.镀Au。
4、在含酶氧化还原两性离子聚合物水凝胶构建中,PMMFc是由什么反应生成的?
A.MPC与MNHS聚合。
B.PMS与AFc反应。
C.GOD与AFc结合。
D.MPC与AFc反应。
5、PMMFc-GOD电极在PBS缓冲液中对葡萄糖检测的线性范围是多少?
A.1-11mM。
B.2-16mM。
C.5-15mM。
D.10-20mM。
6、以下哪种方法不能用于评估电极的抗污性能?
A.电化学阻抗谱(EIS)。
B.原子力显微镜(AFM)。
C.循环伏安法(CV)。
D.荧光观察。
7、在葡萄糖扩散的数值模拟中,哪种传感层组装设计响应速度最快?
A.置于皮肤外(Design1)。
B.位于MN上(Design2)。
C.填充在MN通道内(Design3)。
D.三种设计响应速度相同。
8、MN传感器在Franz扩散池中的灵敏度是多少?
A.6.53nAcm⁻²mM⁻¹。
B.7.70μAcm⁻²mM⁻¹。
C.5.48μAcm⁻²mM⁻¹。
D.8.0μAcm⁻²mM⁻¹。
9、本研究未来的工作重点不包括以下哪项?
A.优化无线信号转导和传输系统。
B.进一步提高传感器的灵敏度。
C.实现多指标ISF生物标志物监测。
D.降低传感器的制备成本。
参考文献:
Zhou S, et al. Biocompatible Core-Shell Microneedle Sensor Filled with Zwitterionic Polymer Hydrogel for Rapid Continuous Transdermal Monitoring. ACS Nano. 2024 Oct 1;18(39):26541-26559.
