
--行业要闻—
2月1日,诺和诺德公布2022年业绩,全年总收入1769.54亿丹麦克朗(约合250.71亿美元),同比增长26%。其中,罕见病业务收入为205.42亿丹麦克朗(29.10亿美元,+7%),主要由血友病药物NovoSeven推动,销售额为83.08亿丹麦克朗(11.77亿美元,+15%)。
2月1日,诺华制药发布2022年第四季度及全年业绩。根据财报,2022全年诺华产品营收505.45亿美元(同比+4%cc),净利润69.55亿美元(-67%cc)。脊髓性肌萎缩症(SMA)基因疗法Zolgensma2022全年销售额为13.7亿美元,增长1%,第四季度销售额下降10%,该药目前已在全球47个国家或地区推出。

1月31日,uniQure和ApicBio宣布,已签署APB-102治疗超氧化物歧化酶1(SOD1)肌萎缩侧索硬化症(ALS)的全球许可协议。根据该协议,uniQure将支付1000万美元的首付款,获得APB-102的开发和商业化的全球权利,为其治疗神经疾病的基因疗法增添新的管线。

1月31日,DaewoongPharmaceutical与CSPharmaceuticals(CSP)达成独家许可协议。根据协议条款,Daewoong将授予CSP特发性肺纤维化和其他呼吸适应症治疗用药Bersiporocin在大中华区的独家开发和商业推广权,总对价高达3.36亿美元,包括7600万美元的预付款和开发里程碑付款以及两位数的净销售额分成。
--前沿进展--
1月30日,荣昌生物宣布,美国食品药品监督管理局(FDA)已批准泰它西普的新药临床试验(IND)申请,以推进其用于治疗重症肌无力(MG)患者的3期临床试验研究,并授予其快速通道资格认定。据了解,由北京医院许贤豪教授牵头完成的国内2期临床研究结果显示,泰它西普240mg组的QMG评分平均降低9.6分,具有临床意义的显著疗效,且体现出良好的有效性和安全性。
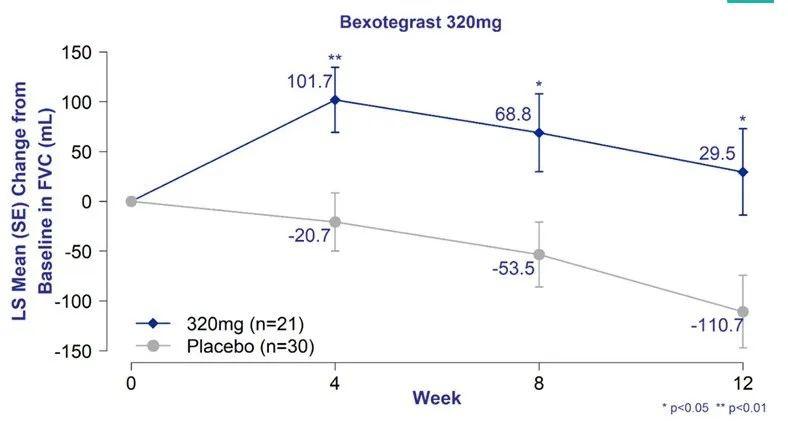
1月22日,PliantTherapeutics公布其药品bexotegrast(PLN-74809)于临床2a期试验治疗特发性肺纤维化(IPF)患者的中期数据。数据显示,与安慰剂组相比,320mgBexotegrast组在所有时间点的FVC均显著增加,超过所有低剂量组,并在12周时对FVC预计百分比(FVCpp)、QLF和促纤维化生物标志物显示出较强的治疗效果。Pliant预计于2023年年中启动临床2b期试验。
--医药速递—
1月31日,ReneoPharmaceuticals宣布美国FDA已授予mavodelpar(REN001)快速通道资格,用于长链3-羟基酰基辅酶a脱氢酶(LCHAD)缺乏症。据悉,LCHAD是长链脂肪酸氧化障碍(LC-FAOD)患者的主要基因型之一,临床表现为嗜睡、肝功能障碍、肌无力、肌肉疼痛或横纹肌溶解以及心脏、肾脏相关疾病,可导致永久性残疾或死亡。此前mavodelpar已获FDA授予的用于治疗原发性线粒体肌病(PMM)快速通道资格。
1月28日,华毅乐健宣布,其自研基因治疗产品GS1191-0445注射液用于A型血友病(HA)患者的临床试验申请,已获得中国国家药品监督管理局药品审评中心(CDE)批准。资料显示,GS1191-0445注射液是国内首个进入探索性临床试验阶段的A型血友病基因治疗产品,单次给药后已观察到长达1年多的良好维持疗效。

1月28日,CDE官网显示,纽福斯生物的第二款眼科基因治疗药物NFS-02眼用注射液在国内申报临床。据悉,NFS-02是一种重组腺相关病毒血清型2载体(rAAV2)的眼内注射基因治疗产品,已于2022年12月获FDA的新药临床试验(IND)许可,用于治疗ND1突变引起的Leber遗传性视神经病变(ND1-LHON)。
1月27日,辉大基因宣布,公司自主研发的眼科基因治疗候选药物HG004已获FDA授予新药临床试验(IND)许可,将在多国开展用于治疗RPE65基因突变引起的相关性视网膜病变的国际多中心临床试验。作为一种新型眼用注射剂,HG004在视网膜色素上皮(RPE)的转导效率至少是腺相关病毒血清型2(AAV2)的10倍,并具有降低临床载体剂量的潜力。
1月26日,Wakix®(替洛利生)获欧洲药品管理局(EMA)建议扩展新适应症人群,适用于6岁以上儿童及青少年发作性睡病的治疗。替洛利生是一种选择性组胺3(H3)受体拮抗剂/反向激动剂,是获得中美欧指南推荐,且在全球范围唯一获得发作性睡病适应症的非精神管控类药物,可同时改善发作性睡病四联症。
1月24日,BlueprintMedicines宣布,FDA已接受其药品Ayvakit(avapritinib)的补充新药申请(sNDA),用以治疗患有惰性系统性肥大细胞增多症(SM)的成人患者,并授予该申请优先审评资格。资料显示,SM是一种由于KIT蛋白D816V突变所驱动的罕见疾病,特征是肥大细胞不可控增生与活化,晚期SM患者会由于肥大细胞的浸润造成器官破坏并危及生命。
--友圈动态--
1月27日,“渐愈互助之家”发布一项关于支持渐冻症研究的资助方案——“春蕾”计划。作为该公益资助计划的发起人,原京东集团副总裁、渐冻症患者蔡磊宣布将携手破冰驿站直播间、攻克渐冻症慈善信托捐助1000万元。资助资金主要来源为破冰驿站直播间经营所得、攻克渐冻症慈善信托等相关渠道,不足部分将由蔡磊先生个人及家庭提供。
1月24日,天津友爱罕见病中心发布“甲型血友病基因治疗临床交流报名”公告。公告指出,甲型血友病基因治疗临床试验在国内开展1年多以来,已有三家国内基因治疗药物公司获国家药品监督管理局批准,正在开展不同阶段的临床试验。本次组织病友报名,旨在帮助血友病病友更好地了解基因治疗,以便及时解答病友关于临床研究的疑问。
