
编者按
2025年03月26至30日,第34届亚太肝病学会年会(APASL 2025)在中国北京隆重召开。会上,南开大学人民医院(天津市人民医院)韩涛教授团队共有5项研究入选大会进行交流,内容涵盖了慢加急性肝衰竭(ACLF)、肝癌、肝纤维化、肝硬化等领域。本刊特进行整理报道,供广大同道参考。
研究一解析慢加急性肝衰竭的演变过程:不同病情阶段的临床特征与预后转归(口头报告,大会编号: OP0024 )
第一作者:张倩,通讯作者:韩涛
研究背景
慢加急性肝衰竭(ACLF)是一种短期死亡率极高的临床综合征,但其全球定义尚未统一,导致早期识别与治疗困难。为了协调世界范围内各种定义之间的差异,更好地加强对ACLF的理解,近期有学者提出依据ACLF病情发展轨迹进行分层,即从尚未符合欧洲肝病学会-慢性肝衰竭联盟(EASL-CLIF)ACLF标准的前期阶段(EASL pre-ACLF)至符合EASL-CLIF ACLF标准的阶段,以更好反映病情严重程度的动态演变。本研究旨在验证这一基于严重程度的分层体系,并比较不同病因如乙型肝炎病毒(HBV)与酒精相关ACLF的临床特征及预后差异,评估不同预后评分系统在各阶段的预测效能。
研究方法
通过多中心回顾性研究,纳入因肝功能急性恶化住院的1193例患者,其中955例满足入排标准。根据病情严重程度,将整体研究队列、HBV及酒精不同病因队列,进一步分为EASL pre-ACLF组 (5≤TBIL<12 mg/dL+INR≥1.5) 和EASL-CLIF ACLF组 (TBIL≥12 mg/dL+INR≥1.5),研究流程图见图1。比较两组间患者的临床特征及预后,并应用ROC曲线评估预测多种预后评分系统对28天和90天病死率的预测效能。

图1. 研究人群筛选流程图
(源自APASL 2025会议)
研究结果
955例患者中,659例(69.01%)为HBV相关ACLF,296例(30.99%)为酒精相关ACLF。无论是整体人群还是HBV及酒精相关ACLF亚组,EASL-CLIF ACLF阶段患者的上消化道出血、细菌感染、肝性脑病和肝外器官衰竭发生率均显著高于EASL pre-ACLF阶段患者(P<0.05),且28天及90天病死率均显著升高(P<0.001)。在EASL pre-ACLF阶段,MELD-Na评分对28天及90天病死率的预测效能更优;而CLIF-C ACLF评分及COSSH-ACLF II评分对EASL-CLIF ACLF阶段患者的预后评估更具预测优势。

图2. 整体队列(a,d)、HBV病因队列(b,e)及酒精病因队列(c,f)中,EASL pre-ACLF阶段与EASL-CLIF ACLF阶段的28天及90天生存率比较
(源自APASL 2025会议)

图3. 预后评分系统预测整体队列 [EASL pre-ACLF (a) 和EASL-CLIF ACLF (b)],HBV病因队列 [EASL pre-ACLF (c) 和EASL-CLIF ACLF (d)] 及酒精病因队列 [EASL pre-ACLF (e) 和EASL-CLIF ACLF (f)] 的28天病死率的受试者工作特征曲线
(源自APASL 2025会议)

图4. 预后评分系统预测整体队列 [EASL pre-ACLF (a) 和EASL-CLIF ACLF (b)],HBV病因队列 [EASL pre-ACLF (c) 和EASL-CLIF ACLF (d)] 及酒精病因队列 [EASL pre-ACLF (e) 和EASL-CLIF ACLF (f)] 的90天病死率的受试者工作特征曲线
(源自APASL 2025会议)
研究结论
基于ACLF病情发展轨迹的分层(EASL pre-ACLF和EASL-CLIF ACLF),能够有效区分不同阶段ACLF患者的临床特征与预后转归。针对ACLF不同严重阶段可采用不同的预后评分系统,有助于提高预后评估的准确性,从而为ACLF的精准分层管理和制定个体化治疗策略提供依据,有助于提高患者生存率。
研究二基于吞噬调控因子的预后特征预测肝细胞癌的临床结局与免疫微环境
第一作者:崔浩,通讯作者:韩涛
研究背景
肝细胞癌(HCC)是全球最常见的恶性肿瘤之一,其发病率和死亡率在各类型肿瘤中均居前列。肿瘤免疫微环境(TIME)在其进展和治疗耐药中发挥关键作用,其中肿瘤相关巨噬细胞(TAMs)尤为重要,但其吞噬调控机制尚不明确。本研究旨在筛选吞噬调控相关基因(PRRGs),解析其促癌机制及预后价值,并构建PRRGs预后模型以评估免疫浸润特征与治疗反应。
研究方法
通过文献挖掘筛选PRRGs,通过GO/KEGG富集分析明确功能通路,基于单细胞RNA测序(GSE149614)验证PRRGs在库普弗细胞的富集。以TCGA-LIHC为训练队列,GSE14520、GSE76427为验证队列,利用单因素Cox和LASSO回归构建预后模型,并通过生存分析和ROC曲线评估效能。采用qRT-PCR验证84对肝癌及癌旁组织基因表达。结合CIBERSORT和ESTIMATE算法分析免疫浸润,基于GSE135222队列评估免疫检查点阻断(ICB)疗效。
研究结果
共筛选271个PRRGs,其富集于免疫激活与吞噬相关通路。45个调控因子(如SIRPA、FCGR2A、ICAM1、AXL)在库普弗细胞中高表达。最终建立包含13个基因(ALAD、BCOR、CADM1、CIT、EMC1、GRSF1、LCK、MUC12、NDUFC1、PODXL、RNF122、SIRPA、TM2D1)的预后模型,训练队列1/3/5年生存率AUC分别为0.758、0.736、0.692,验证队列GSE14520为0.702、0.734、0.656,GSE76427为0.781、0.767、0.905。
进一步的多因素Cox回归证实,基于该模型的风险评分是HCC的独立预后因子。qRT-PCR显示7个特征基因在肝癌与癌旁组织存在差异:ALAD、MUC12、NDUFC1在癌旁高表达,BCOR、EMC1、PODXL、TM2D1在肿瘤中上调。低表达ALAD和CADM1与分化差、AFP升高及预后不良相关(P<0.05)。低风险组免疫评分更高(P=0.003),且富含CD4+/CD8+T细胞、B细胞、NK细胞及树突状细胞,而高风险组M2巨噬细胞浸润显著。该模型预测低风险组对抗PD-1/PD-L1治疗响应更佳(P<0.0001)。
研究结论
本研究构建的PRRGs预后特征可有效预测HCC患者生存及免疫微环境,其风险评分能反映免疫浸润差异并指导个体化治疗策略。
研究三恩格列净减轻四氯化碳诱导的小鼠肝纤维化
第一作者:哈福双,通讯作者:韩涛
研究背景
肝纤维化是慢性肝病的病理特征之一,具有潜在的可逆性。然而,目前尚缺乏公认有效的抗肝纤维化化学药物或者生物制剂。本研究旨在探讨钠-葡萄糖协同转运蛋白2抑制剂(SGLT2i)恩格列净对四氯化碳(CCl4)诱导的小鼠肝纤维化的作用。
研究方法
实验小鼠分为三组:正常对照组、肝纤维化模型组和恩格列净治疗组,评估各组肝功能和肝脏组织学变化,并进行胰岛素耐受试验。
研究结果
与肝纤维化组小鼠相比,恩格列净治疗组肝组织的炎症、坏死和纤维化明显减轻,恩格列净治疗组的超氧化物歧化酶、丙二醛、谷胱甘肽过氧化物酶和过氧化氢酶的水平更接近正常对照组。治疗组Keap1阳性细胞数量较肝纤维化组明显减少。恩格列净治疗并未增加肝纤维化小鼠的ALT及AST水平,胰岛素耐受试验也未观察到血糖水平的降低。
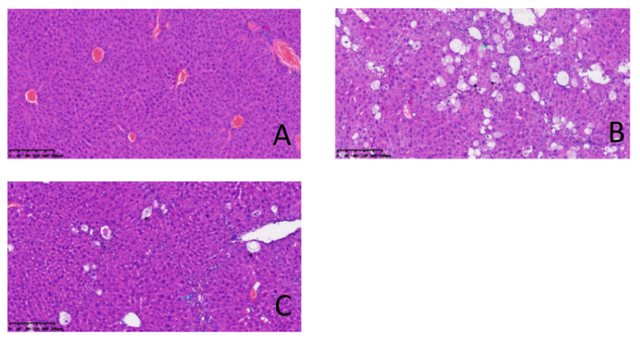
图5. 肝脏HE染色(×100):A为正常对照组,B为肝纤维化组;C为恩格列净治疗组
(源自APASL 2025会议)
研究结论
恩格列净具有一定的抗肝纤维化作用,且未引起肝纤维化小鼠肝功能的恶化,也未诱发低血糖,其减轻肝细胞坏死和纤维化的作用机制可能涉及调节Keap1-核因子E2相关因子2(Nrf2)信号通路,从而减少肝组织的氧化应激。
研究四GPR56通过抑制肝细胞焦亡减轻实验性肝纤维化
第一作者:时哲敏 通讯作者:韩涛,洪伟
研究背景
肝纤维化是慢性肝损伤的共同病理反应,及时有效的干预可以控制或逆转早期肝纤维化,阻止其进一步进展为肝硬化或肝细胞癌。目前临床上对肝纤维化仍缺乏有效的诊治手段,因此阐明肝纤维化的发病机理并寻找能够有效阻止或者逆转肝纤维化的治疗手段已经成为当务之急。
GPR56属于GPCR超家族,广泛分布于人体各器官如脑、甲状腺、肾脏、骨骼肌和造血系统,对多种疾病的发生发展有调控作用。然而GPR56在肝纤维化中的作用尚未见报道。本研究通过生物信息学及体内外实验来阐明GPR56在肝纤维化中的功能及作用机制,为肝纤维化诊断和治疗提供新靶点。
研究方法
构建CCl4及胆管结扎(BDL)诱导的小鼠肝纤维化模型,在小鼠的肝纤维化组织中以及患者的纤维化肝组织中,通过western blot, qRT-PCR及免疫组化检测GPR56的表达水平。结合GO以及WGCNA分析预测GPR56的功能,同时通过体内外实验对GPR56进行敲低及过表达后检测其下游信号通路及肝细胞焦亡相关指标的表达变化。
研究结果
GPR56在患者及小鼠的纤维化肝组织中以及CCl4诱导的纤维化小鼠原代肝细胞中显著过表达。GO以及WGCNA分析预测GPR56与炎症及ECM生成相关。体内实验揭示肝细胞特异性过表达GPR56可以减轻炎症小体诱导的肝细胞焦亡,敲除GPR56则加重肝细胞焦亡。体外实验发现GPR56通过抑制肝细胞焦亡进而抑制肝星状细胞激活。GPR5可通过抑制NF-κB通路减轻肝细胞焦亡。

图6. GPR56在小鼠及患者纤维化肝组织中过表达
(源自APASL 2025会议)
研究结论
本研究发现GPR56通过抑制肝细胞焦亡从而减轻肝纤维化,为GPR56成为肝纤维化诊治的潜在靶点提供一定的理论和实验依据。
研究五肝硬化伴重度食管胃底静脉曲张破裂出血患者内镜下治疗术后危险因素分析
第一作者:周佳美,通讯作者:韩涛
研究目的
本研究旨在探讨肝硬化重度食管胃静脉曲张患者内镜下治疗术后1年内门静脉血栓(portal vein thrombosis, PVT)发生的危险因素以及PVT对患者远期预后的影响。
研究方法
回顾性分析2014年1月-2017年12月因肝硬化重度食管胃静脉曲张或破裂出血首次内镜下治疗且无PVT的755例患者的临床资料,观察1年内PVT的发生情况,二元Logistic回归分析PVT发生的影响因素,并对1年内发生PVT的患者和未发生PVT患者进行生存分析。
研究结果
纳入的755例患者中,43例发生PVT,1年内PVT发生率为5.70%。食管胃底静脉曲张破裂出血史和血白蛋白水平是PVT发生的独立影响因素(P<0.05),PVT组肝病相关死亡人数多于无PVT组,PVT组累积生存率低于无PVT组,差异有统计学意义(P<0.05)。
研究结论
食管胃底静脉曲张破裂出血史和血白蛋白水平是肝硬化重度食管胃静脉曲张患者内镜下治疗术后1年内PVT发生的独立影响因素,PVT对肝硬化患者的长期预后有不利影响。
