海南近年来在细胞疗法领域取得突破性进展,核心驱动力源于一系列创新性政策法规的出台,这些政策不仅打破传统医疗监管框架,更通过“先行先试”机制为细胞治疗技术研发、临床试验及商业化应用开辟绿色通道。以下从政策框架、核心突破、实施成效及未来方向四个维度进行深度解读。

一、政策框架:构建“立法+先行区”双引擎驱动体系
1、顶层设计:自贸港法规赋予医疗创新特区权限
(1)法律依据:2023年《海南自由贸易港博鳌乐城国际医疗旅游先行区条例》修订版,明确赋予乐城先行区“特许医疗政策”,允许开展尚未在国内上市的细胞治疗技术临床转化。
(2)监管创新:设立“医疗技术评估委员会”,简化细胞疗法临床试验备案流程,缩短审批周期至3-6个月(对比传统药物审批的2-3年)。
2、先行区政策叠加优势
(1)特许药械进口:允许进口未在中国注册的细胞治疗设备及试剂,如GMP级细胞培养系统、基因编辑工具。
(2)真实世界数据应用试点:通过临床试验数据与真实世界数据联动,加速产品上市(如2023年PD-1单抗“特瑞普利”基于乐城数据获批)。
(3)人才与资金支持:设立医疗创新专项基金,提供细胞企业最高3000万元研发补贴;实施医疗人才“多执业地点注册”,吸引国际专家团队落地。
二、核心政策突破:破解细胞疗法临床转化瓶颈
1、细胞治疗技术准入机制改革
(1)首批14项技术落地(2025年):政策突破传统“药品”审批路径,通过“医疗技术备案制”允许三甲医院直接申请开展细胞治疗项目(如博鳌超级医院获批CAR-T肿瘤免疫治疗)。
(2)自体细胞疗法监管宽松:对使用患者自体细胞的疗法(如肺上皮细胞再生)实施“医疗机构伦理审查+备案”制度,无需药品注册审批。
2、产业链协同政策
(1)GMP生产中心集群建设:支持乐城建设国际级细胞制剂生产平台(如博鳌未来医院细胞工厂),提供CDMO服务(合同研发生产)降低企业成本。
(2)医保与支付创新:探索将特定细胞疗法纳入商业保险(如2024年“乐城全球特药险”覆盖部分CAR-T项目),缓解患者经济负担。
三、核心政策文件及关键条款
1、《海南自由贸易港博鳌乐城国际医疗旅游先行区条例》(2023年修订版)
2、发布机构:海南省人民代表大会常务委员会
3、核心条款:
(1)第23条:授权乐城先行区开展“特许医疗政策”,允许使用未在国内注册的细胞治疗技术(如嵌合抗原受体T细胞疗法(CAR-T)、干细胞治疗等)进行临床试验和转化应用。
(2)第28条:建立“医疗技术评估委员会”,负责细胞治疗技术的伦理审查、安全评估及备案管理,简化审批流程(备案时限缩短至30个工作日)。
(3)第35条:支持进口国际先进的细胞治疗设备、试剂及耗材,允许使用未获中国NMPA批准的药品、器械(需通过医疗技术评估)。
4、《海南博鳌乐城国际医疗旅游先行区细胞治疗产业发展支持措施》(2024年)
(1)发布机构:海南省卫健委、乐城管理局
(2)关键内容:
资金支持:设立5亿元细胞治疗专项基金,对临床前研究、临床试验及产业化项目给予最高3000万元补贴。
人才激励:对细胞治疗领域高层次人才提供个人所得税最高15%优惠,并允许境外医师“多点执业”。
临床试验加速:允许企业使用乐城先行区**真实世界数据(RWD)**支持产品注册申报,缩短上市周期。
5、《海南自由贸易港药品进口便利化管理办法》(2023年)
(1)发布机构:海南省药监局
(2)与细胞治疗相关条款:
a)第12条:对乐城先行区内医疗机构进口的细胞治疗用药品、试剂及设备,实行“白名单”管理,简化通关手续,缩短至48小时内完成审批。
b)第15条:允许医疗机构使用进口细胞治疗产品开展“同情用药”,为急需患者提供救治途径。
6、《海南自由贸易港生物医学产业知识产权保护条例》(2024年)
(1)发布机构:海南省知识产权局
(2)关键条款:
a)第18条:对细胞治疗领域的核心专利(如基因编辑技术、细胞培养工艺)提供最长20年保护期,并设立快速维权通道。
b)第22条:支持细胞治疗企业通过知识产权质押融资,最高可获贷款金额的150%贴息支持。
四、政策实施案例与效果
1、政策落地案例
2023年:博鳌超级医院通过“医疗技术备案制”获批开展全球首个β地中海贫血CRISPR基因编辑细胞治疗项目,患者治疗费用降低30%。
2024年:某国内细胞治疗企业利用乐城真实世界数据,将一款NK细胞疗法上市周期缩短至18个月(传统路径需3-5年)。
2、产业集聚效应
截至2024年,乐城先行区已聚集23家细胞治疗企业,建成3个GMP级细胞制剂生产中心,年产能达50万份细胞制剂。
五、实施成效与挑战
1、临床转化加速
(1)截至2024年,乐城累计开展细胞治疗临床试验30余项,其中5项进入Ⅲ期临床(如针对糖尿病足溃疡的间充质干细胞疗法)。
(2)国际合作深化:与瑞士Cellartis、美国MD安德森癌症中心等建立联合实验室,推动技术跨境转移。
2、面临的挑战
(1)成本与可及性:高端细胞治疗费用仍较高(如CAR-T疗法超50万元),需进一步通过规模化生产降低成本。
(2)监管标准统一:自体细胞疗法与异体细胞产品的监管尺度需细化,避免伦理风险。
(3)人才缺口:高水平的细胞制备、质控团队仍需引进与培养。
六、未来政策方向:构建全球细胞治疗产业高地
1、政策升级计划
(1)“细胞治疗特区”立法:拟制定专项法规,明确细胞制剂的“医疗产品”属性,简化注册流程。
(2)数据跨境流动:探索与新加坡、香港等建立医疗数据共享机制,支持国际多中心临床试验。
2、产业生态构建
(1)产学研一体化:支持海南大学、中科院海南分院建立细胞治疗研究院,推动基础研究向临床转化。
(2)金融工具创新:设立细胞治疗专项股权基金,鼓励社会资本参与早期项目孵化。
结语:海南细胞疗法政策体系以“先行先试”为核心,通过制度创新破解技术转化痛点,逐步形成“研发-临床-生产-支付”全链条闭环。未来,随着政策持续迭代及产业生态完善,海南有望成为全球细胞治疗技术的“试验田”与“输出地”,推动中国生物医疗产业实现弯道超车。
埃泽思生物公司埃泽思生物( Applied Cell)总部位于上海,专注于细胞治疗、再生医学等相关领域上游产品的研发与生产,公司产品在细胞与基因治疗、细胞样本存储,药物发现,科学研究等领域有广泛应用。

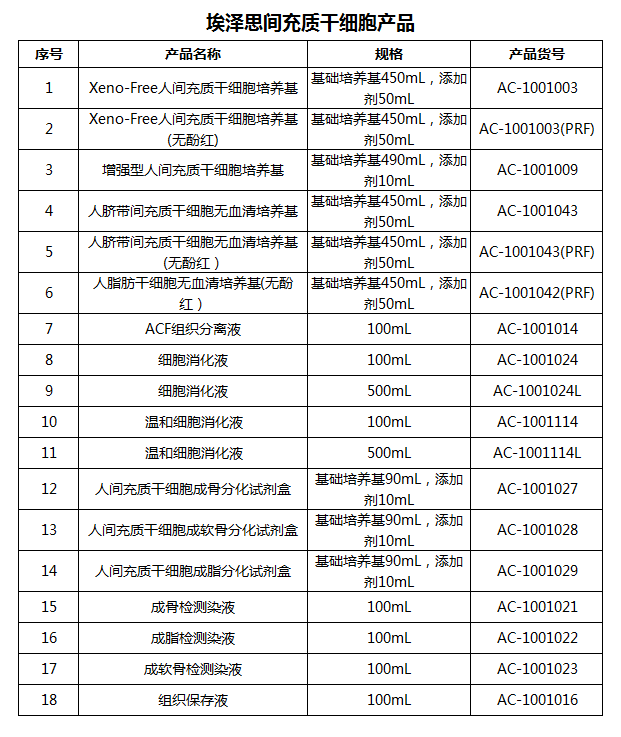
埃泽思生物MSC产品推荐
埃泽思生物(Applied Cell)总部位于上海,在苏州建有生产基地,专注于细胞治疗、再生医学等相关领域上游产品的研发与生产,公司产品在细胞与基因治疗、细胞样本存储,药物发现,科学研究等领域有广泛应用。
AC-1001042(PRF) 人脂肪干细胞无血清培养基(无酚红)

人脂肪干细胞无血清培养基是埃泽思生物(Applied Cell)自主研发的一款无外源动物成分的人脂肪干细胞培养基。可应用于人脂肪组织来源的人脂肪干细胞的扩增与传代培养,并保持其多向分化潜能。

产品特性
* 无外源动物蛋白成分,大大降低各类病毒、霉菌和支原体等的污染风险。
* 全程无血清生产,极大降低批次间差异。
* 培养过程无需包被培养板。
* 扩增效率高,24h 左右增殖翻倍,节省培养时间。
* 内毒素<0.06EU/ml,远低于中国药典水平。
AC-1001043 人脐带间充质干细胞无血清培养基

人脐带间充质干细胞无血清培养基是埃泽思生物(Applied Cell®)自主研发的一款无外源动物成分的人间充质干细胞培养基。可应用于人脐带组织来源的干细胞的原代分离、扩增与传代培养,并保持其多向分化潜能。本产品内毒素水平远低于中国药典标准,生产过程遵循 ISO9001 体系,并符合 GMP 指导原则。

产品特性
* 无外源动物蛋白成分,大大降低各类病毒、霉菌和支原体等的污染风险。
* 全程无血清生产,极大降低批次间差异。
* 可用于原代分离,且培养过程无需包被培养板。
* 扩增效率高,24h 左右增殖翻倍,节省培养时间。
* 内毒素<0.06EU/ml,远低于中国药典水平
