转基因动物能帮助缓解器官短缺吗?经过多年对异种器官移植的研究,该领域正处于一个转折点 —— 然而风险和伦理问题仍然存在。

美国有超过10万人在等待新的心脏、肾脏或其他器官。许多人将在等待中死去。一些科学家在猪的器官中看到了新的希望,这些器官已经被改造成可以在人体内工作。
这种被称为“异种移植”的物种间移植,为一个基本问题提供了一个技术解决方案:需要移植的人比可供移植的器官多,无论是活体器官还是脑死亡器官。
巴尔的摩马里兰大学心脏异种移植项目主任、外科医生默罕默德·曼苏尔·莫希丁说:“不幸的是,就在我们说话的时候,有人正在等待器官移植而死去。”
在过去的几年里,美国和中国的一些人接受了经过特殊改造的猪肾脏、心脏和肝脏,但正如《2024年动物生物科学年度评论》所指出的那样,让这些器官在人体中安全运作是一项巨大的挑战。现在,由于技术和医学的进步,位于马里兰州银泉市的联合治疗公司(United Therapeutics)开始了首次正式的异种器官移植临床试验,许多研究人员认为,这一手术最终可能会成为常规手术。
然而,仍然存在一些问题,包括猪器官将病毒传播给人类的风险,以及一些伦理问题。以下是这项研究的状态以及未来可能发生的事情。
与拒绝作斗争
在经历了漫长的动物移植实验之后,科学家们把目光集中在猪或迷你猪身上,作为器官来源。这种动物繁殖和生长速度很快,它们的器官大小适中,而且没有多少病原体会感染猪和人。
“我认为猪几乎是人类移植的理想供体,”eGenesis公司负责创新的高级副总裁秦文宁(音译)说。eGenesis是一家位于马萨诸塞州剑桥的公司,专门设计微型猪作为器官来源。
但如果没有对这些器官进行任何特殊的调整,人体会立即攻击它们。当人类抗体识别出猪器官血管上的三种外来糖分子时,这种“超急性排斥反应”就会启动。抗体粘附在细胞上,引发一系列凝血事件,阻断血液流动。秦文宁说:“在10分钟内,这个器官就会从粉红色变成黑色。”“器官死了。”
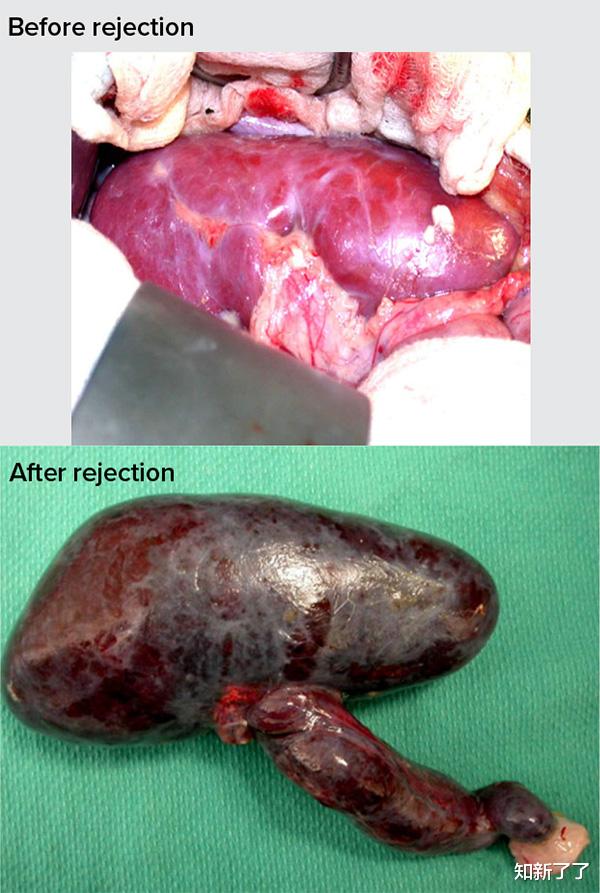
为了解决超急性排斥反应的问题,eGenesis和United Therapeutics等公司已经使用基于CRISPR/ cas的基因编辑系统来修改猪的DNA。例如,eGenesis破坏了负责这些问题猪糖的三个基因。但是,人体免疫系统仍然有办法识别和排斥外来器官 —— 只是多花点时间。曼苏尔·莫希丁说,为人对人移植而设计的标准免疫抑制药物不能完全阻止对异种移植的反应。
为了帮助解决这种后期排斥反应,两家公司还向猪细胞中添加了几个人类基因。这些基因产生的蛋白质位于细胞表面,将猪细胞伪装成人类细胞。2023年,eGenesis报告称,接受该公司猪肾移植的15只食蟹猴中,有5只存活了一年以上。
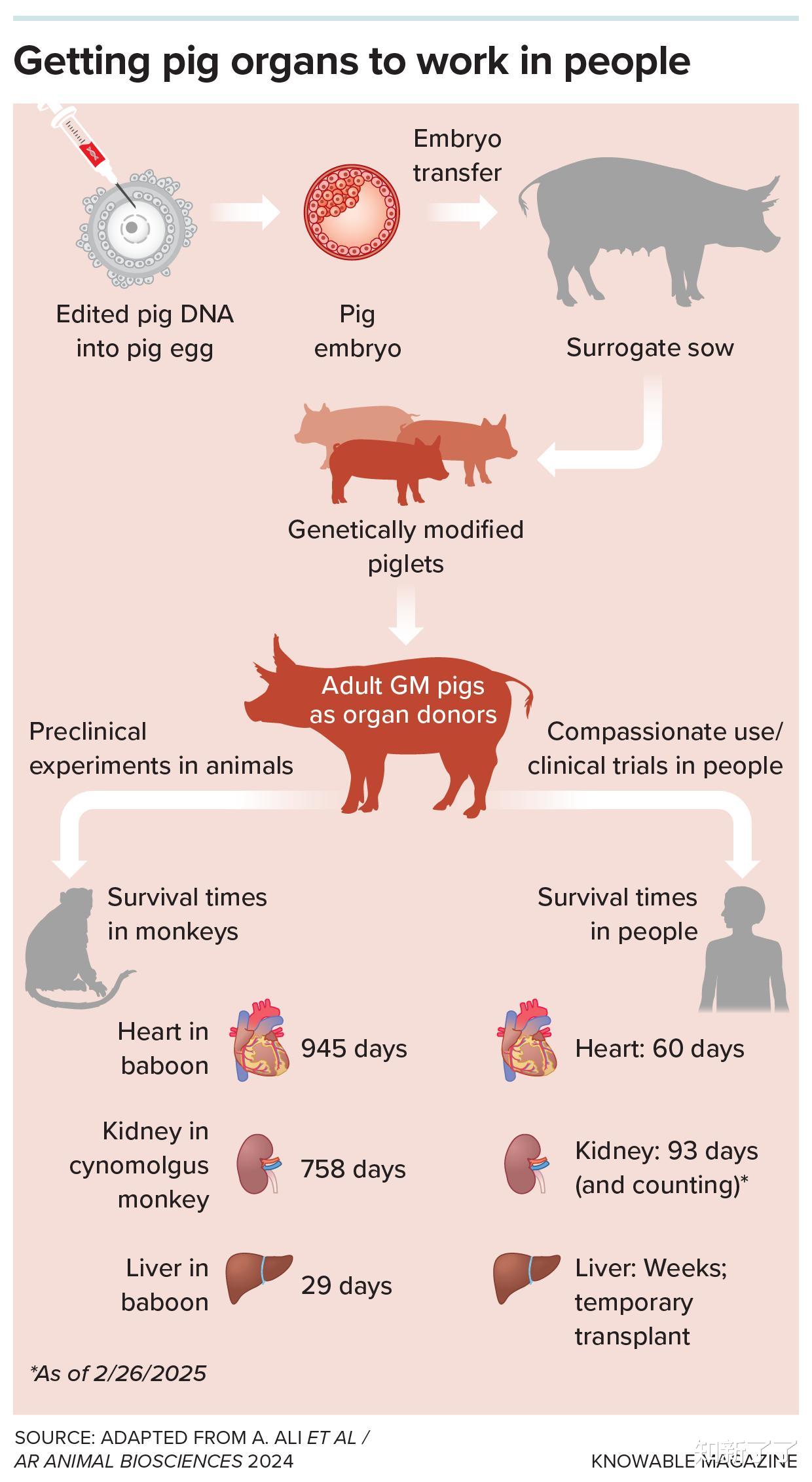
为了进一步抑制这种后期反应,曼苏尔·莫希丁和其他人已经开发出了进一步抑制免疫细胞反应的药物。在将猪心脏移植到五只狒狒腹部的实验中,这种治疗方法使移植的心脏存活了长达两年半。
其他研究人员希望通过训练器官接受者的免疫系统来忽略移植组织,无论是人类还是其他组织,从而消除对长期药物的需求。纽约市哥伦比亚大学转化免疫学中心主任梅根·赛克斯(Megan Sykes)正在解决这个问题,她将来自捐赠者免疫系统的额外组织 —— 骨髓细胞或胸腺细胞 —— 移植到接受者体内。人们希望这种方法能使受者的免疫系统对供体组织更具耐受性。她目前正在测试是否可以安全地从接受了猪器官和胸腺的狒狒身上撤出免疫抑制剂。(赛克斯获得了联合治疗公司(United Therapeutics)的研究经费。)
赛克斯说,这是异种器官移植领域“激动人心的时刻”。“我认为,在不久的将来,我们将在患者身上看到一些重大进展。”

伦理问题
到目前为止,在人类身上已经发生了十几起猪器官移植。第一批移植手术是在脑死亡患者身上进行的短期实验,因此对人体健康没有进一步的风险。在少数案例中,研究人员报告说,经过基因编辑的猪心脏可以跳动,肝脏可以产生胆汁,肾脏可以发挥功能,产生尿液,而不会立即产生排斥反应。
从那里开始,外科医生转移到活体器官接受者身上。这些志愿者要么病得太重,要么不符合人体器官移植的条件。
一些伦理学家对这些人类患者是如何被选择的提出了担忧。在这些早期移植中,医生接触符合条件的接受者,并根据“同情使用”途径向食品和药物管理局申请批准,该途径允许重病患者接受未经批准或未经测试的治疗。
锡拉丘兹纽约州立大学上州医科大学的生物伦理学家l·西德·约翰逊说:“这些病人得到了一个他们无法拒绝的条件。”约翰逊补充说:“我不认为人们为了存活三天、三周或六周而接受大手术、免疫抑制和各种风险。”
曼苏尔·莫希丁说,研究界“完全感谢”这些病人,他补充说,接受者很清楚这些实验程序的风险。他说,前四名接受猪肾或猪心脏移植的患者确实在几周或几个月内死亡,但医生和科学家从中吸取了宝贵的教训,例如,在移植前开始免疫抑制是很重要的。
这些发现帮助后来的移植手术进展得更好;阿拉巴马州的一名妇女于2024年11月在纽约大学朗格尼移植研究所接受了猪肾,并于2月底获准从纽约回家。
病毒外溢担忧
科学家们还担心,猪身上携带的病毒可能会感染人类移植接受者,甚至是与这些患者有接触的人。特别值得关注的是隐藏在猪基因组中的猪内源性逆转录病毒。CRISPR/Cas基因编辑再次提供了一个解决方案:eGenesis对其动物进行了额外的编辑;69个变化中有59个破坏了这些逆转录病毒。
一种不同的猪病毒确实出现在一位移植接受者身上,大卫·贝内特(David Bennett):他是第一个接受联合治疗公司(United Therapeutics)移植的猪心脏的人,在2022年进行了10次基因修改。移植后的测试在他的血液中发现了一些猪巨细胞病毒的DNA。移植小组的联合负责人莫希丁说,这种病毒可能是不活跃的,没有感染班尼特自己的任何细胞。贝内特在大约两个月后死于心脏衰竭,莫希丁说这可能是排异反应的结果。曼苏尔·莫希丁补充说,现在有了更灵敏的病毒检测方法。
即使是很小的病毒传播风险也会对人类产生广泛影响,因为当其他动物的病毒感染人类时,就会产生严重甚至大流行的病毒,如艾滋病毒,可能还有Covid-19。从一个物种到另一个物种的病毒会进化得更糟糕,尤其是在免疫系统较弱的人身上 —— 比如服用免疫抑制剂的病人。
因此,美国公共卫生局和国际异种移植协会建议对异种移植受者进行终身感染监测。但约翰逊指出,这意味着患者没有试验参与者通常享有的随时退出研究的权利。监控可能会扩展到与他们互动的人,这些人根本就没有同意参与这项研究。
另一种防止病毒的方法是将猪饲养在无菌环境中,但动物可能不太喜欢这样。猪是聪明的群居动物,它们真的很喜欢在泥里打滚;约翰逊说,无菌的实验室条件可能会对他们造成“心理和社会伤害”。虽然全世界每年屠宰近15亿头猪作为食物,但她说,这并不一定意味着创造更多的动物用于医疗用途是合乎道德的。
谁受益,谁买单?
如果异种器官移植成为标准医学,它将引发另一个伦理困境:这些器官将如何分配,谁将为此买单?曼苏尔·莫希丁说,马里兰大学的前两次移植手术每次花费约150万美元;其中一项由大学承担,另一项由研究发起人联合治疗公司承担。
约翰逊说:“我更愿意看到我们把时间和资源投入到其他事情上,比如预防器官衰竭、治疗器官衰竭和器官再生。”
然而,异种移植的支持者渴望开始临床试验。FDA已授权eGenesis及其合作者进行另外三例同情用途肾脏移植。首例手术于1月25日在一名新罕布什尔州男子身上进行,该患者已出院。与此同时,联合治疗公司(United Therapeutics)已经获得了FDA的批准,将在2025年中期开始对6名患者进行临床试验,可能会有50名患者接受试验。
“我们并不是说我们有一个完美的解决方案,”曼苏尔·莫希丁说。但他希望,最终异种移植能成为人体器官供应的有效补充。对猪器官的额外编辑或耐受性药物的进展可能使长期的免疫抑制变得不必要。
“如果你到了那个阶段,你就不会有器官短缺的问题,”曼苏尔·莫希丁说。
如果朋友们喜欢,敬请关注“知新了了”!
