
间充质干细胞(mesenchymal stem cells, MSC)是一类具有多分化潜能的干细胞,可分化形成骨细胞、软骨细胞和脂肪细胞等不同功能的细胞,并能够分泌多种细胞因子,调节免疫,促进组织损伤修复。MSC广泛存在于机体的多个器官,但其数量随年龄的增加而快速下降,并因机体衰老和疾病发生功能减退。MSC可分离自骨髓、脂肪、胎盘和脐带等组织,研究认为,从胎盘和脐带等年轻组织获得的MSC更具活力。MSC具有特殊的低免疫原性和免疫调节功能,异体MSC移植不引起明显排斥反应。基于以上多方面的优点,MSC是新药开发的热点,全球已有12个MSC产品(创新药)获批上市。
3D MSC具有多方面的功能优势。目前,MSC基本上均采用二维(2D)贴壁培养方法制备,虽能实现细胞数量的扩增,但细胞在扩增后发生较明显的功能衰退,表现为体积变大、迁徙能力减退、分泌细胞因子量下降和治疗效果不足等,突出体现在细胞静脉注射后不能通过肺循环进入体循环,绝大多数细胞截留于肺小血管并很快死亡,到达肺外脏器的细胞稀少,对肺外脏器疾病的治疗效果不佳。MSC的这些改变发生在体外培养后,是细胞培养条件与体内微环境差异过大所致。MSC在体内以三维(3D)聚集体方式生存,细胞间紧密接触,彼此间传递生物信号,调节生命活动;而在2D培养方法中细胞过于依赖对材料的贴壁黏附所介导的生物学信号,基因表达发生多方面适应性改变。
清华吴耀炯教授团队长期致力于MSC研究,发表MSC研究论文40余篇。针对MSC在2D培养中存在的问题,团队根据仿生原理,模拟MSC体内微环境,研发了基于生物发酵罐的3D MSC无载体培养技术,获多项发明专利。采用该技术制备的MSC较普通MSC体积小70%(图1),细胞表面迁徙关键受体CXCR4的表达显著增加(2D培养的MSC表达率<1%,3D培养的MSC表达率>40%),静脉和动脉注射后均不引起血管阻塞,免疫调节因子和生长因子(如TSG6、STC1、HGF、IL10、VEGF、LIF、BDNF等)表达水平显著提升(图2)。动物实验研究显示,静脉注射后,3D MSC广泛分布到各脏器,并靶向富集到缺血、炎症等损伤组织(图3),发挥修复作用,治疗效果大幅提高。
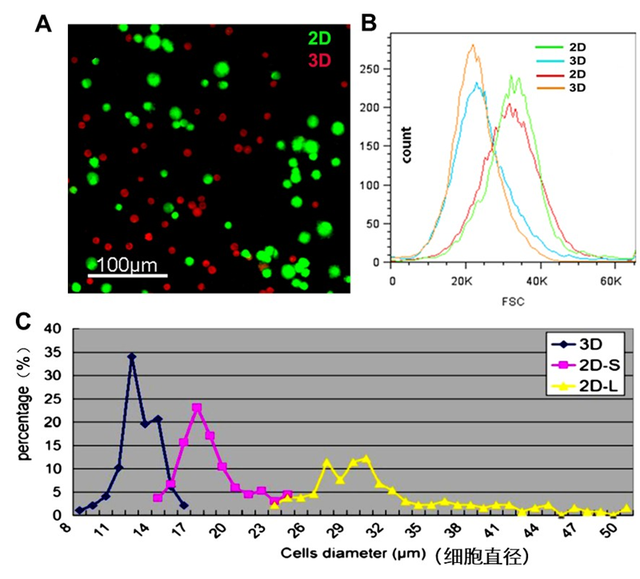
图1. 3D间充质干细胞与2D间充质干细胞对比分析:荧光显微镜下观察混合在一起的2D培养的普通间充质干细胞(绿色标记)和3D培养的间充质干细胞(红色标记),见前者体积明显大于后者。B. 流式细胞仪分析显示,3D间充质干细胞明显小于普通2D间充质干细胞。C. 细胞大小测量显示,3D间充质干细胞大小均一,平均直径13 mm,而普通2D间充质干细胞大小差异很大,平均直径大于20 mm。
基于吴教授团队的这项技术,国健清科生物医药科技(北京)有限公司从2021年开始进行3D MSC创新药生产工艺开发,所开发的人胎盘来源3D 间充质干细胞注射液制剂实现了单一胎盘组织稳定制备10万人份制剂的能力,第三方机构非临床药理试验证明其安全性和有效性较2D MSC有显著提升。基于该制剂的治疗代谢综合征的研究者发起的临床研究(IIT),初步结果显示,3D MSC对机体的多项机能有明显改善。该研究中,对受试者3D MSC治疗前后进行血液蛋白质组学分析,检测血液中7000多个蛋白的水平变化;结果显示,其中300多个蛋白水平治疗后有明显变化,反映了免疫功能、糖代谢和神经记忆等功能的改善,提示3D MSC有提升机体整体机能的趋势。
人胎盘来源3D 间充质干细胞注射液剂治疗缺血性脑梗死的IND临床试验和治疗杜氏肌营养不良(DMD)的IIT临床研究将在近期开始。

图2. 3D间充质干细胞表达更高水平的免疫调节因子和生长因子:RNA测序分析2D和3D培养的MSC,部分免疫调节因子和生长因子的表达情况。
— END —

新干细胞者说
- 科普 情怀 责任 -
