
培养基可以说是细胞培养技术中最重要的因素之一。作为支持细胞生存增殖的重要原料,培养基的质量直接影响了各种实验研究结果以及生物制药的生产速度。因此,对于研究细胞培养的研究人员来说,选择适合的培养基至关重要。而了解细胞培养基的发展历史,对加深培养基理解、明确培养基选择有着巨大的作用。
定义
细胞培养指从生物机体取出部分组织分散成单个细胞或直接从机体取出单个细胞,也可把体外培养细胞分散成单个细胞在体外条件下培养,细胞能继续存活与增殖。培养过程中细胞不再形成组织。发展与完善细胞培养技术围绕防止污染、改进培养方法、设计新型培养容器、设计不同的培养液等几个方面进行。
细胞培养基是一种含有适当营养物质、生长因子和其他必需组分的培养液,旨在为体外培养的细胞提供合适的环境,促使其生长、增殖和维持其功能。
(1)天然培养基:指来自动物体液或利用组织分离提取的一些培养基,如动物血浆、胚胎浸出液、血清和人血清,水解乳蛋白等。
(2)合成培养基:人工设计、配制的培养基,如MEM、199、DMEM、RPMI1640等。
历史和发展细胞培养基的发展经历了从简单到复杂,从天然成分到合成成分,再到定制化和三维培养基的演变。时间轴上看培养基开发可以分三个阶段:1957-1997(从血清到无血清);1998-2011(从无血清到化学成分确定);2011-当下(国内生物医药崛起)。
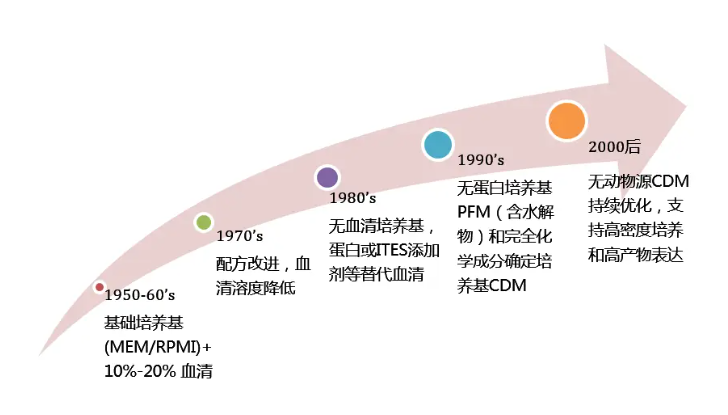
20世纪初期
早期的细胞培养基主要基于简单的无血清液体,其中营养物质主要来自于细菌或酵母的产物。然而,这些基础培养基在支持真正的动物细胞生长方面面临挑战。
20世纪20年代
Alexis Carrel和Montrose Burrows在成功培养出鸡胚心脏细胞后,引入了血清的使用。血清中的生长因子和营养物质促进了细胞的增殖,为细胞培养领域带来了显著的进展。
20世纪50年代
1957年科罗拉多大学医学系教授Dr. Theodore T. Puck从中国仓鼠中分离出卵巢细胞(Chinese Hamster Ovary,CHO),并成功进行体外连续传代培养。
培养基配方开发划时代的里程碑当属Harry Eagle博士分别于1955年和1959年在《科学》杂志上发表的两篇研究文章:1955年Eagle博士发布细胞基础培养基配方,并指出培养基是“一个包含无机盐、氨基酸、糖、维生素及其它必须营养物的等渗透压且具有pH缓冲能力的混合物”。Eagle在1959年的文章中提出了进一步改进的配方,并将该配方命名为“Minimal Essential Medium (MEM)”。MEM配方需要在10%以上的牛血清浓度下才能支持细胞生长,但即使在60年后的今天MEM培养基仍然被用于研究领域和一些疫苗生产工艺里,Eagle的研究工作无疑奠定了近代无血清培养基开发的基础。
20世纪80年代
到了1980年代,Gordon Sato博士和同期其他科学家进一步优化配方,并在替代血清方面取得突破:通过在基础培养基里添加蛋白(如胰岛素、转铁蛋白和白蛋白),可以在很大程度上替代血清。而后1982年Hiroki Murakami博士发现了另外一个在无血清条件下促进细胞倍增的主要成分乙醇胺,由此提出了ITES混合物作为无血清培养基的添加剂(Insulin、Transferrin、Ethanolamine和Selenium),ITES添加可以降低或者免除血清添加并实现高密度细胞培养。
20世纪90年代
历史性的突破在90年代, 1991年GIBCO推出CHO-S-SFM系列无血清培养基实现了CHO细胞完全无血清培养。白蛋白的主要功能是作为微量元素的载体,进一步研究发现微量元素等可以替代白蛋白的添加;类胰岛素生长因子IGF-1可以替代胰岛素;改进铁离子往细胞内转运可以替代转铁蛋白。90年代中期出现了最早的无蛋白培养基(Protein-free Medium,PFM),PFM 往往还含有蛋白水解物,而通过用植物来源的水解物代替动物蛋白胨进一步降低了动物来源成分的风险。
1997年GIBCO推出的CD CHO是第一个完全化学成分确定的培养基(Chemically-defined Medium,CDM),在那个水解物广泛采用的时代,CD CHO是个培养基开发历史上的里程碑,培养基开发从此进入一个全新的时代。
21世纪初
随着研究需求的不断增加,研究人员开始根据特定细胞类型的需求,调整和优化培养基的配方和组成。这些定制化的培养基更加精确地满足了特定细胞类型的生长、增殖和功能要求。
未来发展
近年来,随着三维培养和生物打印技术的发展,培养基也在不断创新和进化。传统的平面细胞培养已经不能满足复杂的组织和器官工程的需求,因此,研究人员开始开发新型的细胞培养基,如支架型培养基和生物透明基质,以提供更接近体内的三维环境。
细胞培养基的发展不仅体现在类型的多样化上,还包括了从天然成分到合成成分的转变,以及针对特定细胞类型的定制化培养基的出现。这些创新和发展使得细胞培养技术在生物制药、组织工程、再生医学和药物筛选等领域具有广泛的应用前景。
*参考文献
Yao T, Asayama Y. Animal-cell culturemedia: History, characteristics, and current issues. Reprod Med Biol. 2017;00:1–19.
Brunner D, Frank J, Appl H, Schoffl H, Pfaller W, Gstraunthaler G.Serum-free cell culture: the serum-free media interactive online database. ALTEX. 2010;27:53–62.
Corner GW. Warren Harmon Lewis. Biograph. Memoirs Natl Acad. Sci. 1967;39:323–358
Alexis Carrel, Montrose T. Burrows; CULTIVATION OF TISSUES IN VITRO AND ITS TECHNIQUE . J Exp Med 1 March 1911; 13 (3): 387–396. doi: https://doi.org/10.1084/jem.13.3.387
Applied Cell相关产品
AC-1001000人多能干细胞培养基
* 与E8体系对标,细胞增殖与形态无差异
* 无外源动物成分,降低各类病毒、霉菌和支原体等的污染风险
* 无血清成分,极大降低批次间差异
AC-1001001Advance人多能干细胞培养基
* 与mTesR体系对标,细胞增殖与形态无差异
* 无需滋养层细胞
* 营养更丰富,适用于大多数细胞系培养,且适用重编程过程细胞培养
* 成分明确,批间差异小
* 无外源动物成分,降低各类病毒、霉菌和支原体等的污染风险
AC-1001003PRF Xeno-Free人间充质干细胞培养基(无酚红)
* 专为脂肪间充质干细胞分离与扩增优化,传代稳定性高,最高可达20代
* 全程无血清生产,极大降低批次间差异
* 可用于原代分离,且培养过程无需包被培养板
* 无外源动物成分,降低各类病毒、霉菌和支原体等的污染风险
* 低热源,内毒素水平<0.12EU/m,适用于细胞治疗应用
AC-1001006无血清细胞冻存液(治疗级)
* 所有成分均为原料药级别,合规性高,很符合药品申报要求
* 低热源,减少外源内毒素干扰,适用于细胞治疗应用
* 无动物源成分,无各类病毒、细菌、菌和支原体等污染
* 冻存细胞复苏率高,常见细胞复苏率普遍高于95%
* 即用型产品,无需程序降温,冻存于-80℃冰箱或液氮中长期保存

