嗨,大家好!今天让我们一起来了解一下这篇《Hydrogel microparticles for biomedical applications》发表于《Nature Reviews Materials》上的一篇文章。水凝胶微粒可以由天然和合成聚合物制成,通过多种制备技术,如批量乳液、微流控乳液、光刻等,被赋予各种形状和大小。它具有可注射性、模块化和高孔隙率等独特性质,在细胞递送、药物输送、支架构建和生物制造等方面发挥着重要作用。接下来,让我们深入了解水凝胶微粒的神奇之处吧。
*本文只作阅读笔记分享*
一、引言
水凝胶在生物医学领域应用广泛,但传统大块水凝胶在某些应用中存在局限性,如注射和尺寸要求等。水凝胶因其高含水量、类似于天然细胞外基质的性质以及多样的性能,被广泛应用于细胞培养、组织工程和药物及蛋白质递送等领域。传统水凝胶通常交联成连续的体积(大块水凝胶),其外部尺寸在毫米级或更大,网孔尺寸在纳米级,以允许分子扩散。然而,大块水凝胶在某些应用中并不适用,例如需要注射或更小尺寸的情况。为了解决这些问题,人们开发了将水凝胶制成微尺度颗粒(约1 – 1000 μm)的技术,称为水凝胶微粒(HMPs)或微凝胶。

二、HMPs的制备
(一)制备技术
批量乳液法:使用不互溶的油和水凝胶前体溶液产生液滴,然后交联成HMPs。该方法简单、粒子生产速率高,兼容小分子和生长因子等生物活性物质以及细胞的封装。例如,在一些研究中,使用批量乳液法制备了含有丙烯酰化或甲基丙烯酰化的聚(乙二醇)(PEG)的水凝胶微粒。

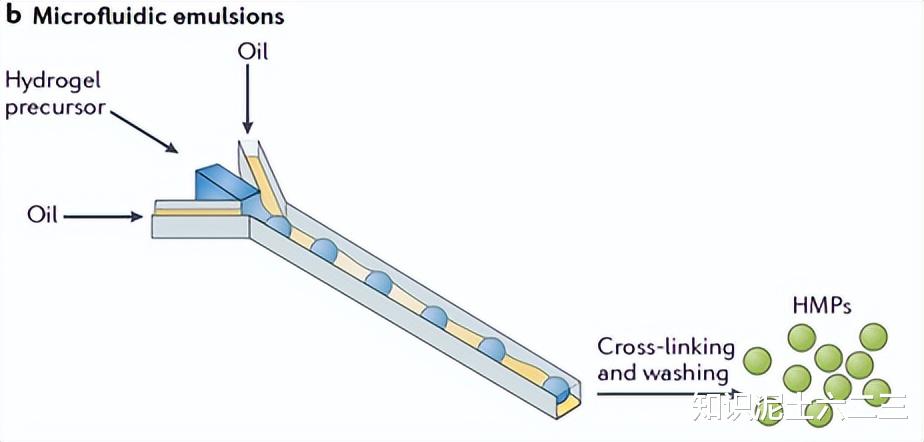
微流控乳液法:通过在交叉点引导油和水溶液的流动来控制液滴的形成,能够精确控制液滴直径,从而产生单分散的HMPs。例如,De Geest等人的研究中,利用微流控设备成功合成了单分散的可生物降解微凝胶。
光刻法:使用光聚合来在微尺度上模板水凝胶,包括印记光刻、光刻和流动光刻三种主要技术。例如,Lee等人的工作中,利用软膜变形和光流体无掩模光刻技术,成功制备了三维异构微结构。

电液动力喷雾法:在注射器针头尖端施加电压,使水凝胶前体溶液挤出形成带电液滴,然后在收集浴中交联。例如,Naqvi等人的研究中,使用该方法制备了用于微创递送的微胶囊和微载体。

机械破碎法:通过机械力将预形成的大块水凝胶破碎成微尺度颗粒。例如,Hinton等人的研究中,通过将交联的水凝胶机械破碎,成功制备了用于三维打印的微凝胶。

(二)技术比较
不同制备技术的关键工艺参数如粒子生产速率和粒径分布等差异显著。每种技术对水凝胶的处理都有一定的限制,例如水凝胶的流变学行为和交联机制必须与所选方法兼容。因此,应根据水凝胶的兼容性、所需的HMP特性(如尺寸和分散性)以及对专业设备的访问权限来选择制备技术。
三、HMPs系统的性质
(一)多尺度性质
HMP悬浮液:由稀HMPs在流体(如液体或空气)中组成,粒子间相互作用可忽略,其宏观力学和流变行为主要由连续相性质决定,单个HMP的机械性能取决于聚合物类型、密度和聚合物链间的交联程度。由于HMPs在悬浮液中的堆积密度相对较低,整体系统扩散率较高,但单个HMP内的扩散率由聚合物网格尺寸决定。

颗粒状水凝胶:由HMPs在堵塞状态下聚集而成,其聚合物网络在纳米尺度、单个HMP在微观尺度、颗粒状水凝胶在毫米尺度上起作用。当HMP堆积密度达到堵塞状态时,粒子间摩擦有助于从液态向固态转变。例如,在研究颗粒状水凝胶的堵塞转变时,Liu和Nagel等人的工作揭示了其与粒子堆积分数、应力和温度的关系。

HMP复合材料:HMPs被嵌入二次材料(如水凝胶)中,二次材料的机械性能通常主导复合系统的行为,除非HMPs的浓度很大且其尺寸和密度特定。例如,在一些研究中,通过将HMPs嵌入水凝胶中,制备了具有特定机械性能的复合材料,用于组织工程等领域。

(二)功能性质
可注射性:HMP系统可通过注射器或导管注射,这是由于其颗粒性质和小粒径。例如,改性透明质酸HMPs(通过微流控制备)被注射到心脏和大脑组织的缺血部位,以促进伤口愈合。在注射过程中,粒子堵塞可使HMPs像塞子一样移动,减少湍流流动,注射后HMPs恢复到具有凝胶状流变性质的粘弹性固体状态。
异质性:通过在粒子内或粒子间引入异质性,可使HMP系统更加复杂。例如,可以通过分隔单个HMP、改变表面化学性质、分层单个HMP或改变单个HMP内的孔隙率来实现粒子内异质性;通过改变水凝胶配方或负载类型来实现粒子间异质性。宏观尺度的各向异性可通过HMP堵塞来实现,从而允许物理分离不同的HMP聚集。
孔隙性:堆积的HMPs之间的间隙空间称为颗粒支架的孔隙,其大小与HMPs的大小成正比。例如,细胞可以轻松浸润和穿越颗粒支架而无需降解水凝胶,相对非多孔水凝胶,颗粒状水凝胶增加了流体流动、质量传输、渗透性和细胞浸润速率。孔隙的平均大小受HMP形状、大小、堆积密度和刚度的影响,外部力可能导致孔隙空间塌陷。

四、HMPs的应用
(一)细胞递送
细胞封装:一系列HMP制备技术(如批量乳液、微流控乳液、光刻和电液动力喷雾)兼容细胞封装,其中微流控乳液和光刻通常用于更好地控制粒子大小和形状,精确控制每个HMP中的细胞数量。通过控制粒子大小、密度和细胞在前体溶液中的浓度等参数,可以实现对细胞分布的控制。

应用案例:
骨缺损修复:例如,通过将BMSCs和骨形态发生蛋白- 2(BMP - 2)封装在使用微流控乳液设备制造的GelMA HMPs中,可生成可注射的成骨微组织,促进骨再生。在Zhao等人的研究中,展示了这种微球在快速生成骨组织构建物中的应用。

软骨组织修复:早期研究表明,BMSCs在微封装于HMPs后,在转化生长因子β3(TGF-β3)存在下可沿软骨生成谱系分化。例如,Li等人的工作中,通过组装含有间充质干细胞的微凝胶,促进了软骨组织的形成。

心脏修复:例如,将心脏侧群细胞(心脏中的一种祖细胞)接种到使用微流控乳液制成的GelMA HMPs表面,可促进细胞粘附和增殖,增强细胞在体内递送后的存活。在Feyen等人的研究中,展示了明胶微球在心脏祖细胞递送中的应用。

胰岛移植:胰岛封装在海藻酸盐HMPs中可用于治疗糖尿病,提供免疫保护屏障,增强营养物质和氧气与周围组织的交换,提高胰岛素向周围血管的转移。例如,Veiseh等人的研究中,观察到了不同尺寸的粒子在免疫反应中的差异。

(二)药物递送
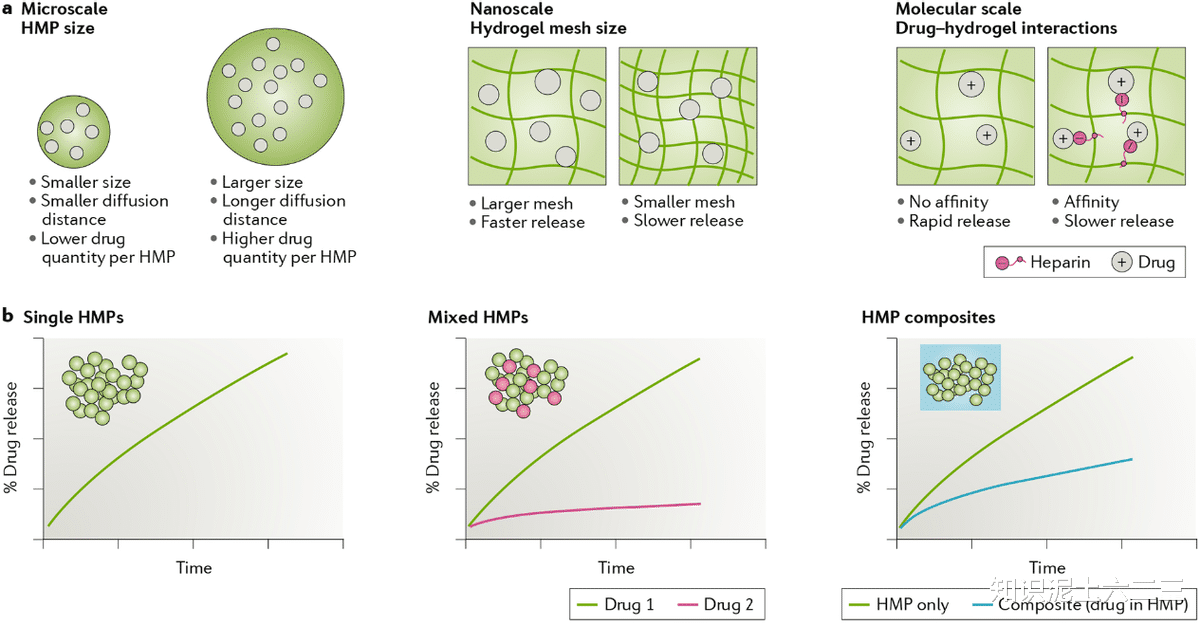
控制药物释放:HMPs用于药物递送的设计类似于大块水凝胶,但有一些独特的特点,如粒子大小和形状影响药物负载量,纳米尺度的粒子网格尺寸影响药物扩散,分子尺度的药物 - 水凝胶化学相互作用可延迟药物释放。多个粒子群体可混合在一起以开发具有多功能行为的注射剂,例如包含不同释放曲线和降解行为的药物。HMPs通常作为HMP复合材料被递送,其中它们被混合到二次大块水凝胶中。例如,在研究药物从HMPs释放的过程中,Chen等人的工作揭示了粒子大小对药物释放的影响。
(三)构建支架
设计颗粒状支架:借鉴大块水凝胶系统的许多概念,包括HMP退火方法、所得HMP和整体机械性能以及整合粘附和其他生物活性信号。许多颗粒状支架由相互退火的HMPs制成以提供稳定性,退火化学提供了对HMP工程的进一步控制,包括各种共价、可逆和静电键。机械性能对细胞至关重要,可通过调节单个HMP的刚度、退火化学、HMP间的退火量和粒子堆积密度来调制。HMP表面和粒子间的空隙空间构成细胞微环境的局部几何形状,影响细胞行为。通过功能化HMP聚合物与整合素结合肽(如精氨酸-甘氨酸-天冬氨酸(RGD))可改善细胞对HMP表面的亲和力。例如,在研究HMP退火方法对支架性能的影响时,Sheikhi等人的工作展示了通过微流控技术制备的可退火天然衍生蛋白微珠构建的底部向上水凝胶。

(四)生物制造
生物组装:早期例子包括使用流体生物组装过程,其中轨道式微流体通道用于引导PEGDA HMPs进入3D结构;外部磁场用于引导磁性纳米粒子负载的GelMA和PEG HMPs进入多层3D结构;以及使用声学波技术操纵HMPs组装3D结构。例如,在Chung等人的研究中,展示了利用轨道式微流体通道进行生物组装的过程。
生物打印:传统的可挤出生物墨水通常是单网络或双网络水凝胶,且其生物物理和生化性质保持均匀,但异质性对于打印复杂组织可能是理想的。例如,将PEG HMPs(通过微流控制备)与可挤出的大块水凝胶前体结合,可制备包含不同微尺度和宏观尺度环境的复合生物墨水。颗粒状水凝胶在挤出生物打印中的剪切稀化行为基于粒子间的物理相互作用,使其可用于制备更多样化的具有多功能行为的墨水。用于3D打印的支持水凝胶(如Carbopol)可与各种生物墨水兼容,用于打印多样化的多细胞结构。例如,在Highley等人的研究中,展示了使用颗粒状水凝胶进行生物打印的过程。

五、其他应用
美容领域:水凝胶(尤其是透明质酸)在美容行业中作为皮肤填充剂用于软组织增强已有数十年历史,通过机械破碎制备的HMPs可与额外的聚合物溶液混合以减少粒子间摩擦或直接作为堆积颗粒使用,较小的颗粒用于浅层填充,较大的颗粒用于深层组织填充。例如,Gilbert等人的研究中,讨论了透明质酸皮肤填充剂的基本科学原理。

细胞微拓扑学:HMPs可作为细胞的局部锚定点,为细胞粘附和接触引导提供微拓扑学线索,有助于恢复细胞外基质的机械性能。例如,Le等人的研究中,展示了微结构线索对细胞的重编程作用。

合成细胞生物学:HMPs可被设计成包含多个隔室,模拟细胞内不同的细胞器。例如,在Tan等人的研究中,使用微流控技术制备了包含多个隔室的异质多组分水凝胶颗粒,作为合成细胞用于不相容的串联反应。

六、未来展望
未来的研究将致力于改进HMPs的制备技术、拓展其应用领域并深入研究其性质和功能。例如,微流控技术和其他技术将继续改进,允许以高生产速率规模化制备具有均匀粒子群体和批间一致性的HMPs,拓宽用于制备HMPs的材料类别,引入刺激响应材料;计算模型和数值方法将有助于更好地设计和理解HMP系统;HMPs的应用领域将可能随着更多研究人员的认识而拓宽,与干细胞和药物设计技术的快速发展相结合,开发具有新的有趣性质的HMPs以更好地模拟天然组织的多尺度机械行为;微流控技术与HMPs和测序技术的整合将有助于在单细胞水平上进行高通量筛选;通过微调物理和生化性质来影响MAP支架中的细胞,以及探索MAP支架中局部空隙空间几何形状对细胞行为、多细胞排列和内源性修复的作用;基于HMPs的材料在生物制造中的应用仍处于起步阶段,未来可能会扩展可加工材料的范围,并制备出更多具有多功能行为的多样化墨水,同时在生物组装领域实现更高分辨率的3D定位。
参考文献:
Daly AC, et al. Hydrogel microparticles for biomedical applications. Nat Rev Mater. 2020 Jan;5(1):20-43.
