衰竭的肾脏:ICU内的肾脏替代治疗
梁宇鹏 翻译
重症行者翻译组
急性肾损伤(AKI)是影响ICU(重症监护病房)患者最常见的器官功能障碍之一。使用多种分类系统进行早期诊断和生物标志物辅助的干预是改善临床结局的关键。符合AKI诊断标准患者的自身因素决定了其接受肾脏替代治疗的最佳时机和方式。对于伴随急性肾损伤的外科ICU患者,在颅内压升高的管理、高危出血患者的抗凝处理以及增强影像的应用方面值得我们特别关注。本文对重症或因外伤接受手术患者在AKI诊断和治疗方面进行重点述评。
引言
急性肾损伤(AKI)影响到三分之一到二分之一入住重症监护病房(ICU)的患者,大约20%的患者需要接受肾脏替代治疗(RRT)。急性肾损伤是重症或因外伤接受手术治疗患者最常见的器官功能障碍。创伤患者AKI发生率在很大程度上受损伤类型所影响, 钝性创伤和烧伤患者AKI发生率分别高达25%和40%。最近的一项队列研究显示,于一级创伤中心就诊的患者AKI发生率为45%。69%的AKI患者(占所有就诊患者的31%)在入院时有肾功能障碍的迹象,但2天内大多数患者的肾功能即得到恢复。术后患者AKI的发生率从腹部大手术后的5%到原位肝移植后的近50%不等。创伤后和术后患者发生AKI的常见原因包括继发于低血容量、出血或休克引起肾缺血导致的急性肾小管坏死、全身炎症反应、包括抗生素和非甾体抗炎药在内的肾毒性药物以及源自横纹肌溶解的肌红蛋白所致的肾损伤。AKI的发生增加医院的总体死亡率。最近的一项在创伤并发严重AKI患者中进行的创伤质量改善过程(TQIP)分析显示此类患者的死亡率为28%。所有在进入ICU后第一周内需要RRT的AKI患者死亡风险达50%。
AKI的诊断和分类
AKI 的诊断和分类有不同的标准。最常用的三个分类系统包括(将肾功能损伤分为)风险、损伤、衰竭、肾功能丧失和终末期肾病(的)RIFLE(标准),急性肾损伤网络(AKIN)(标准)和改善全球肾脏病预后组织(KDIGO)标准。它们的评估标准都是肾功能障碍发生的时间、肾小球滤过率 (GFR)、血清肌酐和尿量 (UOP) 的某种组合。RIFLE分级系统由急性透析质量倡议组织于2004年首次引入。该系统将AKI定义为血清肌酐在 7 天内升高超过 50%,并基于GFR 和 UOP 下降以及肌酐升高的水平对AKI的阶段—风险、损伤和衰竭进行定义。AKIN在2007年对RIFLE进行了改进。将(RIFLE的)关键要素,症状初始时间缩短至48小时,血清肌酐初始升高值降低至0.3,同时排除了GFR。最近,人们正在推动采用 KDIGO 急性肾损伤分类系统,旨在将 RIFLE 和 AKIN 标准融合为 AKI 的单一统一定义。表 1 对这些系统之间的共性和差异进行了总结。在危重患者中进行的比较研究表明, 应用KDIGO可提高 AKI 的诊断率,并且在预测住院死亡率方面更具优势。
最近,生物标志物正在被与功能指标—UOP 和血清肌酐结合起来以对高危患者发生AKI的风险进行识别。细胞周期停滞的标志物,尿 [TIMP2]∙[IGFBP7] ,升高可预测心脏和非心脏手术后 AKI的发生。肾小管损伤的特异性生物标志物,中性粒细胞明胶酶相关脂质运载蛋白(NGAL)、肾损伤分子 1 (KIM-1)、α-谷胱甘肽 S-转移酶 (GST) 和 π-GST ,可在血清肌酐变化之前被检测到并预测 AKI 的进展和严重程度。NGAL 能够以现场快速检验(POCT)的方式快速检测和识别AKI。这种早期检测使及时采取干预措施治疗AKI,并采取措施防止进一步损伤成为可能。一项纳入了294例接受大手术患者的队列研究显示,应用以[TIMP2]∙[IGFBP7] 水平指导的分层肾脏保护策略可显著改善AKI患者肾功能的早期恢复并缩短ICU停留时间。其他正在进行的试验关注于寻找特定的生物标志物以期确定AKI的病因、指导目标治疗并提供有关肾脏恢复的预后信息,从而实现AKI的个体化治疗。
RRT的启动时机?
目前有多种被广泛接受的RRT启动标准。这些(标准)包括以PH<7.2或血清碳酸氢根<12mmol/L为标准的严重酸中毒、血钾>6.0mmol/L、伴脑病或心包炎等并发症的严重氮质血症和液体超负荷状态伴随以PaO2/FiO2<200为标准的呼吸功能障碍。
问题是,对于那些不伴AKI严重并发症的危重患者,应于何时开始RRT。人们假设,在发生严重并发症之前进行早期RRT的优势是恢复生理状态平衡,避免暴露于代谢性中毒并减轻液体正平衡的负面后果。提倡延迟RRT的主要原因是,如果给予适当时间的支持治疗,许多患者的肾功能可能得到恢复,从而完全避免 RRT 及其伴随风险。过去 10 年中进行的几项随机对照研究—ELAIN、AKIKI、IDEAL-ICU、STARRT-AKI、AKIKI 2,对哪些其他因素可指导这些患者开始RRT的理想时机进行了评估。表 2 总结了这些研究的关键点和和结果。
STARRT-AKI 和 AKIKI 2是(有关这个问题)的最新研究。STARRT-AKI 纳入了 来自15 个国家,168 家医院的 3019 名患者,这些患者被随机分组接受早期和延迟(启动RRT)。研究纳入符合KDIGO 2 期或 3 期 AKI 标准的患者。早期(启动RRT组)患者(开始接受RRT治疗)的中位时间为 6.1 小时,延迟(启动RRT组)患者开始接受RRT治疗的中位时间为 31.1小时。该研究的主要发现包括早期开始 RRT 没有任何优势。早期启动RRT治疗不降低患者28天和90天死亡率,两组患者在无需呼吸机、无需血管活性药物和无需ICU天数间没有差异。同样值得注意的是,延迟(启动RRT组)患者不良事件发生率较低,且超过35%的该组患者由于肾功能恢复或死亡而从未接受 RRT。
因注意到更长的RRT延迟启动时间带来更多的患者避免(RRT)治疗,AKIKI 2研究进一步延迟了RRT的启动时间。该研究纳入了来自法国 39 个 ICU 的 278 名患者。AKIKI 2研究纳入了符合KIDGO 3期的AKI患者,(纳入的患者)满足一下标准之一,即可随机接受延迟RRT或更晚期RRT:少尿或无尿超过72小时或血尿素氮(BUN)处于112和140之间。这与AKIKI试验延迟组患者开始RRT的标准相同。延迟(启动RRT)组患者开始接受RRT的中位时间为满足KDIGO 3期AKI标准后44小时,随机分组后3小时。更晚组患者开始接受RRT治疗的标准包括严重酸中毒、电解质紊乱、因水肿造成肺功能障碍或BUN>140。该组患者开始接受RRT的中位时间为满足KDIGO 3期AKI标准后94小时,随机分组后33小时。(该研究的)主要发现显示,更晚启动RRT治疗增加了患者的调整后60天死亡率。这两项研究表明,虽然早期 (启动)RRT 并不能改善结果,但更晚启动(RRT)策略可能与潜在的危害相关。 KDIGO 3 期 AKI 并不强制要求立即进行 RRT;然而,如果 48-72 小时后肾功能没有恢复,开始 RRT 可能会使患者获益。
最佳穿刺点?
一旦决定患者需要RRT,下一步就是选择最佳穿刺点。(穿刺点选择的)目标是在最大程度提高血流量的同时最大程度减少感染和导管血栓形成等并发症的发生。KDIGO指南推荐(将透析导管)优先放置于右颈内静脉,而后是股静脉,最后是左颈内静脉。留置颈静脉导管时,导管尖端最理想的位置是右心房,而放置股静脉导管时,导管尖端应位于下腔静脉。因存在静脉狭窄的风险,不鼓励选择锁骨下静脉通,这也限制了长期瘘管留置位置的潜在选择。虽然过去认为股静脉通路与增加感染风险相关,但最近的研究表明,除了病态肥胖患者之外,(各位置间)具有类似的导管感染发生率。应用无菌技术和最大化保护屏障在放置这些导管的过程中至关重要,
以是否带有Cuff(涤纶套)(是否在留置期间需要构建隧道)和最佳的持续使用时间进行区分,目前有两种不同的导管可用于RRT。启动RRT时最常用的是非隧道式、无Cuff透析导管。重症医师可以很容易的在床旁于超声引导下留置(透析导管)。这类导管被认为是临时的,并且应在出院前拔除。另一种隧道式、带Cuff透析导管通常由介入放射科或外科医师在透视引导下留置。隧道式带Cuff透析导管感染风险更低、透析效率更高、治疗中断和并发症更少。如果认为患者需要接受透析的时间超过2周,没有活动性的血流感染,并且没有明显的凝血功能障碍,则可以考虑首选放置隧道式导管。
那种(RRT)方式最好?
RRT通过超滤、对流和扩散在(患者出现)AKI的情况下维持体液平衡及进行溶质清除。超滤指移动和清除血浆中水分。对流(血液滤过)是一种依赖于水及其溶解的溶质通过半透膜拖动溶质的运动清除溶质的方式。扩散(透析)依靠血液和透析液之间的浓度梯度来清除溶质。扩散的清除率与分子大小成反比。相较于扩散,对流能更有效地清除血液中的中大型分子。
多种RRT模式均可应用于危重患者中。最常用的是间断血液透析(IHD)、连续性肾脏替代治疗(CRRT)和延长间断肾脏替代治疗(PIRRT)。腹膜透析 (PD) 也已应用于 ICU 患者,但其主要应用资源有限的中心或儿童患者中。理想的治疗方式应基于患者的血流动力学和容量状态参数、代谢紊乱情况、RRT的总体目标以及当地的专业知识和资源进行制定。
CRRT 已成为美国 ICU 的主流(RRT)模式。其主要原因是CRRT(过程中)较低的渗透压变化速率降低了危重患者血流动力学不稳定和透析中低血压发生的风险。技术进步、现代(RRT)设备的简化以及对ICU护理人员和医师的教育和整合以在重症监护病房中进行(RRT)治疗促进了对CRRT的接纳。CRRT 的一个主要缺点是需要长时间保持患者与透析管路的连接。CRRT 有多种模式,包括使应用流的连续静脉静脉血液滤过、应用扩散的连续静脉静脉血液透析 (CVVHD) 以及同时应用扩散和对流模式的连续静脉静脉血液透析滤过。表 3 对这些内容进行了详细总结。
IHD 可以更好地满足临床对快速纠正代谢异常(例如严重高钾血症和中毒)的需求。对于血流动力学不稳定的患者,可以通过增加治疗时间、增加透析液钠浓度和降低透析液温度优化 IHD 的应用。许多患者会因其临床状态在不同模式之间进行转换。 PIRRT 在两种更常用的模式之间找到了平衡。模仿 CRRT 的较低速率可减少透析中低血压,同时为患者提供一段RRT间隔时间以便进行手术、影像学检查,为患者活动的改善提供机会。
新冠危机及其造成的资源紧张怎加了腹膜透析在ICU 患者中的应用。这一经验促进了对PD在危重患者中作用的重新评估。相较其他方式,(PD的)主要优势包括失血量最少和较低的血流动力学不稳定程度。PD易于启动,透析通路可以在床旁进行留置并且不需要昂贵的设备。包括近期腹部手术、腹腔脓毒症和严重呼吸衰竭在内的相对禁忌症限制了PD在手术患者中的应用。2024 年初发表的一项荟萃分析显示,相较血液透析,PD在 AKI治疗中可能具有死亡率优势;然而,这项研究存在一些局限。表 4 对不同 RRT 模式的特点进行了比较。
已经有多项对这些不同 RRT 方式之间优劣进行评估的临床研究。目前少有证据表明某种(RRT)模式优于其他模式。对STARRT-AKI研究进行的二次分析确实证明了以CRRT作为(RRT)初始模式选择带来了更低的透析依赖和更短的ICU及住院时间,但是,这些患者更好的基线肾功能限制了这些结果的影响。相反,对AKIKI和IDEAL-ICU研究患者的汇聚分析结果显示将CRRT作为(RRT)模式初始选择与更高的60天死亡率相关,与透析依赖无关。
一旦确定那种治疗方式合适患者,就必须制定RRT剂量。对于透析而言,这是通过函数Kt/V来确定的,其中K为透析器的(尿素)清除率,t为透析治疗持续时间,V为尿素分布体积。CRRT的治疗剂量是根据体重调整的,以每公斤每小时的毫升数表示。由于CRRT中断的常见,治疗剂量可能比设定剂量少20%。多中心研究—VA/NIH ARFTN(急性肾衰竭试验网络)实验和RENAL研究结果均显示高剂量治疗并无益处。基于这些发现,KDIGO小组提出了关于RRT最佳治疗剂量的建议。每个(患者的治疗)剂量都应个体化以满足患者在电解质管理、酸碱状态、溶质清除和液体平衡方面的个体化目标。并且应在每次透析开始之前对此进行重新评估。IHD或PIRRT的推荐剂量为3.9 Kt/V每周,而CRRT的推荐治疗剂量为20-25mL/kg/h,这通常需要更高的设定剂量。药物和营养液(的用量)应基于RRT方式和治疗剂量进行调整。
外科ICU患者的特殊考虑
颅内高压
对创伤性颅脑损伤(TBI)、卒中、硬膜下血肿(SDH)、肝功能衰竭和脑水肿患者而言,液体和血钠水平的管理至关重要。对于这些患者,推荐CRRT作为RRT的选择。应用IHD会导致渗透压更大幅度的变化,从而导致峰值颅内压(ICP)升高和脑水肿的加重。CRRT可降低透析中低血压的发生风险,改善ICP的稳定性。最近一项临床研究在同时罹患终末期肾病(ESRD)和SDH患者中对不同RRT方式进行了对比,结果显示,相较CVVHD,IHD显著增加了影响神经功能的血肿进展的风险(IHD后29.7%,CVVHD后为12%)和住院死亡率或出院至医疗照护机构的风险(IHD后 35%,CVVHD后 5%)。
横纹肌溶解
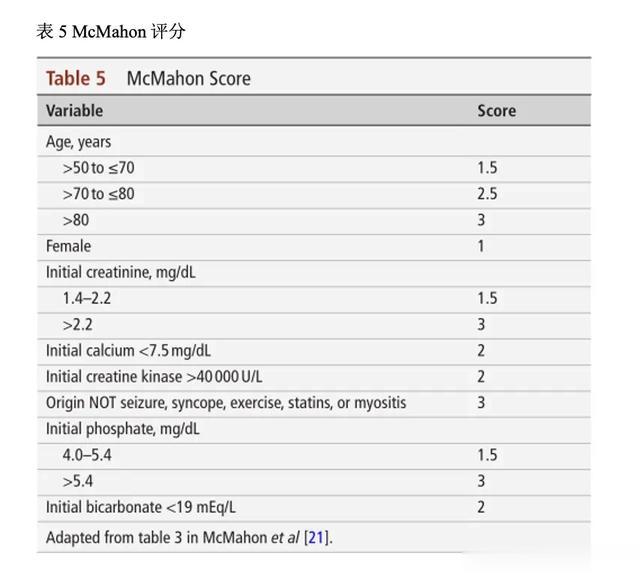
虽然横纹肌溶解在外伤性损伤后较为常见,但这些患者中只有大约10%发生AKI,5%的患者需要接受RRT。常用(诊断横纹肌溶解的)生化诊断参考标准是肌酸激酶(CK)值>5倍正常上限或>1000IU/L。建议初始应用晶体液以400毫升/小时的速度进行复苏,而后滴定至UOP1-3毫升/公斤/小时。在这些患者中,RRT没有预防AKI的作用,并且只有当患者满足RRT启动标准时才应开始RRT应用。McMahon评分(表5)使用8个变量来预测(此类患者的)RRT风险或院内死亡率。在确定哪些患者需要接受RRT时,评分≥6的敏感性为86%,特异性为68%。在该研究中,61.2%的风险评分>10的患者需要RRT或死亡
抗凝
手术和创伤后的患者相较其他ICU患者具有更高的出血风险。虽然通常可以在没有抗凝的情况下完成IHD治疗,但因为血液暴露于体外循环促进凝血,CRRT通常需要某种形式的抗凝治疗以优化治疗剂量,减少停机时间,减少并发症。如果出血风险很小,可以以部分凝血活酶时间(PTT) 1.5-2倍正常值为目标进行全身肝素应用。另一种选择是局部柠檬酸抗凝(RCA)。RCA通过螯合钙离子并在循环回路中降低<0.45mmol/L的iCa来阻止凝血瀑布的关键步骤。RCA虽然降低了出血的风险,但有较高低钙血症的风险,对于肝功能衰竭导致的柠檬酸盐代谢受损的患者应谨慎使用。抗凝选择应根据患者出血的风险、出血的后果和所需的RRT方式个体化进行。
增强CT
虽然过去关于静脉造影剂对肾功能障碍的影响存在争议,但最近的许多证据并不支持应用现代静脉造影剂进行CT扫描与AKI之间存在相关性。美国放射学会和国家肾脏基金会就肾脏疾病患者静脉注射碘化造影剂达成共识。他们指出,如果估计肾小球滤过率(eGFR)≥45,造影剂诱发AKI的风险接近0%,如果eGFR为30-44,则为0-2%,如果eGFR<30,则为0-17%。他们建议对eGFR降低的患者应用生理盐水预防造影剂诱导的AKI。最近,一项纳入14449例患者的队列研究评估了静脉应用造影剂对AKI患者的影响,结果显示静脉应用造影剂与出院时持续AKI或180天内开始RRT均无相关性。造影剂的应用在外科和创伤患者中识别出血和增强成像是必不可少的,如果需要,在AKI患者中也不应避免。
RRT的停止时机
少有指导ICU患者何时以及以何种方式停止RRT的指南推荐意见。当有肾脏恢复和急性疾病消退的迹象时,应对停止RRT进行评估。KDIGO小组建议,“当不再需要RRT时,应该停止RRT,因为患者自身的肾功能已经恢复到足以满足患者需要的程度。”在临床上,这通常采用不同的标准来表示(1) UOP>1000mL/天或应用利尿剂情况下UOP>2000mL/天,(2)血清肌酐的自发下降,(3)没有任何AKI KDIGO分期,(4)过去7天内不需要接受RRT。(这些患者中的那些)仍需要CRRT和PIRRT的ICU患者如果继续需要RRT治疗,则应转为IHD。
重点
外科和创伤患者具有较高的AKI发病率,(并发AKI)增加了(其他)并发症的发生率和死亡率。
KDIGO是AKI的首选定义和分类系统。
生物标志物[TIMP2]∙[IGFBP7]、NGAL、KIM-1和GST可以以POCT的方式用于早期诊断和指导AKI的治疗,从而改善预后。
如果不存在可接受的启动条件,早期RRT没有任何益处。
KDIGO 3期AKI并不要求立即进行RRT。但是如果在48 - 72小时后肾脏功能没有恢复,开始RRT将使患者受益。
延迟启动RRT的策略可以避免许多AKI患者接受RRT。
使用右侧颈内静脉留置血管通路。导管尖端应在右心房。
相较IHD,支持CRRT作为首选RRT模式的证据有限,即使在不稳定的患者中也是如此。
由TBI、肝功能衰竭、脑卒中、脑水肿所致的颅内高压患者可从CRRT中获益。
应用RCA进行局部抗凝是接受CRRT的外科和创伤患者的一种理想选择。
静脉应用造影剂对AKI患者是安全的。造影前后应进行充分的静脉补液。