通过吸入途径将药物递送至肺部是日常临床管理气道疾病患者的基础。与全身给药相比,吸入途径可以将药物直接靶向肺部的作用部位,从而实现更快的起效时间、减少所需药物剂量,并提高治疗疗效。
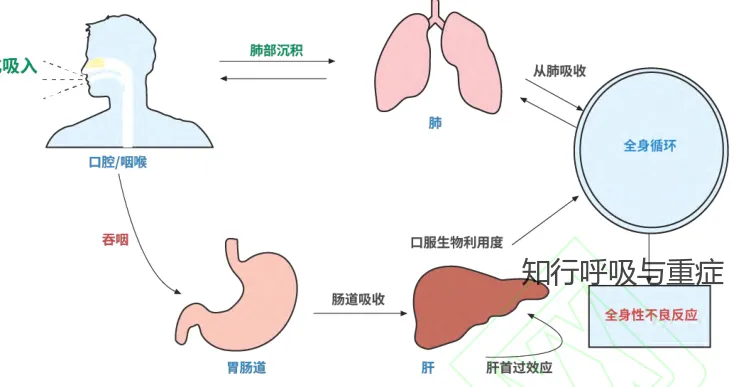
本期文章将讨论影响吸入药物在肺内运输和沉积的物理化学因素。
·一、药物在肺部沉积的机制 ·
吸入药物的沉积是一个主动过程,要求吸入的治疗颗粒尽可能被肺部气道最大程度地保留,同时减少药物在呼气时的损失。影响吸入药物气溶胶在气道内沉积的主要机制包括惯性撞击、沉降和扩散。
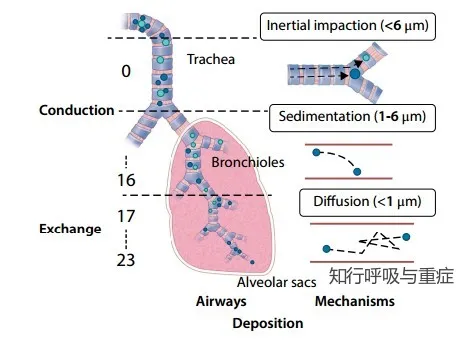
这些机制在吸入药物颗粒沿呼吸道气流轨迹运动的过程中共同作用,最终促进药物气溶胶在肺部的沉积。各机制的相对贡献及其主导作用的程度取决于药物颗粒的理化特性、局部气道的病理状态和解剖结构、气流参数,以及患者的吸入方式和呼吸模式。
· 1.1 惯性撞击·
当吸入药物颗粒被吸入时,初始的动量使其保持原始路径和气流方向,在气道内发生气流方向改变的区域撞击周围气道壁时,就会发生惯性撞击。惯性撞击主要发生在气道的分叉处,即较大气道的分支部位,这些部位的气流速度较高,气流路径和方向变化迅速。
虽然药物颗粒在肺部的撞击沉积有对整体药物沉积率正向作用,但惯性撞击也是药物沉积于口咽部的主要决定因素,口腔内的药物经吞咽后可能导致局部不良反应。
某些吸入装置(如部分加压定量吸入器(pMDIs))所喷出的气溶胶具有高初始速度,而部分干粉吸入器(DPIs)则要求患者使用较强的吸气力量,这些因素可能导致大量药物颗粒沉积在口咽部,甚至有时不到20%的药物能够进入肺部。
目前,吸入装置已逐步优化,以降低喷雾气溶胶的速度。例如,现代pMDIs采用了改良的药物制剂,如软雾剂(SMI)可释放缓慢而稳定的气溶胶,而某些DPIs设计要求患者以较温和的吸气流速进行吸入,这些改进均有助于减少口咽部的撞击沉积。在临床实践中,有时会在pMDIs上附加阀控储雾罐(VHCs)和储雾器,以延长喷雾气溶胶的行程距离,从而降低气溶胶的速度,带来双重效果。
首先,VHCs能够为气溶胶推进剂的蒸发提供时间,从而形成更小的药物颗粒,相较于较大的药物颗粒,小颗粒更容易到达下呼吸道。其次,它减少了气溶胶药物在口咽腔的撞击力。此外,软雾吸入器能够释放更缓慢、更稳定的气溶胶,其雾化持续时间更长,相较于pMDIs,其中含有更高比例的细颗粒药物。惯性撞击和重力沉降是影响1μm至10μm大且快速移动的吸入药物颗粒沉积的主要机制。

· 1.2 重力沉降·
药物颗粒在肺部的沉降发生于重力作用下,当重力作用力超过空气阻力时,药物颗粒会沉积在气道内。沉降通常发生在气流速度较低的区域,此时,吸入药物颗粒有足够的停留时间在气道壁上沉积。沉降作用在分支较多的小气道中最为显著,因为在这些区域内,药物颗粒到达气道壁的距离较短。在吸入药物后给予患者屏气指令可以延长药物颗粒在气道内的停留时间,从而增强沉降作用,提高药物沉积率。
· 1.3 扩散·
扩散是气道内空气分子与极小药物颗粒(通常小于1μm)之间的随机碰撞作用,从而推动药物颗粒在气道内进行不规则、无序的运动。受扩散作用影响,即使在无气流或无重力的情况下,药物颗粒仍会在气道内随机移动,从而增加与气道壁接触并沉积的概率。扩散主要发生在远端小气道和肺泡区,这些区域气流速度最低,颗粒在气道内停留时间最长,且颗粒与气道壁之间的距离最短。扩散是决定小于1μm缓慢移动的微粒沉积的主要机制。

· 二、影响沉积的因素 ·
许多因素可影响吸入气溶胶药物颗粒在气道内的沉积,通常可分为气溶胶特性和患者因素。

· 2.1 气溶胶的特性·
在理化特性方面,药物颗粒的大小是决定药物沉积总量及其在气道不同区域分布的最重要因素。呼吸道的分支系统主要作为一种防御机制,类似于一系列过滤器,依次从吸入气流中去除有害颗粒。因此,吸入药物颗粒需要克服这些障碍,以实现有效沉积。
a)通常情况下直径大于100μm的吸入颗粒通常被鼻腔截留,
b)直径大于10μm的颗粒主要沉积于口咽部
c)2-6μm的颗粒沉积于传导气道,
d)超细颗粒(小于2.1μm)最有可能到达小气道和肺远端区域。
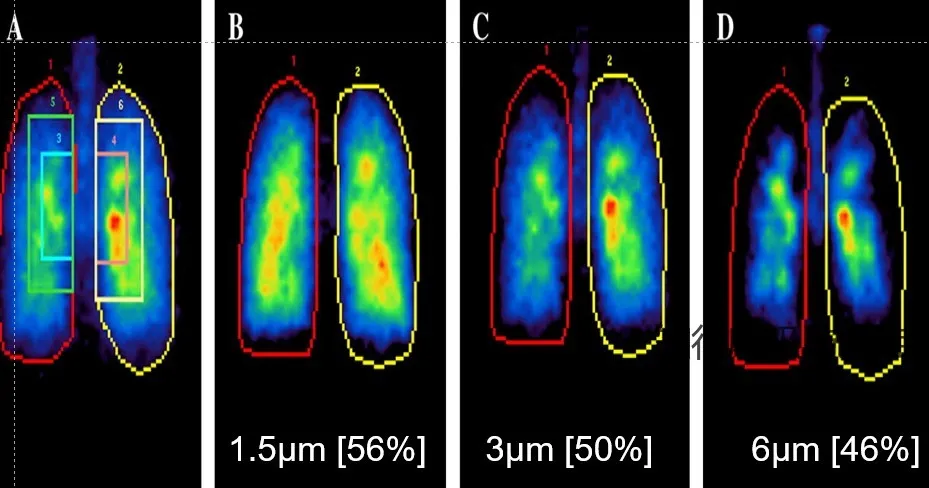
整体而言,较小粒径的药物在肺部的沉积量高于较大粒径的药物,因此通过调节药物颗粒的大小,可以优化肺部药物递送,从而提高患者的临床获益。
在呼气方面,小颗粒药物是否易于被呼出也是一个关注点。体外模拟研究发现,小粒径气溶胶可能被呼出,其比例可高达70%,但这些研究的实验模式和呼吸条件未能真实模拟人体肺部环境,且所使用的颗粒并非治疗性气溶胶。随后,体内研究发现,小粒径的治疗性药物颗粒被呼出的比例仅为4–6%,与大颗粒药物的呼出率(1–3%)相当。
目前已采用多种方法优化药物的理化特性,以提高吸入药物的沉积率,包括改变粒子形态、利用静电荷、使用低密度气体(如氦气)、以及低密度大孔颗粒以改变气溶胶特性。此外,气溶胶粒径在递送过程中可能发生变化。例如,挥发性气溶胶在输送系统和呼吸道内运动时可能因蒸发而变小。即使在100%湿度条件下,由于表面张力引起的小液滴内部压力升高,纯水液滴仍会迅速蒸发:1微米水滴在室温下约0.5秒内完全蒸发,10um水滴在约1分钟内蒸发。
然而,药物的最佳沉积区域还取决于药物类别、药理作用以及靶向受体在气道中的分布。
· 2.2 患者因素·
每位个体的呼吸方式都会影响药物在气道内的沉积。呼吸频率、潮气量和肺容量会影响气溶胶在肺内的停留时间,从而影响其在重力沉降和扩散作用下的沉积率。肺容量的变化还会改变气道和肺实质的大小尺寸。
实验结果表明,呼吸模式对气溶胶沉积分布的影响包括:a) 总沉积量随着呼吸频率的增加而减少;b) 缓慢而深的呼吸会使气溶胶均匀分布于肺内,但大气道内的气溶胶沉积较少;c) 快速而浅的通气会增强大气道的气溶胶沉积,并导致沉积分布的不均匀性;
d) 在高呼气末肺容积(EELV)下缓慢而浅的呼吸可增强小气道的沉积
1.吸气方式:在临床中,影响吸入气溶胶在肺内沉积的最重要患者变量是吸气方式,其影响着吸入药物颗粒的沉积效率和治疗效果。
对于定量气雾剂(pMDI)和软雾吸入器(SMI),最佳的吸气方式是在 5 秒内缓慢而平稳地吸入,患者应以“缓慢、平稳、自然、深沉、舒适”的方式吸气。
在使用吸入装置前,患者应抬起下巴以打开气道,同时呼气至潮气末功能残气量(FRC),以确保有足够的吸入气量将药物颗粒带入吸气气流。更大的吸入气量有助于更多气溶胶颗粒有效沉积在肺内,并向外周气道输送。
与 pMDI 不同,干粉吸入器(DPI)依赖患者的吸气流速来启动,需要更快、更强的吸气流速才能产生足够的峰值吸气流量(PIF),从而最佳地分离药物粉末与其载体分子,并有效地将粉末气溶胶化为可吸入的颗粒,以实现足够的肺部沉积。DPI 的内部阻力因不同设计而异,因此克服此阻力所需的流速也有所不同。
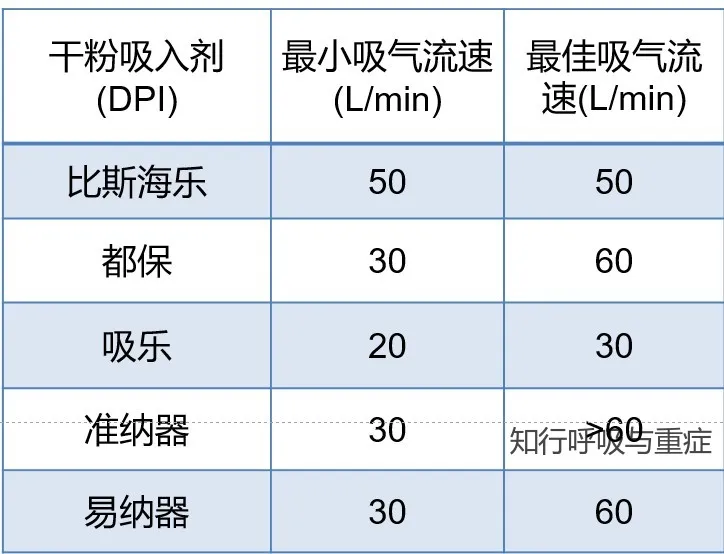
2.吸气峰值流速:相关研究表明因慢性阻塞性肺疾病(COPD)急性加重住院的患者中,32-47%在出院前表现出PIF低于60L/min;在稳定期COPD患者中,19-78%也表现出PIF减弱。这些发现表明,许多患者无法产生足够的吸气力来克服其处方DPI的阻力。
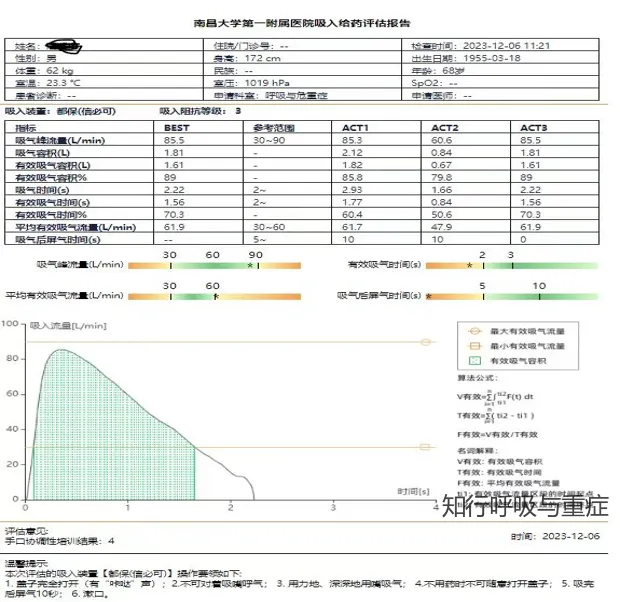
3.屏气时间:在吸气结束时的屏息暂停有助于吸入药物在肺内的沉积,使气溶胶颗粒在气道内停留足够的时间,通过重力沉降和扩散机制接触气道壁。
4.肺部和气道的解剖结构:对于沉积效率至关重要,因为沉积的有效性部分取决于气道的直径、分支角度以及到肺泡壁的平均距离。此外,除了吸气流速外,气道解剖结构还决定了局部气流速度,以及气流是层流还是湍流。
5.呼吸系统疾病:显著影响吸入颗粒的分布。支气管收缩会导致气流转移至未受阻的气道。随着疾病的进展,残存的健康气道可能会越来越多地暴露于吸入颗粒。炎症或黏液导致的气道狭窄可能会增加气流的线速度,增强惯性沉积,并导致更集中的中央沉积模式。在病情极其严重的患者中,流速受限与气溶胶沉积的增加相关。
· 总结 ·
肺部吸入给药作为全身性治疗药物的递送途径正受到越来越多的关注。肺部,特别是肺泡区域,具有广阔的表面积和丰富的血管供应,使吸入药物能够高效吸收。此外,一些无法经胃肠道吸收或易被肝脏代谢降解的大分子肽类和蛋白质药物,也可能通过吸入途径实现全身作用。相比注射治疗,吸入给药方式不仅可降低药物的不良反应,还能避免针剂使用的不便,具有明显的临床优势。
但是越来越多的研究表明,医护人员因为自身对吸入装置的知识和培训不足导致对患者进行吸入装置的操作教育存在不足。因此,患者要么接受了错误指导,要么根本没有接受指导,而吸入技术的错误已进一步导致疾病控制不佳、急性加重的增加,并增加医疗经济负担。
总的来说,特别需要在门诊和住院期间向患者演示吸入装置的正确使用方法是管理呼吸系统疾病患者的关键部分,并可改善疾病结局。此外,研究表明,随着时间的推移,正确的吸入技术会下降,因此应在每次就诊时检查患者的吸入技术。
· 参考文献 ·
[1]Lavorini F, Buttini F, Usmani OS. 100 years of drug delivery to the lungs.
Handb Exp Pharmacol 2019;260:143–159.
[2]Lavorini F, Fontana GA, Usmani OS. New inhaler devices - the good, the
bad and the ugly. Respiration 2014;88(1):3–15. DOI:10.1159/000363390
[3]Capstick, T. G., & Clifton, I. J. (2012). Inhaler technique and training in people with chronic obstructive pulmonary disease and asthma. Expert review of respiratory medicine, 6(1), 91–103. https://doi.org/10.1586/ers.11.89
[4]Mitchell JP, Berlinski A, Canisius S, et al. Urgent appeal from International Society for Aerosols in Medicine (ISAM) during COVID-19: Clinical
decision makers and governmental agencies should consider the inhaledroute of administration: A statement from the ISAM Regulatory and
Standardization Issues Networking Group. J Aerosol Med Pulm DrugDeliv 2020;33(4):235–238.
[5]Darquenne C. Deposition mechanisms. J Aerosol Med Pulm Drug Deliv2020;33(4):181–185.
[6]Verbanck S, Kalsi HS, Biddiscombe MF, et al. Inspiratory and expiratory aerosol deposition in the upper airway. Inhal Toxicol 2011;23(2):104–111.
