凌晨三点,55岁的魏女士被一阵钻心的腰痛惊醒,她以为只是普通的肌肉劳损。但短短两个月后,一次轻微的弯腰动作后腰部竟然无法动弹——这场看似意外的腰痛危机,最终被诊断为乳腺癌骨转移。
像魏女士这样的患者并非个例:5%的乳腺癌患者在初次就诊时即可出现骨转移,75%患者也可能会在未来10年中面临发生骨转移的风险[1],骨骼甚至成为乳腺癌复发转移的第一站。为什么癌细胞总对骨骼“情有独钟”?那些被忽视的夜间骨痛、不明骨折,是否在敲响转移警钟?

魏女士于2021年8月确诊为浸润性导管癌,早在1年前她便发现了左乳有一个包块,却因不痛不痒将其判定为“乳腺增生”。正是这份误判,让隐匿的癌细胞悄然完成骨转移,魏女士及家人深感后悔,因为早期的忽视,错过了最佳治疗时机。
乳腺癌为什么容易发生骨转移?
肿瘤细胞局部侵袭以逃离原发肿瘤周围组织,然后侵入血液或淋巴管,在循环系统中存活,随后从循环系统逃逸、外渗,最终形成转移灶。值得注意的是,乳腺癌骨转移灶内高钙、低pH值及低氧的微环境有利于肿瘤细胞定植,进而促进骨转移的形成与发展。
这也提醒我们:乳腺癌患者一定要提前保护骨骼,并且密切关注骨骼的异常情况。
骨转移的“信号”,千万要读懂
* 骨痛
这是最常见的症状,可能表现为间歇性或持续性疼痛,夜间或活动时加重。
* 病理性骨折
由于肿瘤对骨骼的破坏,骨骼变得脆弱,容易在日常活动中发生骨折。
* 局部肿胀和关节僵硬
骨转移可能导致局部肿胀和关节活动受限。
* 神经压迫症状
如麻木、疼痛、无力,甚至截瘫。
* 高钙血症
骨转移破坏骨骼,释放大量钙质进入血液,可能引发高钙血症。

01、病情概述
魏女士于2021年8月26日至2022年3月完成了8周期化疗,肿瘤从化疗前的19×12×13mm缩小至5×3×4mm。2022年4月14日,她接受了根治性手术治疗。术后分期为cT4bN2M1 IV期,病理显示:浸润性乳腺癌,手术切缘阴性,淋巴血管侵犯(LVI),有乳头受累,无皮肤受累,左腋窝淋巴结(6/6)枚查见癌转移,余脂肪组织内见癌浸润。左锁骨下淋巴结及尾叶结节为纤维脂肪组织查见癌浸润。免疫组化结果显示:ER(强+,>90%)、PR(强+,70%)、HER2(2+)、CK5/6(-)、Ki-67(+,20%)。
术后,魏女士接受了25次放疗和8周期化疗,并随后给予来曲唑及阿贝西利治疗。
尽管魏女士初诊时为IV期,但通过化疗获得了手术机会。然而,术后病理显示存在淋巴结的广泛转移、脉管癌栓等危险因素。2023年5月10日的骨显像显示:胸腰部分椎体骨代谢增高灶,考虑肿瘤转移可能,这可能对预后产生不利影响。面对这样的困境,难道只能坐以待毙等待肿瘤复发吗?
魏女士和家人一直在寻求新的治疗方法,希望能长期控制肿瘤。他们了解到清华大学医学院张明徽教授的vNKT细胞治疗技术,或许能成为她治疗的新希望。
乳腺癌骨转移:系统治疗是关键
在魏女士这类IV期乳腺癌骨转移患者中,狡猾的肿瘤细胞早已突破局部防线,侵入骨骼与淋巴系统。如果,仅靠局部放疗或骨科手术只能暂时解决局部问题,残余的肿瘤细胞还会卷土重来。
而vNKT细胞治疗正展现出“全域追缉”的战略优势——vNKT细胞治疗能通过血液到达全身,杀伤逃逸的肿瘤细胞,同时通过清除抑制性免疫细胞MDSCs,起到改善肿瘤免疫抑制性微环境的作用,打破“转移-骨破坏-促转移”的恶性循,建立正常免疫系统,从而进一步预防乳腺癌的复发转移。
# vNKT细胞免疫治疗
NKT细胞 (Natural killer T cell),是一种细胞表面既有T细胞受体TCR,又有NK细胞受体的特殊T细胞亚群,它兼具NK细胞和T细胞的重要特征,具有非特异性和特异性识别肿瘤细胞的双重能力,可以非常快速地杀伤肿瘤细胞。在NKT细胞亚群中,有一种个头更大、杀伤能力更强的特种兵,就是清华大学张明徽教授的实验团队发现的vNKT(Variant Natural Killer T)细胞。
这群vNKT细胞在体内的数量非常少,且不会轻易被激活。但是一旦被活化,却能以一当百,杀灭那些可能残存在体内无法被发现的肿瘤细胞。另外,研究还发现vNKT细胞具有双重抗肿瘤效应,不仅能够直接杀伤癌细胞,还会调节肿瘤组织内部的免疫微环境,杀伤抑制性免疫细胞MDSCs,打破肿瘤的免疫逃逸,重建正常免疫系统,进一步预防复发转移。
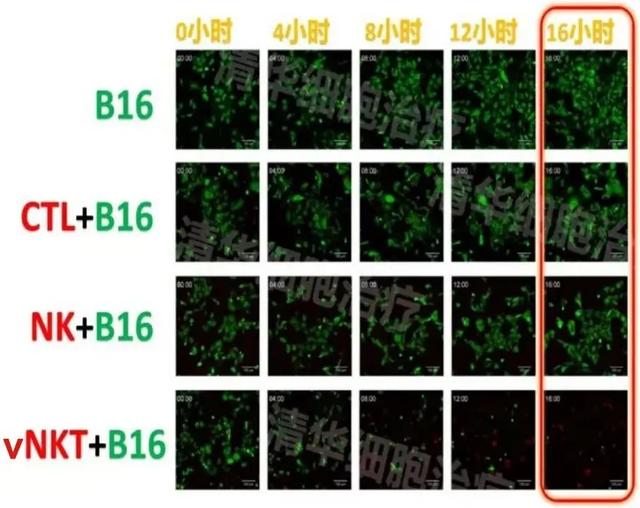
实验条件:有vNKT细胞存在的情况下,经过16个小时,近乎所有B16肿瘤细胞被杀死!
魏女士于2023年7月5日开始接受vNKT细胞治疗,治疗方案为1疗程/月,截至2024年7月5日,她已顺利完成12疗程。
目前随访显示病情稳定,未出现复发转移,魏女士精神状态良好,食欲和睡眠俱佳,生活质量显著提升。影像学检查的结果也逐步显示出积极的变化,从最初的骨转移灶代谢增高,到后来的密度变淡,直至最新的扫描结果显示,虽然仍存在部分代谢增高灶,但整体骨代谢水平未见明显恶化,这无疑是对治疗效果的最佳注解。
02、影像学改变

骨扫描:
2021年8月19日:右侧第6肋腋段、T9椎体代谢增高灶,考虑肿瘤骨转移;T10-T12椎体骨代谢增高灶,骨转移不除外。
2022年1月12日:T9-T12椎体见点状、片状放射性浓聚增高影。
2023年5月10日:胸腰部分椎体骨代谢增高灶,肿瘤转移可能,对比2022年1月12日骨显像,T9椎体骨代谢程度稍增加。2023年10月30日:T9椎体代谢增高灶,密度变淡。
2024年7月26日:部分胸腰骶椎、右侧肩胛骨下方骨代谢增高灶,考虑肿瘤骨转移治疗后改变,较前骨代谢水平未见明显改变;右侧第6后肋近腋段骨代谢增高灶,倾向治疗后改变。

胸部CT:
2020年12月24日、2022年8月13日及2022年4月11日的影像学检查均显示左乳外上象限10点实性肿块。
2023年10月及2024年7月复查肺CT提示左乳腺术后改变,术区未见复发征象。
04、结论与点评
乳腺癌骨转移≠无药可救
根据美国癌症协会(American Cancer Society,ACS)的统计数据,乳腺癌患者的5年生存率为91%,10年生存率为84%[2]。然而,具有骨转移的乳腺癌患者生存期明显缩短,仅存在骨转移的乳腺癌患者3年生存率为50.5%,中位生存期为36个月[3]。
魏女士通过vNKT细胞治疗,至今已平稳度过3年,达到了理想的治疗效果,她的故事是对所有乳腺癌患者的一针强心剂。在这个过程中,vNKT细胞免疫治疗在降低复发转移的风险中发挥了不可替代的作用,为患者获得肿瘤长期稳定甚至治愈提供了可能性。
尽管骨转移表明乳腺癌已进入晚期阶段,但它并不等同于生命的终结。与肺、脑、肝等其他部位的转移相比,骨转移的预后是相对较好的。事实上,有人即便带着骨转移的病灶,也依然能够开启新的人生旅程,关键在于保持警惕、及时寻求医疗帮助并接受科学治疗。
评论区可以交流骨转移的症状,治疗心得,抗癌路上我们一起携手前进。
参考文献:
[1] Anwar SL, Avanti WS, Dwianingsih EK, et al. Risk factors, patterns, and distribution of bone metastases and skeletal-related events in high-risk breast cancer patients[J]. Asian Pac J Cancer Prev, 2022, 23(12): 4109-4117.
[2] DeSantis CE, Ma J, Gaudet MM, et al. Breast cancer statistics, 2019[J]. CA Cancer J Clin, 2019, 69: 438-451.
[3] Wang R, Zhu Y, Liu X, et al. The clinicopathological features and survival outcomes of patients with different metastatic sites in stage IV breast cancer[J]. BMC Cancer, 2019, 19: 1091.

张明徽:乐和新医创始人
清华大学医学院免疫学博士,2002年发现vNKT细胞至今,张明徽教授带领的研究团队走过了20余年的研究历程,积累了700余例实体肿瘤的治疗经验,涉及几乎所有常见实体肿瘤,研究结果充分证明vNKT在实体肿瘤治疗中具有巨大价值。

适用于病理恶性程度较高或存在复发风险的术后患者;经化疗、放疗、靶向治疗等常规治疗肿瘤已基本控制但仍未达到治愈的患者;持续存在较高致癌因素的患者;放疗、化疗不耐受的患者。这些患者如果在传统抗肿瘤治疗后没有进行有效的后续治疗,复发、转移或再发肿瘤将是大概率事件,在这种情况vNKT细胞治疗是理想的后续治疗手段,可显著改善患者的预后。
