
背景
卵巢癌是最致命的妇科癌症,全世界每年有超过20万人死于该疾病。卵巢癌的高死亡率很大程度上是因为在诊断时,卵巢癌细胞已经转移到腹膜,这意味着治愈它的可能性很小。事实上,晚期上皮性卵巢癌的5年总生存率很低,约为30%至50%。我们对上皮性卵巢癌生物学的理解有了显著的提高,这导致了新的靶向治疗和后续治疗[1]。
BRCA1/2基因突变
[2]BRCA1/2是重要的抑癌基因,对于维持细胞正常的生长增殖至关重要,也是维持细胞HRR功能最重要的基因。携带BRCA1/2突变的多种肿瘤对PARP抑制剂敏感,在SOLO-1研究中,携带胚系或体细胞BRCA1/2突变的晚期上皮性卵巢癌患者在初始治疗缓解后应用奥拉帕利维持治疗,相比安慰剂,患者复发或死亡风险下降70%,中位PFS延长3年以上[3]。BRCA1/2胚系突变还与肿瘤的遗传易感性相关[3]。
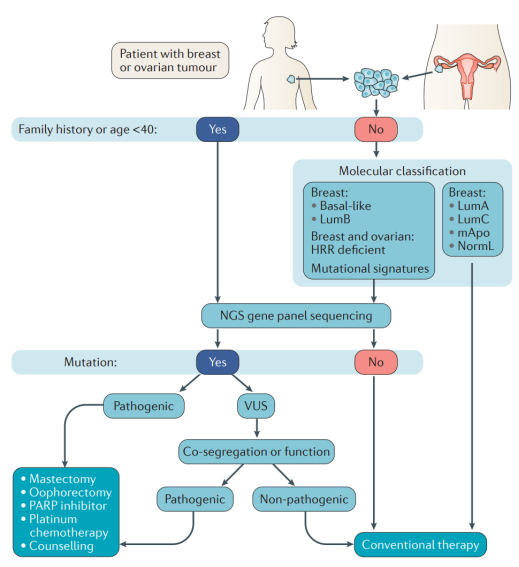
▲乳腺和卵巢肿瘤的临床管理建议
文献报道-现实世界中胚系与体系之间的一致性BRCA1/2在上皮性卵巢癌中的地位[5]。
在2021年4月11日至2023年10月11日期间,来自412名患者的442份肿瘤样本使用Myriad的myChoice®CDx进行了测试。肿瘤细胞含量从5%到80%(61/442[13.8%]份样本未提供肿瘤细胞含量)。肿瘤BRCA1/2检测失败率为10.2%(45/442例肿瘤)。未通过肿瘤检测的样品中肿瘤细胞含量为5%至65%(10/45样品中未提供肿瘤细胞含量)。对29例患者的2个或2个以上肿瘤样本进行了检测,检测失败(肿瘤BRCA1/2和GIS检测);23/29例患者)或因为患者被错误地检测了两次(6/29例患者)。肿瘤BRCA1/2检测在382例患者中成功。其中,15名患者(3.9%)未进行胚系BRCA1/2检测。
研究组包括367例成功接受肿瘤和胚系BRCA1/2检测的患者(表1)。其中,大多数患者被诊断为晚期、高级别、非粘液上皮性卵巢癌。

所有在肿瘤DNA中检测到BRCA1/2致病变异的患者都进行了胚系BRCA1/2检测。在36种胚系BRCA1/2致病变异中,在肿瘤DNA中检测到33种。胚系BRCA1/2致病变异在胚系和肿瘤DNA中的一致性为91.7%(33/36)(表3)。所有小片段测序BRCA1/2致病变异均在胚系和肿瘤DNA中检测到。三种生殖系肿瘤DNA中未检测到的BRCA1/2致病变异均为大片段重排,包括2个BRCA1外显子13重复(n = 2)和1个BRCA2外显子1-24缺失(n = 1;表4)。


结论与讨论
结论:我们报告了在一个被诊断为上皮性卵巢癌的现实世界的大队列患者中,胚系和肿瘤BRCA1/2致病变异之间的一致性。如果Myriad myChoice®CDx用于肿瘤HRD检测,我们的数据支持在所有年龄< 79岁的上皮性卵巢癌诊断患者中进行胚系和肿瘤BRCA1/2检测的测试模型,只有年龄≥80岁的肿瘤BRCA1/2致病变异患者才需要进行胚系BRCA1/2检测。
讨论:本研究的主要局限性是样本量适中和单中心状态。我们也承认,近4%(15/382)的研究组没有进行胚系BRCA1/2检测。对这些患者临床记录的回顾显示,几乎所有拒绝做胚系检测的患者或者临床上有预后不良的因素的患者在做胚系检测前已死亡。我们还认识到,研究组中有少数(12/367)未被诊断为高级别卵巢癌,因此不适合进行肿瘤HRD检测。
同样值得注意的是,没有肿瘤BRCA1/2检测被证实可以区分胚系和体细胞致病变异,因此,所有患有肿瘤BRCA1/2致病变异的患者,无论使用何种肿瘤检测,都应进行胚系检测。
BRCA1/2基因突变检测
飞朔生物推出的BRCA1/2基因检测,基于飞朔专利的RingCap®技术检测BRAC1/BRCA2基因编码区域的突变情况,检测结果准确可靠。自接收样本开始仅需5个工作日即可出具检测报告,无需长时间等待。通过该项检测,临床医生可以综合评估患者基因状态,优化患者管理,针对患者制定个性化治疗方案。
检测意义
1.通过检测先证者或高危人群是否携带BRCA1/2基因胚系突变,为遗传性肿瘤诊断和后续的诊疗提供依据;
2.评估BRCA1/2突变恶性肿瘤患者对奥拉帕利等PARP抑制剂的敏感度。
检测优势
1.操作简单:自主研发专利RingCap®技术,文库构建仅需两步,3.5小时即可完成。
2.灵敏度高:可检出10 ng DNA样品中含量低至5%的基因突变。
3.检测全面:由于BRCA1/2基因不存在高频率的突变热点,对编码区和相邻边界区进行测序,可以保证检测的全面性。
4.严谨专业:全面、严格的质控标准,自动化分析+专业团队双重复核,真正做到全面精准解读。
参考文献
[1]基于下一代测序技术的BRCA1/2基因检测指南(2019版)
[2]上皮性卵巢癌PARP抑制剂相关生物标志物 检测的中国专家共识
[3]N Engl J Med, 379, 26(2018): 2495-250
[4]Nat Rev Cancer. 2016 Sep; 16(9): 599-612.
[5]Cancers 2024, 16, 177. https:// doi.org/10.3390/cancers16010177
声明:本文仅用于分享,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!
