帕金森病是一种困扰全球数百万人的神经退行性疾病,患者大脑中负责产生多巴胺的神经元逐渐死亡,导致震颤、僵硬、运动迟缓等症状。尽管现有药物可以缓解症状,但无法阻止疾病进展。
近年来,干细胞技术的飞速发展为帕金森病的治疗带来了全新可能。近期,《自然》杂志同期发表的两项早期临床试验结果,标志着这一领域迈出了从理论走向实践的关键一步。

图1 美国研究试验论文首页截图

图2 日本研究试验论文首页截图
干细胞治疗的原理与历史探索
此次两项研究分别采用了两种明星干细胞:美国团队使用人胚胎干细胞衍生的多巴胺能神经祖细胞移植,日本团队选择了诱导性多能干细胞(iPSC)。前者源自早期胚胎,具有强大的分化潜力;后者通过将成人皮肤细胞等体细胞“重编程”获得,既能避免伦理争议,又能实现患者特异性治疗。两者都在试验中被成功诱导为多巴胺能神经祖细胞,这些细胞移植到大脑后,有望成熟为功能神经元,重建受损的神经环路。
安全性的坚实证明
任何新型疗法的临床应用,安全性永远是第一道门槛。两项试验共纳入19例中晚期帕金森病受试者(美国受试者12例,日本受试者7例),分别将不同剂量的干细胞产物移植到大脑壳核(多巴胺信号的关键中转站)。令人振奋的是,在观察期内,两项试验均没有出现与移植直接相关的严重不良事件。美国试验中仅报告1例术后短暂癫痫发作;日本试验中所有不良事件均为轻度,最严重的仅是中度运动障碍。更关键的是,影像学监测均未发现肿瘤形成或异常组织增生,这直接回应了人们对干细胞可能失控生长的最大担忧。
免疫排斥是异体细胞移植的另一大挑战。为此,这两项试验均采用短期免疫抑制方案,成功避免了严重排斥反应。值得注意的是,日本研究团队使用的iPSC源自与受试者免疫特征匹配的供体库,这种“现成型”策略既保留了个性化治疗的优点,又大幅降低了成本和时间门槛。这些数据共同证明,经过严格质量控制的干细胞产品在大脑环境中具有可靠的生物相容性。
此外,这两项试验均实现了零死亡,所有受试者均未出现危及生命的严重不良事件。试验过程中观察到的不良事件均在可控范围内,进一步验证了该治疗策略的安全性。
疗效信号的初现曙光
虽然早期试验主要评估安全性,但受试者临床表现的变化同样引人注目。统一帕金森病评定量表(MDS-UPDRS)显示,在两项试验中,大多数受试者在停用抗帕金森药物 24 h后,运动症状显著改善。
美国临床试验数据显示,多巴胺能神经祖细胞移植18个月时,低剂量组MDS-UPDRS评分平均降低8.6分,高剂量组MDS-UPDRS评分平均降低23分;日本临床试验数据显示,接受iPSC移植24个月时,受试者MDS-UPDRS评分平均下降9.5分。
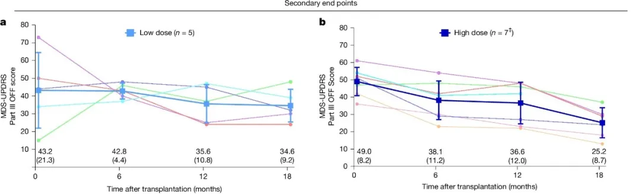
图3 美国试验的低剂量组和高剂量组受试者在移植后不同时间的MDS-UPDRS评分变化情况。X轴表示移植后的时间(月),Y轴表示MDS-UPDRS评分(0-80)。每条线代表一个患者的评分变化,蓝色方块表示低剂量组的平均评分,深蓝色方块表示高剂量组的平均评分。垂直的误差线表示数据的变异程度或标准差。

图4 日本试验受试者24个月内相对于基线的MDS-UPDRS评分变化。X轴同样代表时间(月),Y轴代表相对于基线的评分变化(-20到10)。每条彩色线代表一个患者的评分变化,黑色线表示所有患者的平均评分变化,虚线代表基线(0分)。
但这些改善并非立竿见影,细胞移植后需要数月时间逐渐成熟并建立神经连接,这与其他动物实验观察到的时程一致。同时,疗效呈现剂量依赖性。美国试验中高剂量组与低剂量组的MDS-UPDRS平均评分差距过大,这提示未来研究需要进一步优化细胞剂量和递送策略。尽管样本量有限,这些数据为干细胞替代丢失神经元的功能可行性提供了首个临床证据。
此外,两项研究的巧妙设计体现了转化医学的智慧。美国团队选择壳核作为移植靶点,而非多巴胺神经元原生的黑质区。这是因为帕金森病中黑质到壳核的神经通路断裂,直接将新细胞植入“信号接收端”更能规避复杂的神经环路重建。
日本团队则开创性地建立iPSC供体库,通过筛选常见免疫特征,使同一批细胞可匹配约40%人群。这种平衡个性化与标准化的思路,对降低治疗成本至关重要。
医学新纪元的黎明
尽管结果振奋人心,但我们仍需保持谨慎的态度。现有数据仅能证明短期安全性,需要更长期随访评估细胞的持久性和潜在晚期风险。如今,美国团队已启动Ⅱ期双盲对照试验,日本团队也计划扩大研究规模,这些研究将为疗效判定提供更可靠证据。
回溯历史,人类对抗帕金森病的武器从左旋多巴类药物到深部脑刺激,再到今天的干细胞疗法,每一步突破都凝聚着无数科学家的智慧。这两项研究犹如黑暗中的曙光,不仅为帕金森病患者带来希望,更为阿尔茨海默病、亨廷顿病等神经退行性疾病的干细胞治疗铺平道路。在这个时代,受损的神经回路或许不再意味着永久性的功能丧失,而是可以通过“细胞重编程”技术,使受损的神经回路得以重建,从而获得新生。
参考文献
[1] Tabar V,Sarva H,et al.Phase I trial of hES cell-derived dopaminergic neurons for Parkinson’s disease.Nature(2025).
[2] Sawamoto N,Doi D,Nakanishi E,et al.Phase I/II trial of iPS-cell-derived dopaminergic cells for Parkinson’s disease.Nature (2025).
