一,利特昔替尼简介及上市历程
利特昔替尼是一种口服的双重激酶抑制剂,主要靶向JAK3(Janus激酶3)和TEC激酶家族(如BTK)。其作用机制是通过阻断炎症信号通路关键蛋白的活性,抑制自身免疫反应,从而治疗与免疫系统过度激活相关的疾病。
适应症:
斑秃:为主要获批适应症,适用于12岁及以上中度至重度斑秃患者。
其他潜在适应症:包括类风湿性关节炎、溃疡性结肠炎和克罗恩病(处于临床试验阶段)。
特点:
高选择性:相较于广谱JAK抑制剂(如巴瑞替尼),利特昔替尼对JAK3和TEC激酶的抑制更具特异性,可能减少全身性副作用。
疗效显著:临床试验显示,约40%-50%的重度斑秃患者在治疗6个月后实现80%以上的头皮毛发覆盖。
上市历程
1. 研发背景
原研公司:由辉瑞主导研发,其最初基于对JAK/TEC通路在自身免疫性疾病中作用的研究。
收购整合:辉瑞通过收购生物技术公司整合相关专利,加速该药的开发进程。
2. 关键临床试验
ALLEGRO 2b/3期试验(2022年):
纳入718例严重斑秃患者,结果显示,每日口服50mg利特昔替尼组的患者中,23%在24周后达到SALT≤20分(即头皮覆盖率≥80%),显著优于安慰剂组(1.6%)。
安全性:常见不良反应包括头痛、上呼吸道感染,严重副作用(如血栓、心血管事件)发生率较低。
青少年扩展试验(2023年):确认在12-17岁患者中的安全性和有效性,支持扩大适应症。
3. 全球审批与上市
FDA批准(2023年6月):获美国FDA优先审评资格,基于突破性疗法认定,成为首个获批用于青少年斑秃的JAK抑制剂。
欧盟EMA批准(2024年1月):通过加速审批程序,要求上市后继续监测长期安全性数据。
日本PMDA批准(2024年3月):同步纳入医保,定价为每月约3000美元。
中国NMPA状态:2023年9月提交上市申请,目前处于审评阶段,预计2024年底获批。
二,利替昔替尼的临床试验数据
利特昔替尼是一款每日1次的口服特异性JAK3/TEC抑制剂,对表达于TEC激酶家族中的酪氨酸激酶成员和Janus激酶3(JAK3)具有高选择性,可阻断导致斑秃的信号分子和免疫细胞活性,从而抑制免疫系统杀伤毛囊细胞以达到治疗斑秃的目的。与第一代泛JAK抑制剂相比,利特昔替尼在降低毒性方面更有优势。
本次获批上市是基于一项随机、双盲、安慰剂对照的IIb/III期ALLEGRO研究。该研究旨在评估利特昔替尼治疗12岁及以上斑秃患者(n=718)的疗效和安全性。入组患者至少有50%的头发因斑秃而脱落,包括全秃(头发全部脱落)和普秃(全身毛发均脱落)患者,并且已持续6个月至10年的斑秃发作。患者随机接受每日1次利特昔替尼 30mg或50mg(接受或不接受1个月的初始治疗:每日1次利特昔替尼 200mg)、利特昔替尼 10mg或安慰剂治疗)
主要终点为第24周时绝对SALT评分≤20,接受利特昔替尼治疗后头皮毛发再生患者比例。SALT是一种测量头皮脱发量工具,评分越高,脱发越严重。结果显示,每日服用30mg或50mg 利特昔替尼 24周后,实现头皮毛发覆盖率≥80%的患者比例显著高于安慰剂组,达到了主要疗效终点。
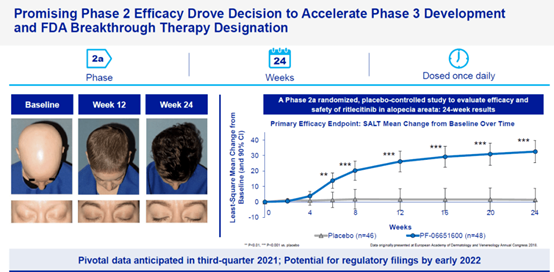
此外,利特昔替尼在成人和青少年患者中耐受性和安全性良好。最常见的不良事件为头痛、鼻咽炎和上呼吸道感染。
另外一项正在进行的开放标签的、长期的III期ALLEGRO-LT研究,旨在评估利特昔替尼在脱发率为25%或以上的成人斑秃患者和脱发率为50%或以上的12岁青少年斑秃患者中的安全性和有效性。
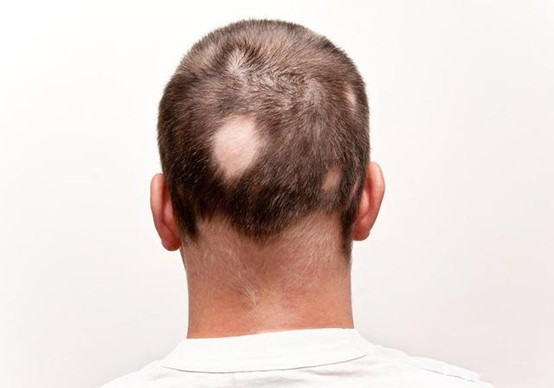
斑秃是一种以斑块状脱发为特征的自身免疫性疾病。这种脱发通常发生在头皮上,但也会影响眉毛、睫毛、面部毛发和身体的其他部位。斑秃患者的症状由免疫细胞攻击健康毛囊引起,导致头发脱落。斑秃平均发病年龄在25至35岁之间,但也可影响老年人、儿童和青少年,无明显性别差异。斑秃严重影响患者健康和生活质量,可能引起严重心理障碍,包括抑郁和焦虑。美国约有680万人患有斑秃,全球约有1.47亿人患有斑秃。
三 利特昔替尼的简要说明书(老挝)
【药品规格】50mg*28粒
【全部名称】利特昔替尼、利特昔替尼、Litfulo、LuciRit
【适应症】利特昔替尼(利特昔替尼)是一种激酶抑制剂,适用于治疗成人和12岁及以上青少年的重度斑秃。
【使用限制】不建议与其他 JAK 抑制剂、生物免疫调节剂、环孢菌素或其他强效免疫抑制剂联合使用。
【剂型和规格】胶囊:50mg*28片
【用法用量】使用利特昔替尼(利特昔替尼)治疗前应注意:
1、结核病 (TB) 感染:不建议活动性 TB 患者开始利特昔替尼(LITFULO)治疗。对于潜伏性 TB 患者或潜伏性 TB 检测阴性且 TB 风险较高的患者,在开始利特昔替尼(LITFULO)治疗前开始潜伏性 TB 的预防性治疗[见警告和注意事项]。
2、根据临床指南进行病毒性肝炎筛查:不建议乙型肝炎或丙型肝炎患者开始利特昔替尼(LITFULO)治疗[见警告和注意事项]。
3、淋巴细胞绝对计数 (ALC) 的患者不应开始利特昔替尼(LITFULO)治疗< 500/mm 3或血小板计数 < 100,000/mm 3[参见警告和注意事项]。
4、根据现行免疫接种指南更新免疫接种[参见警告和注意事项]。
一、推荐剂量
1、利特昔替尼(利特昔替尼)的推荐剂量为50 mg,口服,每日一次,可与或不与食物同服。
2、整粒吞服胶囊。请勿压碎、掰开或咀嚼胶囊。
3、如果漏服一剂药物,应尽快补服,除非距下次给药时间不足8小时,此时跳过漏服的剂量。此后,按照正常的服药时间恢复给药。
二、重度肝损害患者
不建议重度 (Child Pugh C) 肝损害患者使用利特昔替尼(LITFULO)。
【注意事项】
一、严重感染
在接受利特昔替尼(LITFULO)治疗的患者中报告了严重感染。最常见的严重感染为阑尾炎、COVID-19感染(包括感染性肺炎)和脓毒症 [参见不良反应]。在机会性感染中,利特昔替尼(LITFULO)组报告了多皮区带状疱疹。
活动性严重感染患者应避免使用利特昔替尼(LITFULO)。在以下患者中开始使用利特昔替尼(LITFULO)前,应考虑治疗的风险和获益:
1)伴有慢性或复发性感染
2)曾暴露于 TB
3)有严重感染或机会性感染史
4)居住在 TB 流行区或真菌病流行区或在该区旅行的患者
5)患有可能使其易患感染的基础疾病
在利特昔替尼(LITFULO)治疗期间和治疗后,密切监测患者是否出现感染的体征和症状。如果患者发生严重或机会性感染,则中断 利特昔替尼(LITFULO)治疗。对于在利特昔替尼(LITFULO)治疗期间发生新感染的患者,应及时进行免疫功能低下患者的全面诊断性检查,并开始适当的抗菌治疗,同时应对患者进行密切监测。一旦感染得到控制,可重新开始使用利特昔替尼(LITFULO)。
肺结核:开始治疗前筛查患者的结核病 (TB)。活动性 TB 患者不应使用利特昔替尼(LITFULO)。在新诊断为潜伏性 TB 或既往未经治疗的潜伏性 TB 患者中,应在开始利特昔替尼(LITFULO)治疗前开始抗结核治疗。在潜伏性 TB 检测阴性的患者中,对于高风险患者,在开始利特昔替尼(LITFULO)治疗前考虑抗结核治疗,并考虑在利特昔替尼(LITFULO)治疗期间筛查 TB 高风险患者。
病毒再活化:临床试验中报告了病毒再激活,包括疱疹病毒再激活病例(例如,带状疱疹)[参见不良反应]。如果患者出现带状疱疹,考虑中断治疗直至事件消退。
在开始利特昔替尼(LITFULO)治疗前,应按照临床指南进行病毒性肝炎筛查。有 HIV 感染或乙型肝炎或丙型肝炎感染证据的患者从临床试验中排除。
二、恶性肿瘤和淋巴增生性疾病
在利特昔替尼(LITFULO)临床试验中观察到恶性肿瘤,包括非黑色素瘤皮肤癌 (NMSC)[见不良反应]。
对于皮肤癌风险增加的患者,建议定期进行皮肤检查。
三、主要不良心血管事件
在另一种 JAK 抑制剂治疗50岁及以上有至少一种心血管风险因素的 RA 患者的大型、随机、上市后安全性研究中,与接受 TNF 阻滞剂治疗的患者相比,使用 JAK 抑制剂时观察到主要不良心血管事件(定义为心血管死亡、非致死性心肌梗死 (MI) 和非致死性卒中)的发生率更高。当前或既往吸烟者的风险增加。在开始或继续利特昔替尼治疗前,考虑个体患者的获益和风险,尤其是在当前或既往吸烟者以及具有其他心血管风险因素的患者中。应告知患者严重心血管事件的症状和发生时采取的步骤。发生心肌梗死或卒中的患者应停用利特昔替尼。
四:血栓栓塞:在一项大型、随机、上市后安全性研究中,使用另一种 JAK 抑制剂治疗50岁及以上有至少一种心血管风险因素的 RA 患者,观察到总体血栓形成、DVT和 PE 的发生率高于接受 TNF 阻滞剂治疗的患者。血栓形成风险可能增加的患者应避免使用利特昔替尼(LITFULO)。如果发生血栓形成或栓塞症状,患者应中断利特昔替尼(LITFULO)治疗,并及时接受评价和适当治疗。
五、过敏:在临床试验中接受利特昔替尼(LITFULO)的患者中观察到严重反应,包括过敏反应、荨麻疹和皮疹。如果发生具有临床意义的超敏反应,停用利特昔替尼(LITFULO)并进行适当的治疗。
六、实验室检查异常:利特昔替尼治疗与淋巴细胞和血小板减少相关。在开始利特昔替尼治疗前,进行 ALC 和血小板计数 [见用法用量]。开始利特昔替尼治疗后,根据 ALC 和血小板计数异常,建议中断或停止治疗[见用法用量]。
【特殊人群用药】
1、妊娠:如果患者在接受利特昔替尼(LITFULO)期间怀孕,应尽快咨询医生。在妊娠女性中使用 LITFULO 的临床试验的现有数据不足以确定。重大出生缺陷、流产或其他不良母体或胎儿结局的药物相关风险。在动物生殖研究中,根据曲线下面积 (AUC) 比较,在暴露量分别为最大推荐人用剂量 (MRHD) 的49倍和55倍时,在器官形成期对妊娠大鼠和家兔经口给予利妥昔单抗导致胎仔毒性和胎仔畸形。
2哺乳期:由于成人中的严重不良反应,包括严重感染和恶性肿瘤的风险,建议女性在利特昔替尼(LITFULO)治疗期间和末次给药后约14小时内(约6个消除半衰期)不要哺乳。
3、儿童用药:已在12岁及以上儿童患者中确定了利特昔替尼(LITFULO)治疗斑秃的安全性和有效性。尚未确定利特昔替尼(LITFULO)在12岁以下儿科患者中的安全性和疗效。
4、老年患者用药:≥65岁的患者无需调整剂量。利特昔替尼(LITFULO)的临床试验未纳入足够数量的65岁及以上患者,因此无法确定其反应是否与年轻成人患者不同。由于一般老年人群的感染发生率较高,因此治疗老年人时应谨慎。
5、肝损害:轻度 (Child Pugh A) 或中度 (Child Pugh B) 肝损害患者无需调整剂量。
不建议重度(Child Pugh C级)肝损害患者使用利特昔替尼(LITFULO)[见用法用量]。
【贮存方法】将利特昔替尼储存在20℃-25℃下,允许的波动范围为15℃-30℃。
【不良反应】1、头痛、腹泻、痤疮、皮疹、口腔炎
2、荨麻疹、毛囊炎、发热、特应性皮炎
3、头晕、血肌酸磷酸激酶升高、带状疱疹、红细胞计数降低
注:版权声明,本网站平台所有注明来源”医有我伴”的文字、图片和视频资料,版权均属于医有我伴网站所有,未经授权,任何媒体、网站或个人不得进行转载,否则将追究其法律责任。在取得书面授权转载时,须注明来源“医有我伴”,本平台所转载的文章目的是信息的传递,转载内容不代表本站立场。如有涉及请与我网站联系,进行删除。
如果本文对你有帮助,请给个关注并赞一下,【医有我伴】将持续分享优质内容
