各位专家同道好,本期CDM月评(第八十三期)将分享近期的肝硬化门静脉高压诊疗领域5篇文献(诊断监测3篇,多学科治疗2篇)。本期特邀月评专家:南京鼓楼医院感染科赵倩雯教授、首都医科大学附属北京市佑安医院肝病消化中心刘燕娜教授、天津市第三中心医院贾科峰教授、北京市大兴区人民医院消化内科张文辉教授。
 01 靶向门静脉中的5-羟色胺受体1A可减缓门静脉高压症
01 靶向门静脉中的5-羟色胺受体1A可减缓门静脉高压症Zhu CP, Liu SQ, Wang KQ, et al. Targeting 5-Hydroxytryptamine Receptor 1A in the Portal Vein to Decrease Portal Hypertension. Gastroenterology. 2024 Jun 19.
门静脉高压症(PH)是慢性肝病最常见的并发症之一。有研究者发现,肝硬化患者外周血中5-羟色胺(5-HT)水平升高。近日,来自海军军医大学长征医院的Zhu CP等人探讨了门静脉5-羟色胺受体1A(HTR1A)对PH的影响及其作用机制。相关内容发表在Gastroenterology杂志上。
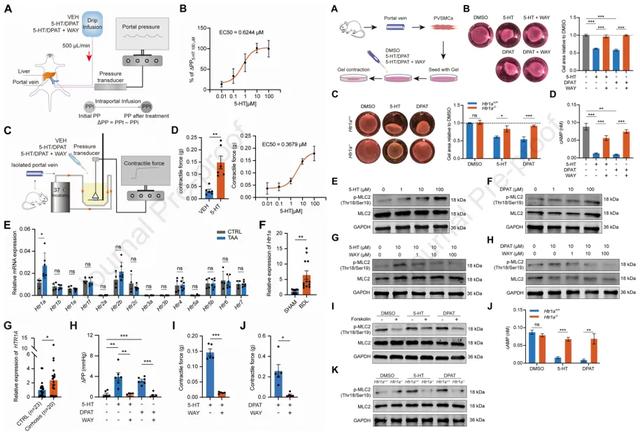
研究者采用硫代乙酰胺(TAA)注射、胆管结扎(BDL)或部分门静脉结扎(PPVL)诱导PH模型;采用实时荧光PCR、原位杂交和免疫荧光染色检测HTR1A的表达;通过门静脉内原位输注来评估5-HT、HTR1A激动剂8-OH-DPAT和HTR1A拮抗剂WAY-100635对门静脉压力(PP)的影响;利用Htr1a敲除(Htr1a-/-)大鼠和血管平滑肌细胞(VSMC)特异性Htr1a敲除(Htr1a-/-ΔVSMC)小鼠来证实HTR1A对PP的调节作用。
结果发现,HTR1A在PH大鼠模型及肝硬化患者中表达明显升高。此外,8-OH-DPAT增加了大鼠的PP,而WAY-100635降低了大鼠的PP,但均不影响肝纤维化和全身血流动力学改变。另外,5-HT或8-OH-DPAT可直接诱导离体门静脉(PV)的收缩。大鼠中的Htr1a基因缺失和小鼠中的VSMCs特异性Htr1a敲除可阻止PH的发展。而且,5-HT通过PV中的Htr1a触发cAMP途径介导的PV平滑肌细胞收缩。研究者还证实,HTR1A拮抗剂阿尔维林(alverine)在TAA-、BDL-和PPVL诱导的门脉高压大鼠中均有降低PP的能力。
因此,该研究结果表明,5-HT通过诱导PV收缩来促进PH,而HTR1A是一个有希望的治疗靶点。作为HTR1A拮抗剂,阿尔维林有望成为临床PH治疗的候选药物。
简评丨赵倩雯
南京鼓楼医院感染科
门静脉高压是慢性肝病最常见的并发症之一,同时也是肝硬化的主要结局,目前已成为肝硬化患者死亡的首要原因。然而针对肝硬化药物的研发仍处于探索阶段,因此可通过降低门静脉压力预防并发症的发生,从而改善患者预后。该研究团队探讨了门静脉中5-羟色胺受体1A(HTR1A)在降低门脉高压中的具体作用机制。
研究者发现5-羟色胺的表达不论在门脉高压大鼠模型中,还是在肝硬化患者中均显著上调,5-羟色胺可直接作用血管加速其收缩,且具有剂量依赖性,提示5-羟色胺可直接调控门静脉压。因此,确认5-羟色胺作用受体可作为治疗门脉高压的有效靶点。经筛选HTR1A是5-羟色胺加速血管收缩过程中的关键受体,同样仅在肝硬化人群中检测到HTR1A高表达,健康人群中几乎不表达。
为进一步确认HTR1A在门脉高压中的调控作用,研究者分别采用了HTR1A的激动剂8-OH-DPAT及拮抗剂WAY-100635,观察对门静脉压力的影响。结果显示,WAY-100635可显著抑制TAA及BDL诱导的大鼠门脉高压的发生,同样,8-OH-DPAT则会加速大鼠血管收缩,加剧门脉高压的发展。为进一步确认HTR1A是否是潜在治疗门脉高压的靶基因,研究者分别构建了全身敲除HTR1A大鼠(KO)和血管平滑肌细胞特异敲除HTR1A大鼠(CKO),结果均提示KO鼠和CKO鼠可显著减缓门脉高压的发展,这是通过抑制cAMP信号通路激活介导的血管收缩,降低门脉压来实现。
因此,研究者认为HTR1A有望成为治疗门脉高压的有效靶基因,设计并合成HTR1A拮抗药物可能是潜在的临床治疗门脉高压的重要手段。
02 脾脏硬度测量在排除门窦血管疾病患者高危静脉曲张中的作用Moga L, Paradis V, Ferreira-Silva J, et al. Performance of spleen stiffness measurement to rule out high-risk varices in patients with porto-sinusoidal vascular disorder. Hepatology. 2024 Jul 2.
Baveno VII 共识建议,当通过振动控制瞬时弹性成像(VCTE)测量到的脾脏硬度(SSM)≤40 kPa时,代偿期肝硬化患者的高危静脉曲张(HRV)率较低,因此可以免于内镜筛查检查。相反,所有门窦血管疾病(PSVD)的患者都需要进行内镜筛查。近日,来自巴黎西岱大学的Lucile Moga等人探讨了SSM-VCTE在PSVD和门静脉高压症患者中排除HRV的效果。详细内容发表在Hepatology杂志上。
该回顾性研究纳入了21个VALDIG中心的309例PSVD患者,这些患者存在至少1个以上的门静脉高压征象,无静脉曲张出血史,在上消化道内镜检查前后2年内接受SSM-VCTE。分别有154例患者纳入训练队列,155例患者纳入验证队列。
结果显示,训练队列中43%患者伴有HRV。通过多因素logistic回归分析发现,SSM-VCTE>40 kPa、血清胆红素≥1 mg/dL与HRV相关。SSM-VCTE≤40 kPa且胆红素<1 mg/dL,排除HRV的敏感性为96%,可以免去38%的内镜检查,HRV漏诊率为4%,阴性预测价值(NPV)为95%。在验证队列中,SSM联合胆红素可以节省21%的内镜筛查(HRV漏诊率为4%,NPV为94%)。
因此,SSM-VCTE≤40 kPa联合胆红素<1 mg/dL可鉴别出PSVD合并门脉高压患者,其HRV概率<5%,此类患者可免于进行内镜筛查。

简评丨刘燕娜
首都医科大学附属北京市佑安医院肝病消化中心
本研究探讨了在合并门静脉高压的PSVD患者中,基于振动控制瞬时弹性成像(VCTE)检测的脾脏硬度(SSM)无创排除高危静脉曲张(HRV)的准确性。研究最终提出了一个基于SSM及血清总胆红素水平(TBIL)的模型,即SSM≤40 kPa且TBIL<17 μmol/L的患者存在HRV的概率<5%,因此利用该模型可用于除外HRV发生,使患者免于内镜检查。
门静脉肝窦血管性疾病(PSVD)是由欧洲肝脏血管病研究组(VALDIG)在2019年提出的新概念,其提出是建立在临床上存在肝脏活检病理符合非肝硬化性门静脉高压特征、但无门静脉高压相关临床及实验、影像学表现患者的背景上。目前对于合并门静脉高压的PSVD患者,其管理主要是按照肝硬化门静脉高压相关指南进行。然而,由于发病机制不尽相同,针对肝硬化门静脉高压患者所提出诊断临床显著性门静脉高压、HRV的标准可能并不适用于PSVD人群。
随着新概念的提出,近年来PSVD相关研究是肝病领域的“小众”热点之一。本研究的优势在于一方面聚焦临床上少见的一类门静脉高压类型,另一方面是已发表SSM诊断HRV相关主题研究中样本量最大的,且排除HRV诊断的准确性最高。此外,研究的验证队列来自欧洲20家单位,一定程度上肯定了该模型的可靠性。与肝硬化门静脉高压人群不同的是,模型最终未纳入血小板(PLT),而是纳入TBIL,可能原因是研究人群有25%的患者原发病为血液系统疾病,因此可能影响PLT的水平。相比已受到大量验证的Baveno VII标准,该模型的准确性仍有待进一步在其他人群背景及更大样本队列中验证。对于PSVD患者,无创诊断相关预后事件如临床显著性门静脉高压、HRV等,将会是未来研究的热点之一。
03 小直径支架的经颈静脉肝内门体静脉分流术联合静脉曲张栓塞治疗胃静脉曲张:一项多中心队列研究Xia Y, Tie J, Wang G, et al. Small Transjugular Intrahepatic Portosystemic Shunt Plus Variceal Embolization for Gastric Varices: A Multicenter Cohort Study. Clin Gastroenterol Hepatol. 2024 May 16.
目前,经颈静脉肝内门体静脉分流术(TIPS)联合静脉曲张栓塞术(VE)治疗胃静脉曲张(GV)的效果仍存在争议。近日,来自山东省立医院的Xia Y等人探讨了在小直径(8 mm支架)TIPS上联合VE是否可以降低不同类型GV患者的再出血发生率。相关内容发表在Clin Gastroenterol Hepatol杂志上。
该回顾性队列研究纳入了7家医疗中心接受8 mm支架TIPS治疗胃底静脉曲张的629名患者。主要终点是全因再出血,次要终点包括显性肝性脑病(OHE)和全因死亡率。
共纳入629名患者,其中,429名(68.2%)患有1型胃食管静脉曲张(GOV1),145名(23.1%)患有2型胃食管静脉曲张(GOV2),55名(8.7%)患有1型孤立性胃静脉曲张(IGV1)。在整个队列中,与单独进行TIPS相比,联合辅助栓塞降低了再出血率(6.2% vs. 13.6%;P=0.005)和OHE(31.0% vs. 39.4%;P=0.02)。然而,死亡率差异无统计学意义(12.0% vs. 9.7%;P=0.42)。对于GOV2和IGV1患者的亚组分析显示,TIPS联合VE术可降低再出血率(GOV2:7.8% vs. 25.1%;P=0.01;IGV1:5.6% vs. 30.8%;P=0.03)和OHE率(GOV2:31.8% vs. 51.5%;P=0.008;IGV1:11.6% vs. 38.5%;P=0.04)。然而,对于GOV1患者,联合VE术无法降低TIPS后再出血率(5.9% vs. 8.7%;P=0.37)或OHE率(33.1% vs. 35.3%;P=0.60)。
因此,与单纯进行TIPS相比,8毫米支架的TIPS联合VE术可减少GOV2和IGV1患者的术后再出血和OHE。这些发现表明,与GOV1患者相比,GOV2和IGV1患者可从TIPS联合栓塞术中获益。

简评丨贾科峰
天津市第三中心医院
既往TIPS术中联合曲张静脉栓塞一直是临床常规做法,但在覆膜支架时代TIPS术中是否联合曲张静脉栓塞,尤其是当门静脉压力梯度(PPG)降至12 mmHg以下时,一直是个具有争议的话题。在临床实际中当PPG低于12 mmHg时仍存在胃静脉出血的情况,表明TIPS术中联合胃静脉曲张栓塞可有效避免再出血,但缺乏大规模临床研究数据证实。
该全国多中心研究共纳入629例接受TIPS治疗的患者,全因再出血为研究的主要终点,次要终点为显性肝性脑病(OHE)的发生和死亡率。相比6 mm、8-10 mm及12 mm直径支架,8 mm支架在国内TIPS术中更为常用。研究发现在小直径(8 mm)TIPS中加入静脉曲张栓塞可显著减少GOV2和IGV1患者的再出血和OHE发作,没有证据表明对GOV1患者有额外的益处。提示临床医师可以依据胃静脉曲张类型选择TIPS或TIPS+E。
该研究的局限性:(1)该研究排除了门静脉伴有血栓的患者,临床上门静脉血栓患者的比例并不低,限定了结果的应用;(2)研究中并没有排除伴有较大分流道的患者,因为对于伴有较大分流的GOV2和IGV1患者而言,栓塞的作用可能更大,会明显影响术后再出血及OHE的发作。
04 TIPS术后患者肺内血管扩张的高患病率和临床相关性Mauz JB, Rieland H, Berliner D, et al. High Prevalence and Clinical Relevance of Intrapulmonary Vascular Dilatations in Patients Undergoing TIPS Implantation. Clin Gastroenterol Hepatol. 2024 May 9.
选择恰当的患者对于确保经颈静脉肝内门体分流术(TIPS)实施后的最佳效果至关重要。然而,关于肺内血管扩张(IPVD)或肝肺综合征(HPS)对TIPS置入后临床病程的影响缺乏相应数据。近日,来自德国汉诺威的Mauz JB等人探讨了TIPS置入术患者IPVD与HPS的相关性,相关内容发表在Clin Gastroenterol Hepatol杂志上。
该研究共纳入265例患者;采用超声心动图造影及血气分析方法检测患者是否存在IPVD和HPS,其中136例为IPVD,71例符合HPS标准;采用多因素竞争风险分析评估随访1年内心脏失代偿(CD)、肝失代偿(HD)和无肝移植(LTx)生存。
结果显示,IPVD患者TIPS后Freiburg生存指数(FIPS)评分较低,肌酐较低,更因静脉曲张出血而经常接受TIPS。IPVD的存在与CD(HR:1.756,95%CI:1.011-3.048,P=0.046)和HD(HR:1.841,95%CI:1.255-2.701,P=0.002)的发生率显著升高相关。然而,IPVD患者和非IPVD患者的无LTx生存率相当(HR:1.081,95%CI:0.630-1.855,P=0.780)。HPS患者表现出更多CD(HR:1.708,95%CI:0.935-3.122,P=0.082)和HD(HR:1.458,95%CI:0.934-2.275,P=0.097)的趋势,但未达到统计学意义。HPS患者与非HPS患者的无LTx生存率无差异(HR:1.052,95%CI:0.577-1.921,P=0.870)。
因此,实施TIPS前筛查IPVD有助于进一步识别心脏和肝脏失代偿风险较高的患者。

简评丨贾科峰
天津市第三中心医院
肝硬化和门静脉高压引起的并发症如腹水或静脉曲张出血的患者治疗选择有限。如果不能进行肝移植,TIPS术已成为临床上最常用的治疗方法。其目的是通过减轻门静脉压力,降低进一步失代偿的风险,提高生存率。但相当一部分患者在TIPS术后容易出现心脏失代偿(CD)及肝脏失代偿(HD)等并发症,这些患者中伴发肺血管扩张(IPVD)及肝肺综合征(HPS)的比例不低。例如该研究中报道51%的患者伴有IPVD,36%的患者患有HPS。这部分患者接受TIPS术后是否会导致失代偿风险进一步增加,进而影响生存是临床医生比较顾忌和担忧的。
该研究发现患有IPVD的患者TIPS术后CD及HD的发生率显著增加,其中85%的CD严重程度为轻度至中度,临床可以通过加强利尿剂来控制。主要的HD是腹水和肝性脑病,部分患者需要调整TIPS支架直径,然而这部分患者并未导致死亡率增加。患有HPS的患者TIPS术后,CD和HD的发生率也增加,但未达到统计学意义,HPS患者与非HPS患者的无肝移植生存率无差异。本研究为临床医师提出了警示:在TIPS术前筛查IPVD有助于进一步识别心脏和肝脏失代偿风险较高的患者。
但该研究存在一些局限性,例如,接受TIPS治疗的患者大多数失代偿会发生在术后前3个月内,例如研究中提到的,术后出现CD、HD的中位时间分别为32天、33天。现有很多研究报道小直径的TIPS支架,可降低短期内失代偿事件的发生。但该研究中绝大多数患者使用的支架直径为8-10 mm,需要辨析术后失代偿事件的发生是因为支架直径的选择还是术前伴有IPVD、HPS导致的。
05 在丙型肝炎病毒相关肝硬化患者中,血管性血液病因子与ADAMTS13的比值是持续病毒学应答后食管胃底静脉曲张进展的有效预测指标Iwai S, Akahane T, Takaya H, et al. Ratio of von Willebrand factor to ADAMTS13 is a useful predictor of esophagogastric varices progression after sustained virologic response in patients with hepatitis C virus-related liver cirrhosis. Hepatol Res. 2024 Jun 5.
食管胃底静脉曲张(EGV)是丙型肝炎病毒(HCV)相关肝硬化(HCV-LC)的严重并发症。在大多数情况下,通过直接抗病毒(DAA)治疗实现持续病毒学应答(SVR)后,门静脉高压症会得到改善。然而,在某些情况下,在HCV消除后仍会发生EGV恶化。近日,来自日本奈良医科大学的Satoshi Iwai等人研究了血管性血液病因子(VWF)和具有血小板反应蛋白1型基序13的去整合素样金属蛋白酶(ADAMTS13)是否可以预测达到SVR后HCV-LC的EGV进展。详细内容发表在Hepatol Res杂志上。
该项回顾性研究纳入了47名经DAA治疗后达到SVR的HCV-LC患者。18名患者在达到SVR后出现EGV进展(EGV进展组)。29名患者在达到SVR后未出现EGV进展(无EGV进展组)。在DAA治疗前一天测量血浆VWF抗原水平和ADAMTS13活性。
结果显示,EGV进展组的血浆VWF抗原水平(P=0.00331)和VWF/ADAMTS13比值(P=0.000249)显著高于无EGV进展组。多因素logistic回归模型发现,VWF/ADAMTS13比值>2.3是SVR后EGV进展的唯一危险因素([HR:18.4,95%CI:3.08-109,P=0.00138)。观察期间,VWF/ADAMTS13比值>2.3的患者在实现SVR后EGV进展的累积发生率明显高于比值≤ 2.3的患者(HR:6.4,95%CI:1.78-22.96,P=0.0044)。
因此,HCV DAA治疗前VWF与ADAMTS13的比值可预测SVR达成后的EGV进展。

简评丨张文辉
北京市大兴区人民医院消化内科
食管胃静脉曲张(EGV)是肝硬化的一个严重并发症,高达85%的肝硬化患者在某个时间点会出现EGV。丙型肝炎病毒相关肝硬化(HCV-LC)也是如此。在大多数情况下,HCV-LC门静脉高压症在使用DAA治疗达到持续病毒学应答(SVR)后得到改善;然而,在某些情况下,即使清除了HCV,EGV仍有恶化。但不管是HVPG还是内镜,都属于侵入性操作,如何通过微创或无创的方法来预测EGV的出现和恶化仍然是困扰临床医生、研究者的热点问题。
该研究的特色之处是在DAA治疗前一天测定血浆VWF抗原水平和ADAMTS13活性,同时用内镜评估EGV情况。结果发现基线VWF/ADAMTS13>2.3的患者在SVR达到后EGV进展的累积发生率显著高于比值≤ 2.3的患者,因此得出结论DAA治疗HCV前的VWF/ADAMTS13比值可以预测达到SVR后的EGV进展。同时,考虑到EV和GV血流动力学的差异,该研究也发现在EV和GV进展组,该比值均明显增高。而通过该指标对患者进行分层,可以避免低危患者进行不必要的内镜检查。
但该研究也存在一些局限性:(1)样本量较小(一共47名患者,18名出现EGV进展,29名无进展);(2)为单中心的回顾性、观察性研究,未进行验证性队列研究;(3)诊断门静脉高压的依据体格检查、实验室结果及影像学,未测量患者的HVPG。
