2024年11月17日,亚盛医药宣布,其自主研发的新型选择性BCL-2抑制剂APG-2575(力胜克拉片、Lisaftoclax)的新药上市申请(NDA)已获国家药品监督管理局(NMPA)药品审评中心(CDE)受理,并被推荐纳入优先审评程序,用于治疗难治或复发性(r/r)慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)。值得一提的是,这是首个在国内提交NDA的国产原研BCL-2抑制剂,有望成为全球第二个上市的BCL-2抑制剂。维奈克拉是全球首款且唯一获批的BCL-2抑制剂。
APG-2575是亚盛医药在研的新型口服BCL-2选择性小分子抑制剂,通过选择性抑制BCL-2蛋白来恢复肿瘤细胞程序性死亡机制(细胞凋亡),从而诱导肿瘤细胞凋亡,达到治疗肿瘤的目的。

通用名:力胜克拉片、Lisaftoclax
代号:APG-2575
厂家:亚盛医药
美国首次获批:尚未获批
中国首次获批:尚未获批
临床数据
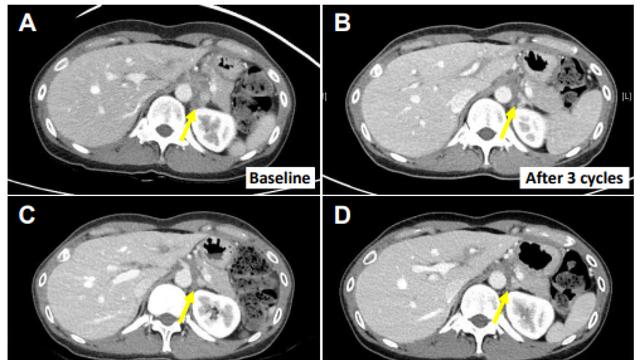
此次提交的NDA是基于一项在中国开展的关键注册II期临床研究(APG2575CC201)结果。该研究旨在评估APG-2575单药治疗难治或复发性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤患者的有效性和安全性。研究的主要终点指标为总缓解率(ORR)。
在2024年第66届美国血液学会(ASH)年会上,亚盛医药公布了APG-2575单药或联合阿可替尼或利妥昔单抗治疗初治、复发/难治性或既往接受过维奈克拉治疗的慢性淋巴细胞白血病/小淋巴细胞淋巴瘤的新临床数据。2020年3月20日至2024年6月27日期间,共纳入了176例患者,其中单药组46例;联合利妥昔单抗组39例;联合阿可替尼组91例。
结果显示,在87例接受APG-2575联合阿可替尼治疗的患者中,客观缓解率(ORR)为96.6%,中位缓解持续时间(DOR)和中位无进展生存期(PFS)均未达到。12个月和18个月的PFS率分别为89%和86%。
在安全性方面,所有队列中常见的任何级别治疗相关不良反应(TEAEs)包括:中性粒细胞减少(33.5%)、腹泻(21.6%)、贫血(15.3%)和血小板减少(14.8%)。≥3级TEAEs在单药组、联合利妥昔单抗组和联合阿可替尼组中分别为中性粒细胞减少(32.6%、25.6%、24%)、贫血(21.7%、12.8%、13.2%)。
小结
总的来说,BCL-2抑制剂APG-2575在慢性淋巴细胞白血病/小淋巴细胞淋巴瘤患者中具有单药和联合治疗潜力,有望为难治或复发性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤患者提供一种安全有效的治疗选择。
【重要提示】所有文章信息仅供参考,具体治疗谨遵医嘱!